Nat. Commun. | 机制驱动AI新策略:设计专门攻击MRSA持留细胞的抗菌肽
Nat. Commun. | 机制驱动AI新策略:设计专门攻击MRSA持留细胞的抗菌肽

DrugOne
发布于 2026-03-25 16:28:35
发布于 2026-03-25 16:28:35
DRUGONE
研究人员提出了一种用于设计抗菌肽的机制驱动人工智能框架CAMPER(Constraint-driven AMP Engineering with Ranking),该方法将机器学习预测与生物物理评分相结合,用于优先筛选能够破坏细菌膜结构的短肽,从而有效清除耐甲氧西林金黄色葡萄球菌(MRSA)的持留细胞和生物膜。通过该框架,研究人员从候选肽库中筛选得到12肽长度的WP-CAMPER1,该分子在体外对金黄色葡萄球菌表现出较强抑菌活性,并在小鼠皮肤感染模型中显著降低细菌负荷。进一步研究表明,其D-构型变体在生物膜感染模型和深部感染模型中均能有效清除持留细胞。单细胞微流控实验显示,该肽能够杀死指数生长期的持留细菌,证明机制型人工智能可用于开发针对耐药和持留菌的新型抗菌肽。

抗菌药物耐药性已成为全球公共卫生的重要威胁,金黄色葡萄球菌尤其是耐甲氧西林菌株在医院和社区感染中广泛存在,并常导致败血症、肺炎和骨感染等严重疾病。除耐药外,该菌还能形成生物膜并进入低代谢状态形成持留细胞,使传统抗生素难以发挥作用,导致慢性感染和复发。因此,开发能够杀死持留菌的新型抗菌策略十分迫切。
抗菌肽是一类具有潜力的候选分子,它们通常通过破坏细菌膜而发挥作用,因此不依赖细菌代谢状态,对持留细胞和生物膜同样有效。然而,传统的抗菌肽设计主要依赖经验性调控电荷、疏水性和螺旋结构等参数,难以在庞大的序列空间中高效筛选。近年来,机器学习被用于抗菌肽预测,但多数方法只依赖统计相关性,缺乏对膜作用机制的约束,导致筛选结果在生物学上不一定可行。
为解决这一问题,研究人员提出一种机制型人工智能策略,将机器学习模型与生物物理约束评分结合,通过同时考虑统计预测和膜作用机制,从而优先筛选具有真实膜破坏能力的抗菌肽,并专门用于靶向持留细胞和生物膜。
方法
研究人员构建了CAMPER框架,该方法包含两个核心部分:首先使用基于随机森林的机器学习分类器预测肽的抗菌活性,其训练数据来自已知抗菌肽数据库,并利用理化性质和结构特征进行表征;随后引入生物物理评分函数,对候选肽按照净电荷、疏水性、疏水矩和螺旋倾向等关键参数进行排序,以确保所筛选分子符合膜破坏型抗菌肽的机制特征。通过这一双重筛选流程,研究人员能够在大规模候选肽库中优先选择具有膜靶向活性并可能对持留菌有效的序列,并进一步通过体外实验、单细胞分析和动物模型验证其抗菌效果。
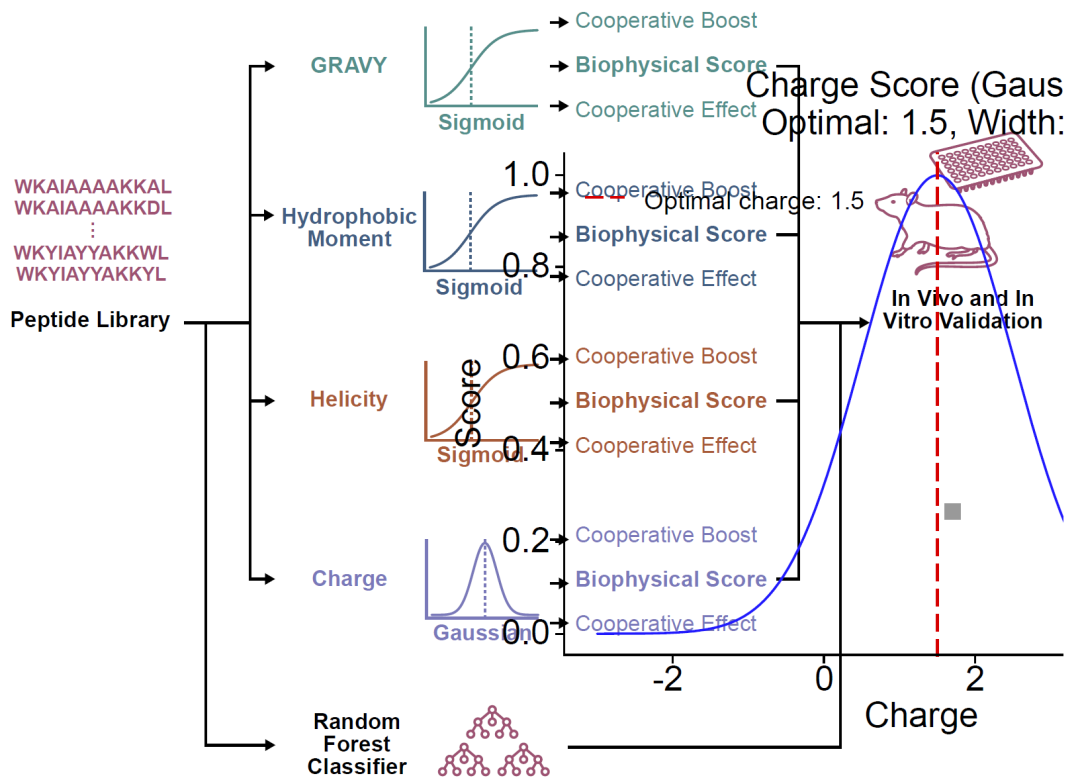
图1:CAMPER抗菌肽优先筛选流程概览。
结果
CAMPER框架构建与模型性能
研究人员建立了一个由机器学习分类器和生物物理评分组成的双模块筛选流程,并利用包含数千条抗菌肽序列的数据集训练模型。结果显示,随机森林模型能够较准确预测抗菌活性,而加入生物物理评分后,假阳性显著减少,使筛选结果更加符合膜作用型抗菌肽的特征。该方法在疏水性、螺旋结构和电荷分布等关键特征空间中表现出更高的精确度,从而提高了候选分子的可靠性。
候选肽筛选与体外抗菌活性验证
研究人员将CAMPER应用于基于天然肽模板构建的候选库,并合成排名最高的五条肽序列进行实验验证。结果表明,排名第一的WP-CAMPER1具有较强抗菌活性,在不同盐浓度、pH条件和血清存在时仍保持稳定抑菌能力。进一步的结构-活性关系分析显示,该肽的电荷和疏水性接近最佳平衡,过度增加任一性质反而降低活性,说明CAMPER能够筛选出接近最优理化参数的序列。
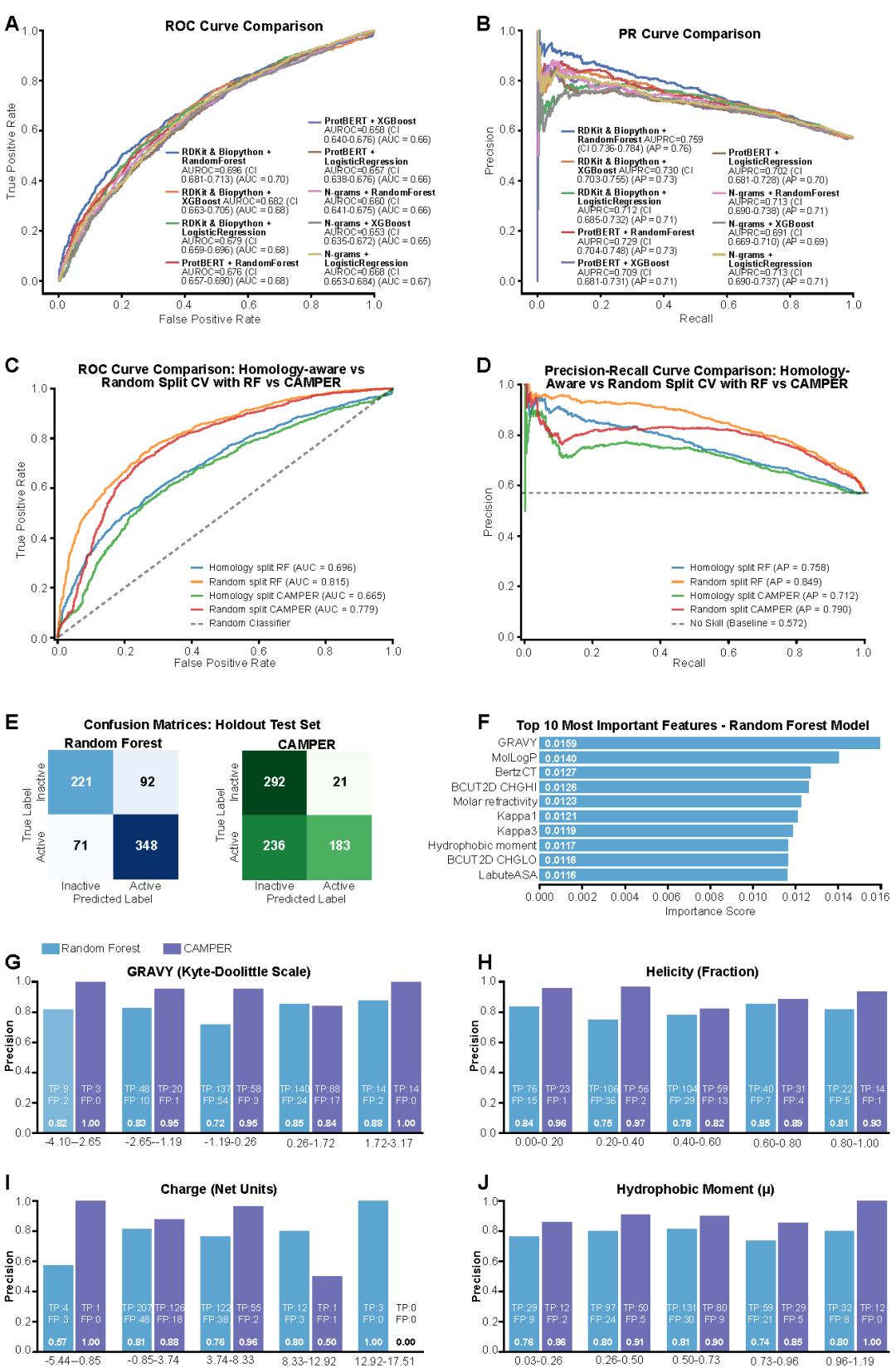
图2:分类器性能、同源性感知评估、特征重要性分析及CAMPER在生物物理特征空间中的预测精度。
对持留细胞和生物膜的杀菌能力
实验结果显示,WP-CAMPER1不仅能杀死指数生长期细菌,还能快速清除静止期持留细胞,并对耐药菌株同样有效。在生物膜模型中,该肽能够抑制生物膜形成并破坏成熟生物膜,显著降低细菌数量,表现出优于常规抗生素的活性,证明膜破坏机制能够有效对抗耐药和休眠状态细菌。
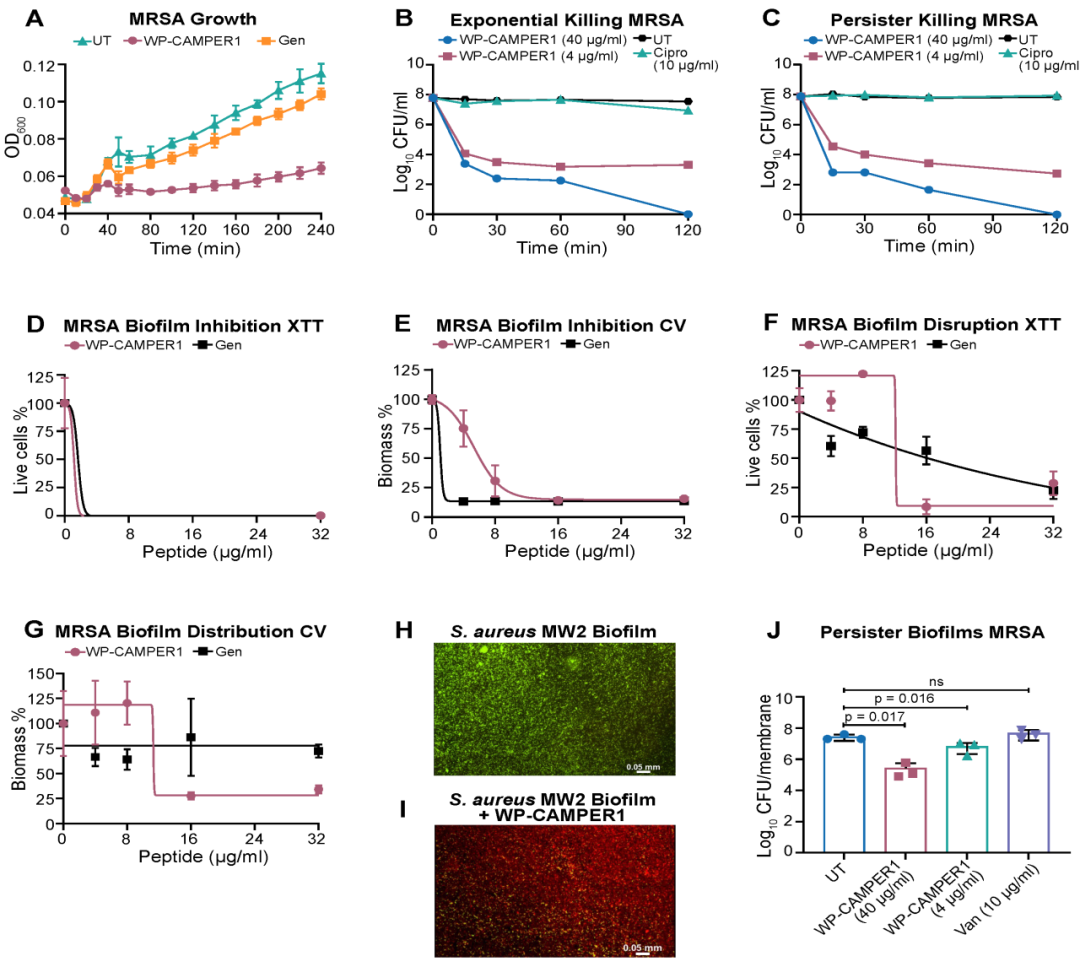
图3:WP-CAMPER1在体外对金黄色葡萄球菌MW2的指数期、持留状态及生物膜相关细胞的生长抑制和杀菌活性。
膜作用机制验证
结构分析和分子动力学模拟表明,WP-CAMPER1在膜环境中形成α螺旋结构并插入脂质双层。荧光染料实验、膜电位检测和电子显微镜观察均显示该肽能够破坏细菌膜完整性,并诱导活性氧生成和能量代谢紊乱。转录组分析进一步表明,该肽影响多条与膜功能和能量代谢相关的通路,支持其以膜破坏为主的杀菌机制。
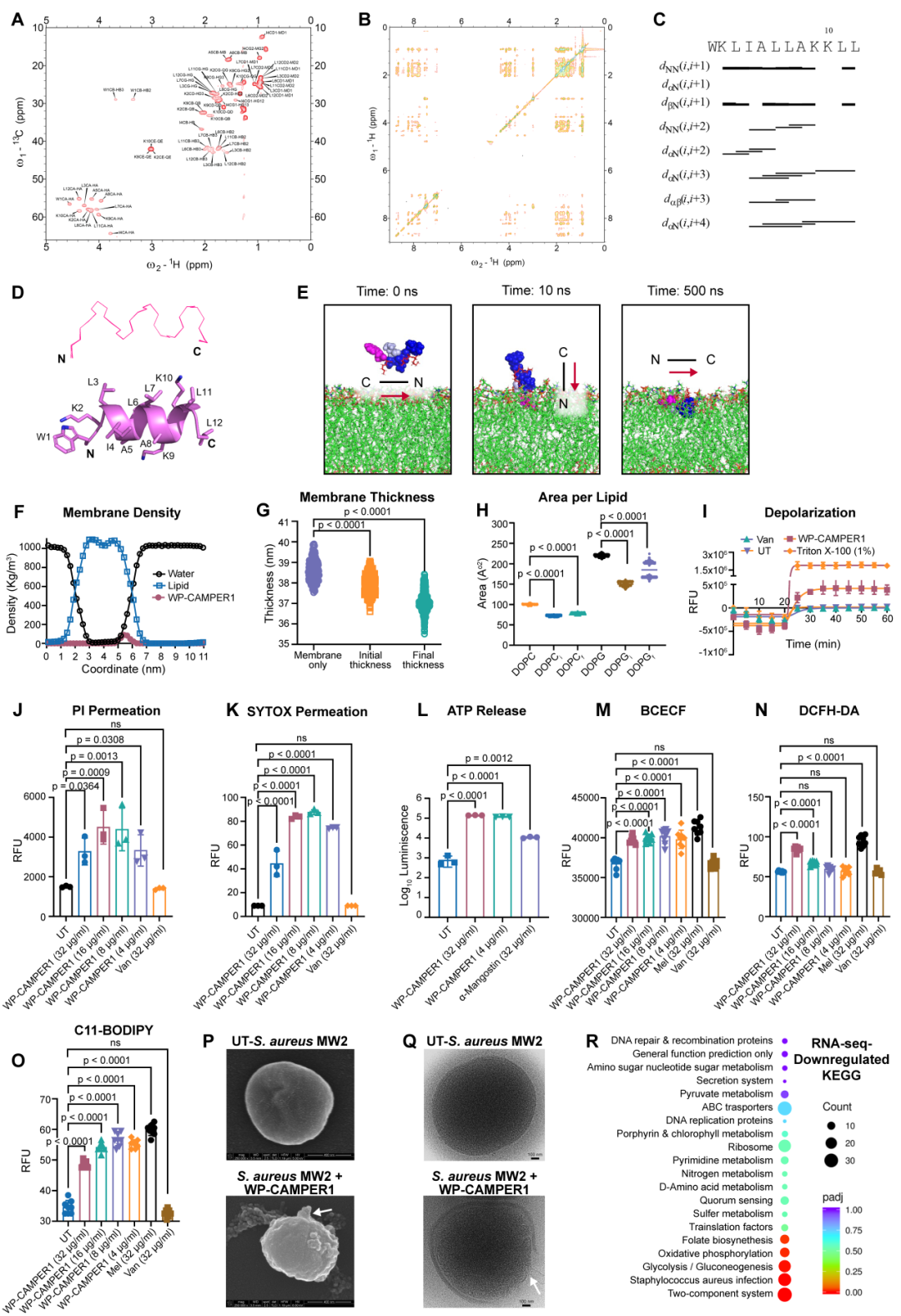
图4:WP-CAMPER1靶向细菌膜的结构与生物物理机制解析。
动物模型与D-构型肽的抗持留效果
在小鼠皮肤感染模型中,WP-CAMPER1显著降低细菌负荷,而D-构型变体具有更好的稳定性和持续杀菌能力。在单细胞微流控实验中,该肽能够清除极少数存活的持留细胞。在深部感染模型中,D-构型肽显著减少持留菌数量,而常规抗生素效果有限,说明该策略具有潜在临床应用价值。
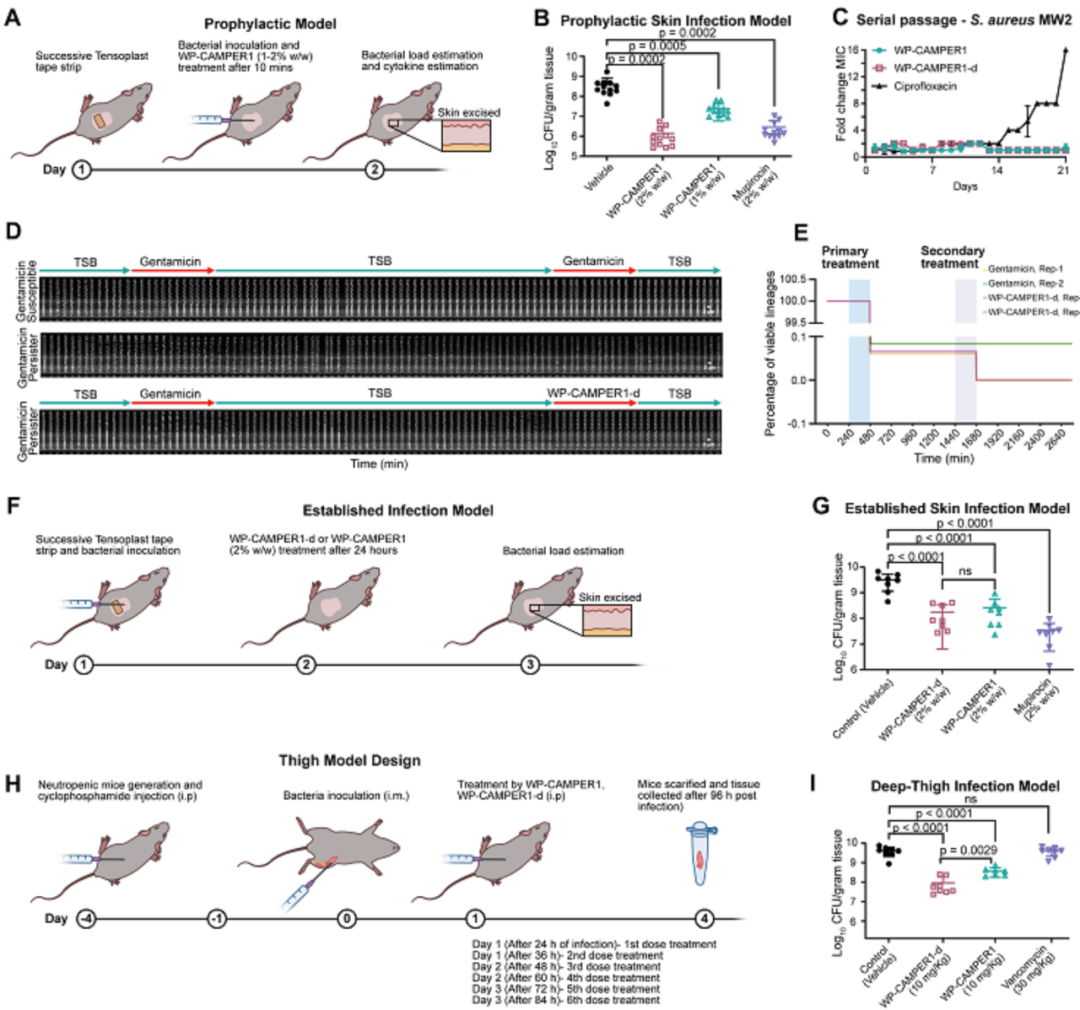
图5:WP-CAMPER1及其D-构型在小鼠皮肤感染模型、单通道微流控系统和深部股部感染模型中的体内抗金黄色葡萄球菌MW2效果评估。
讨论
本研究提出的CAMPER框架展示了机制驱动人工智能在抗菌肽设计中的优势。与传统机器学习方法不同,该方法不仅依赖统计预测,还通过生物物理约束保证候选分子具有明确的膜破坏机制,从而提高筛选效率并减少无效合成。实验结果表明,CAMPER能够设计出短而稳定的抗菌肽,对耐药菌、生物膜和持留细胞均具有显著活性,并在动物模型中显示出良好疗效。
研究人员认为,膜靶向抗菌肽是一种有前景的抗感染策略,而将机器学习与机制约束结合,可以显著提升新型抗菌分子的发现效率。该框架具有良好的通用性,可应用于不同微生物靶点或不同设计目标,并可与其他生成模型或进化策略结合,用于未来抗菌药物开发。
整理 | DrugOne团队
参考资料
Shehadeh, F., Mishra, B., Ferrer-Espada, R. et al. CAMPER: mechanistic artificial intelligence for designing peptides that target MRSA persisters. Nat Commun (2026).
https://doi.org/10.1038/s41467-026-70348-9
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-03-13,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

