Nat. Mach. Intell. | SequenTx: 基于强化学习的肿瘤演化驱动序贯药物治疗设计
Nat. Mach. Intell. | SequenTx: 基于强化学习的肿瘤演化驱动序贯药物治疗设计

DrugOne
发布于 2026-03-25 14:29:50
发布于 2026-03-25 14:29:50
DRUGONE
肿瘤细胞在癌症进展及治疗过程中会不断发生演化,表现为细胞状态的动态变化与显著的异质性。因此,如何理解这种复杂的细胞动态,并据此设计能够针对肿瘤演化过程的治疗策略,是肿瘤治疗中的关键问题。研究人员提出了一种名为 SequenTx 的计算框架,该方法受到人工智能虚拟细胞理念的启发,将肿瘤细胞模型与强化学习相结合,用于设计针对不同肿瘤类型和多种药物的序贯治疗策略。该方法利用基于转录组扰动数据构建的模型来模拟药物诱导的肿瘤细胞状态变化,并通过强化学习探索能够产生协同疗效的药物给药顺序。
在多种实体瘤细胞系中的大规模体外实验验证显示,SequenTx 预测的序贯治疗组合中约33%(102种组合中的34种)表现出明显疗效。在体内实验中,研究人员进一步证明 BET 抑制剂预处理能够提高黑色素瘤模型对奥沙利铂的敏感性。转录组分析表明,初始药物可持续改变癌细胞的转录状态,从而增强后续药物的治疗效果并产生协同作用。此外,该框架揭示了一种具有普遍意义的序贯治疗策略,即先使用表观遗传抑制剂,再使用其他抗癌药物。整体而言,SequenTx 为理解肿瘤演化及其治疗提供了一种新的计算框架,可帮助设计更加合理的序贯抗癌疗法。

癌症的发展往往伴随着基因转录程序的稳定激活或抑制,这种变化会推动正常细胞向肿瘤细胞转化。在癌症进展和治疗过程中,肿瘤细胞会在不同细胞状态之间发生动态转变,从而形成高度的肿瘤异质性和表型可塑性。药物诱导的转录变化往往能够持续存在,使肿瘤细胞逐渐获得耐药性,并最终导致疾病进展。因此,仅依赖单一药物治疗通常难以获得长期疗效。
近年来,人工智能虚拟细胞技术的发展使得模拟复杂细胞动态成为可能。借助这种预测能力,研究人员可以在计算机中模拟肿瘤在治疗压力下的状态演化,并据此设计新的治疗策略。在肿瘤学研究中,序贯治疗被认为是一种重要策略,即按照特定顺序依次使用不同药物,而非同时联合给药。已有研究表明,一些治疗效应具有明显的时间依赖性,需要与细胞生物学过程同步才能产生最佳效果。例如,“一击两段式”治疗策略通过先诱导肿瘤细胞衰老,再利用第二种药物清除这些细胞,从而获得显著疗效。
尽管实验研究已经证明序贯治疗具有潜力,但目前相关研究往往局限于少数药物和少数肿瘤类型,因此迫切需要一种统一的计算框架来系统探索不同药物顺序、不同给药时间以及不同肿瘤状态之间的复杂关系。
方法概述
为了解决上述问题,研究人员开发了 SequenTx 框架。该方法将序贯药物治疗问题建模为一个序列决策问题,并通过强化学习进行求解。在该框架中,肿瘤细胞状态由转录组表达谱表示,而药物则被视为对细胞状态的扰动。研究人员利用 L1000 基因表达数据来刻画肿瘤细胞在药物作用下的状态变化,并构建肿瘤细胞模型来预测基因表达和细胞存活率的变化。
在强化学习框架中,系统被形式化为一个马尔可夫决策过程。模型的状态为肿瘤细胞的基因表达谱,动作是选择某种药物进行治疗,而奖励函数则由两个部分组成:治疗效果奖励和序贯协同奖励。前者反映药物对细胞数量的抑制作用,后者衡量序贯用药相对于单药治疗所产生的额外协同效应。
SequenTx 由两个核心模块组成:一是肿瘤细胞模型,用于模拟药物扰动下细胞状态的变化;二是强化学习智能体,用于在不断变化的肿瘤状态下选择最优药物序列。系统通过多次训练强化学习模型,并从多个随机初始化中筛选出表现最好的模型,最终生成有效的序贯药物组合列表。
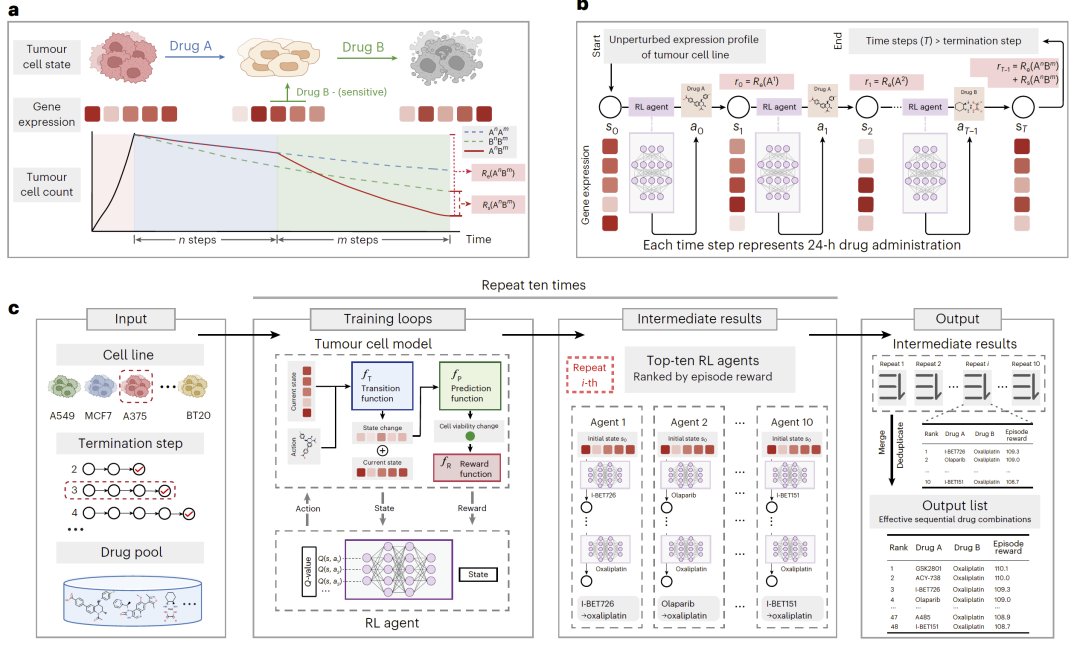
图1:SequenTx 框架概览。
结果
SequenTx框架概览
序贯药物治疗设计可以被视为在不断变化的肿瘤状态下进行的一系列决策过程。研究人员通过强化学习智能体,根据肿瘤细胞当前的基因表达状态逐步选择药物,从而形成完整的治疗序列。每一步代表一次24小时的药物给药周期。通过不断模拟不同药物组合及其顺序,SequenTx 能够在巨大的治疗策略空间中寻找具有协同效应的药物组合。
SequenTx的计算模拟与性能评估
研究人员首先评估了肿瘤细胞模型在预测药物扰动转录组变化方面的能力。在随机划分数据集的情况下,模型预测的表达变化与实验数据之间的平均相关系数约为0.49。当测试集中包含未见过的药物时,模型仍能保持较高预测能力;而在测试集中包含新的细胞系时,预测准确度有所下降,表明细胞系本身的转录背景对预测具有重要影响。
进一步与多种先进模型进行比较后发现,该状态转移模型在多个评估指标上具有竞争力,并在预测新细胞系方面表现更优。此外,研究人员还构建了细胞存活率预测模型,其预测结果与实验数据之间的相关系数达到0.59。通过这些模型,SequenTx 能够有效模拟肿瘤细胞在不同药物组合下的动态变化。
在强化学习训练过程中,智能体逐渐学会选择更有效的药物组合,其奖励值随训练过程不断提高。与随机生成的药物序列相比,SequenTx 预测的序贯药物组合在协同效应和治疗效果两个指标上均显著优于随机策略。
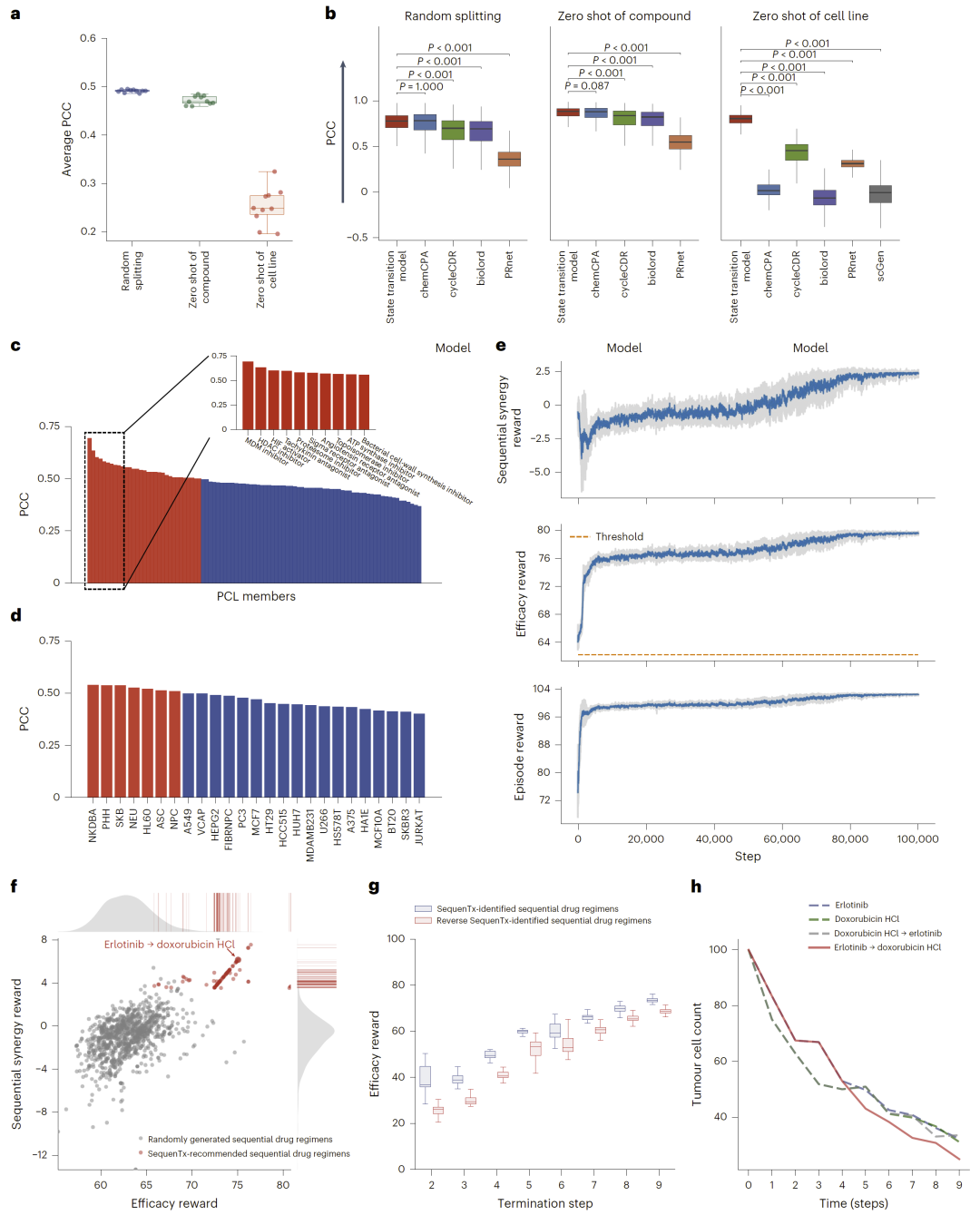
图2:SequenTx 的计算机模拟(in silico)评估与性能验证。
不同肿瘤细胞系中的序贯治疗规律
研究人员进一步分析了 SequenTx 在不同细胞系中预测的序贯药物组合,以回答三个关键问题:药物A的治疗时间如何影响药物B的疗效,哪些细胞状态对协同效应至关重要,以及序贯治疗中第一种药物是否具有特定类型偏好。
研究发现,药物A的给药时间长度对药物B的疗效具有明显影响,不同组合呈现出多种趋势模式。例如,在某些情况下,延长药物A的处理时间会逐渐增强药物B的疗效,而在其他情况下则会出现先增强后减弱的趋势。
通过对转录组通路进行富集分析,研究人员发现某些细胞状态在产生序贯协同效应中尤为关键,特别是与 DNA复制、细胞周期和细胞衰老相关的生物学通路。这表明,某些药物可以通过诱导特定细胞状态,使肿瘤细胞对后续治疗更加敏感。
进一步分析还发现,在许多有效序贯治疗方案中,第一种药物往往属于 组蛋白乙酰化抑制剂或拓扑异构酶抑制剂。这些药物能够显著改变细胞的转录程序,从而为后续药物创造更加有利的治疗条件。

图3:SequenTx 识别的序贯药物组合分析。
体外实验验证
为了验证 SequenTx 的预测结果,研究人员在六种癌细胞系中进行了大规模体外实验,对 102 种序贯药物组合进行了测试。实验结果显示,其中 34 种组合表现出明显协同作用,总体成功率约为 33%。当第一种药物能够显著改变转录状态时,成功率进一步提高至 42%。
研究人员还重点研究了表观遗传药物作为序贯治疗第一步的策略。实验表明,BET 抑制剂 I-BET726 或 I-BET151 的预处理能够显著提高肿瘤细胞对奥沙利铂的敏感性。此外,顺序给药通常比反向给药具有更强的抑制作用,进一步证明了药物顺序的重要性。
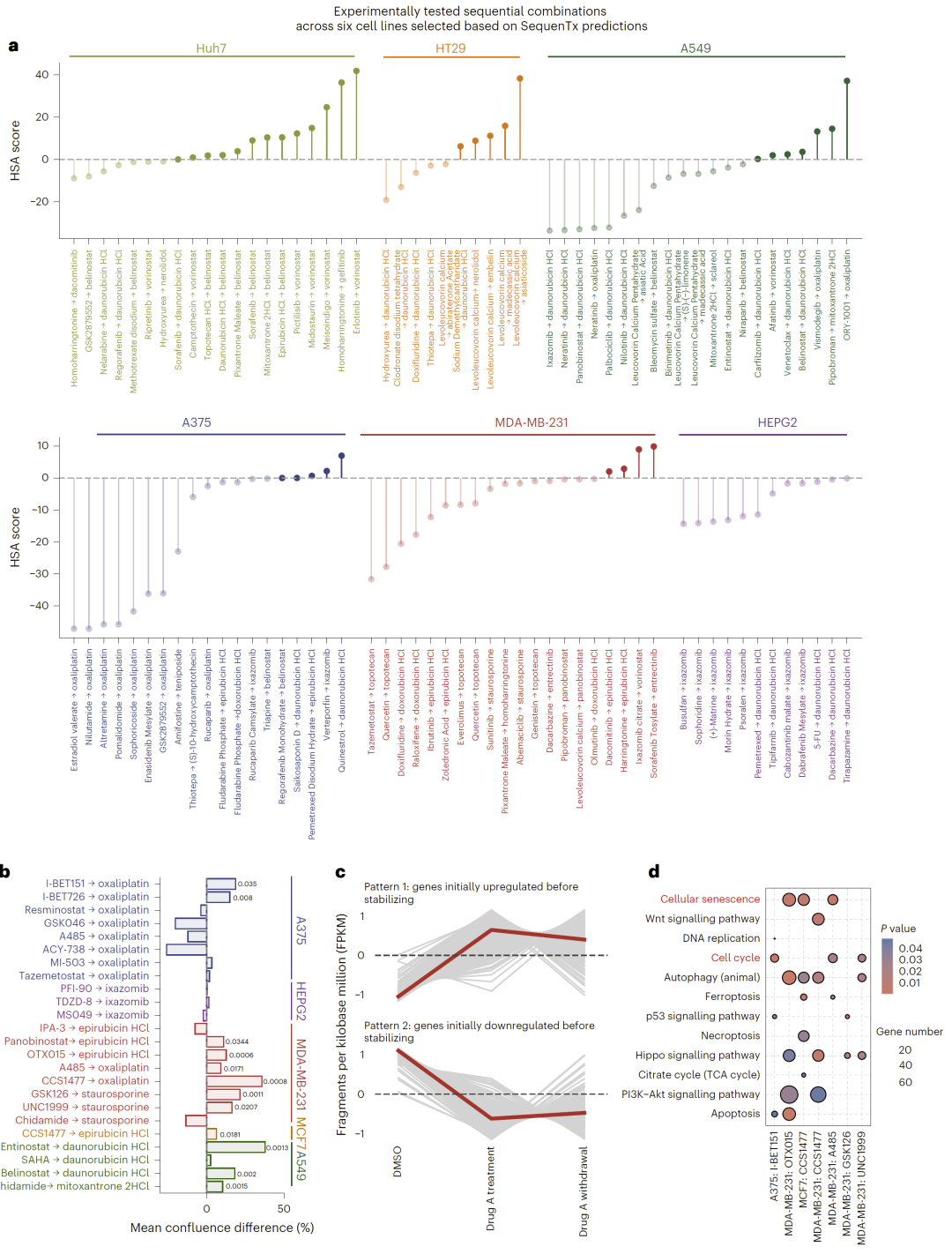
图4:SequenTx 在序贯治疗中的体外实验验证。
转录组机制分析
RNA测序分析表明,某些药物诱导的基因表达变化在药物撤除后仍然保持稳定,这些变化主要集中在细胞周期和细胞衰老相关通路。说明序贯治疗的关键机制在于第一种药物改变了肿瘤细胞的转录状态,使其进入对第二种药物更加敏感的状态。
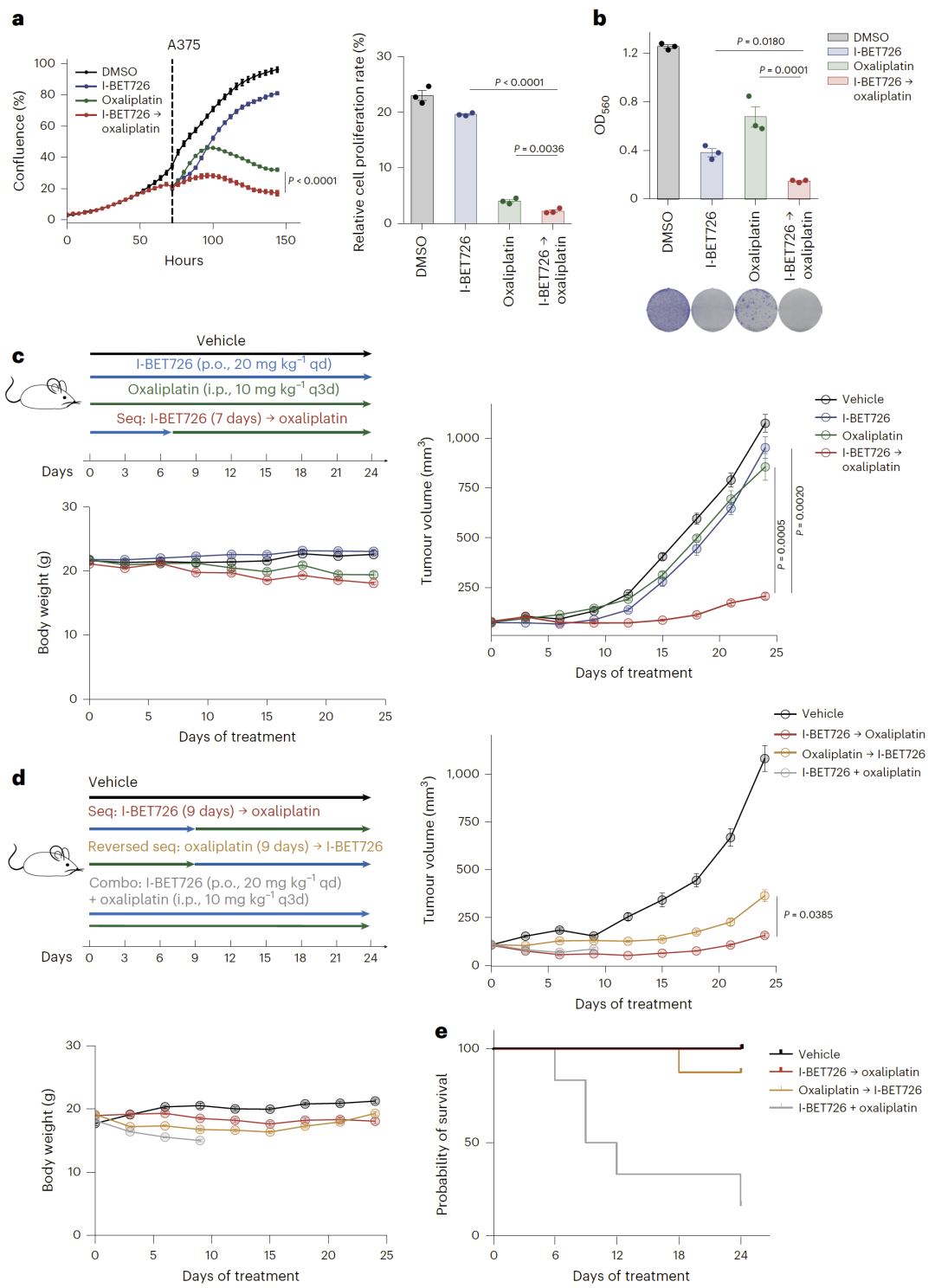
图5:I-BET726 与奥沙利铂的序贯治疗可有效抑制 A375 黑色素瘤细胞的增殖。
动物模型验证
在黑色素瘤异种移植模型中,研究人员验证了 I-BET726 与奥沙利铂的序贯治疗方案。实验结果显示,与单药或联合给药相比,序贯治疗能够显著抑制肿瘤生长并延长生存时间,进一步证明了 SequenTx 在真实生物系统中的应用潜力。
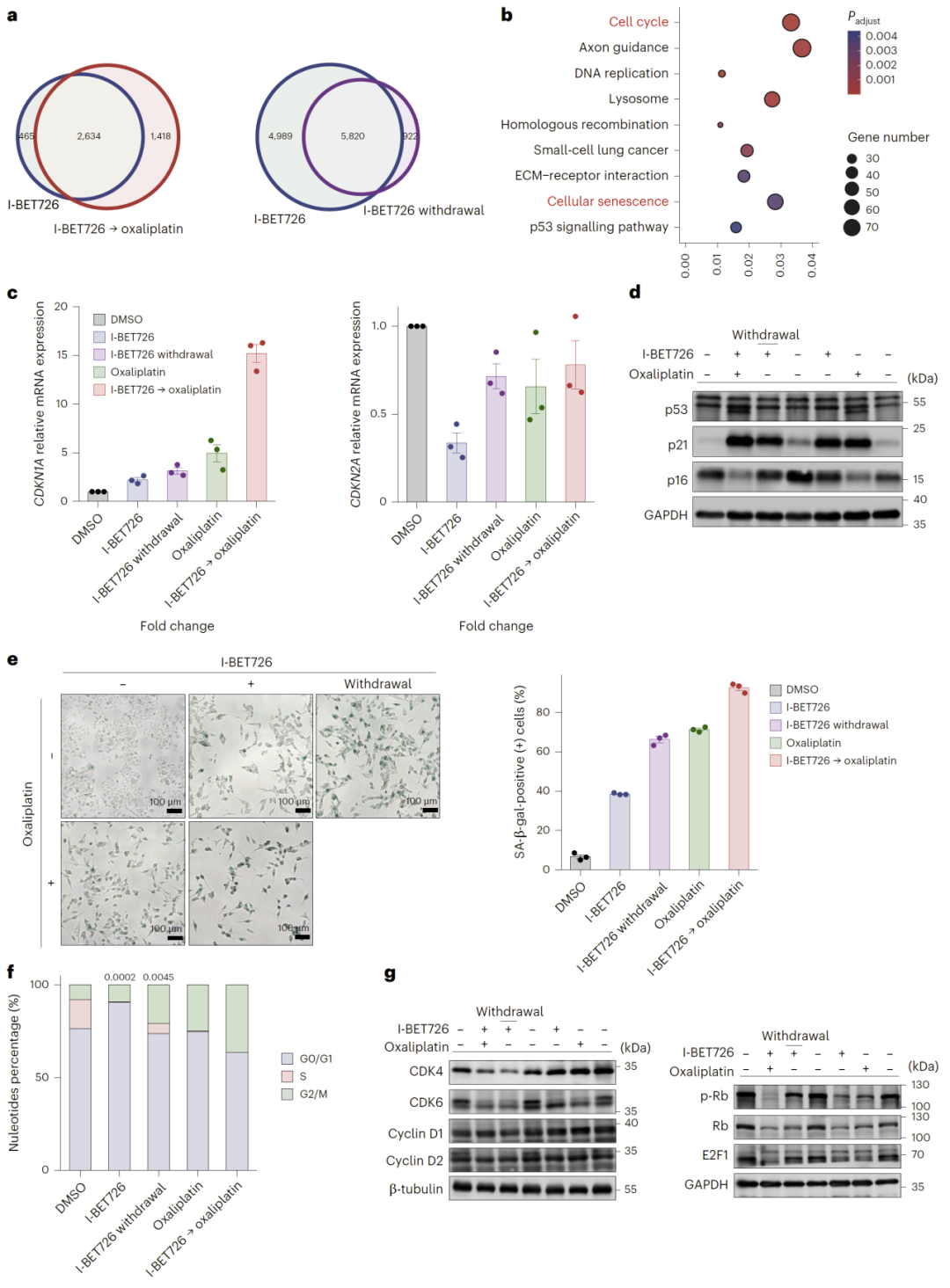
图6:I-BET726 在 A375 细胞中诱导细胞衰老表型,从而增强其对奥沙利铂治疗的敏感性。
讨论
该研究提出了一种结合强化学习与虚拟细胞建模的新型计算框架,用于设计针对肿瘤演化过程的序贯药物治疗策略。与传统联合治疗相比,序贯治疗能够利用药物诱导的转录变化,使肿瘤细胞逐步进入更易被后续药物攻击的状态,从而产生更强的治疗效果。
SequenTx 的研究结果表明,肿瘤治疗中的关键并不仅仅是选择哪些药物,而是如何合理安排药物的给药顺序和时间。特别是能够改变转录状态的表观遗传药物,在序贯治疗中可能具有重要作用。通过将强化学习与转录组数据相结合,该框架能够在巨大的药物组合空间中系统探索潜在的治疗策略。
总体而言,SequenTx 为理解肿瘤演化与治疗策略之间的关系提供了新的计算工具,并为未来开发更加精准的抗癌治疗方案提供了重要思路。
整理 | DrugOne团队
参考资料
Chen, X., Deng, Y., Yang, X. et al. Reinforcement learning-based design of sequential drug treatment targeting the evolving tumour landscape with SequenTx. Nat Mach Intell (2026).
https://doi.org/10.1038/s42256-026-01192-1
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-03-06,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

