J. Med. Chem. | 基于结构的三维小分子药物生成:我们到达了吗?
J. Med. Chem. | 基于结构的三维小分子药物生成:我们到达了吗?

DrugAI
发布于 2026-01-06 13:46:33
发布于 2026-01-06 13:46:33
DRUGONE
基于结构的药物设计(Structure-Based Drug Design, SBDD)在临床前药物发现中起着核心作用。近年来,研究人员开发了一系列基于三维结构的生成式算法,可根据蛋白结合口袋结构自动生成新颖且具有药物样特征的小分子。然而,这些算法生成的化合物在化学合理性(chemical plausibility)上的评价体系仍不完善。研究人员在本研究中提出了两种新的指标,用于评估生成分子的化学合理性,并证明部分算法会生成化学上不合理的结构,其分布特征与已知药物分子显著不同。通过在三种代表性靶点(c-SRC 激酶、Smoothened 受体、D1 多巴胺受体)上进行高通量虚拟筛选对比,研究人员发现这些新指标有助于揭示生成分子的不足,并为提升药物样性和可合成性提供指导。

药物发现过程漫长且成本高昂,因此如何加速先导化合物设计始终是药物化学的核心问题。生成式人工智能(Generative AI)的出现为这一领域带来了新的可能性——它能够学习蛋白–配体相互作用规律,并直接在三维空间生成与靶点结合的候选分子。
基于结构的生成模型通过学习蛋白–配体复合物数据(如 PDBbind、BindingNet、CrossDocked 等),可以在蛋白结合口袋的几何与化学约束下生成新分子(图1)。然而,目前缺乏有效指标来评估生成分子的化学合理性与药物样性,导致这些方法虽在对接得分上表现良好,但在化学稳定性、可合成性等方面仍存在严重偏差。
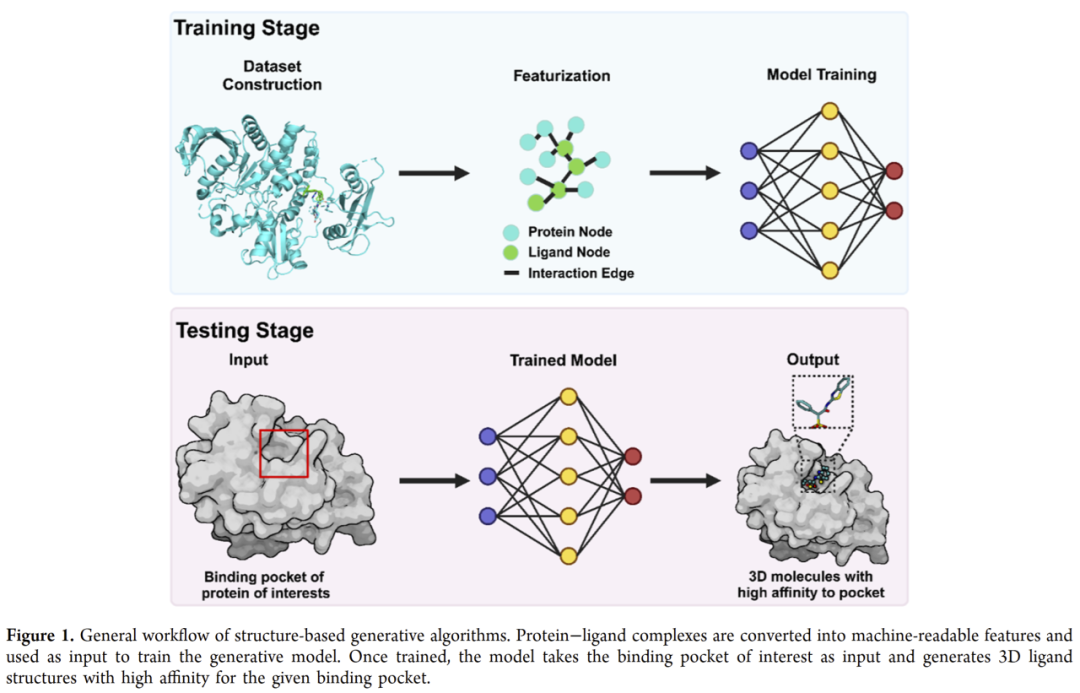
图1 | 基于结构的三维生成算法总体流程
方法概述
现有结构驱动生成模型主要在三方面存在差异:
- 三维表示方式(如体素网格、原子坐标、欧氏距离矩阵);
- 领域知识整合(如药效团信息、氢键或疏水作用模式);
- 生成策略(自回归逐步生成或一次性扩散生成)。
这些模型通常以口袋结构条件为输入,优化 Docking 得分。然而,仅使用对接得分、QED 或 SA 等传统指标无法全面反映化学合理性。研究人员因此引入新的定量评估体系。
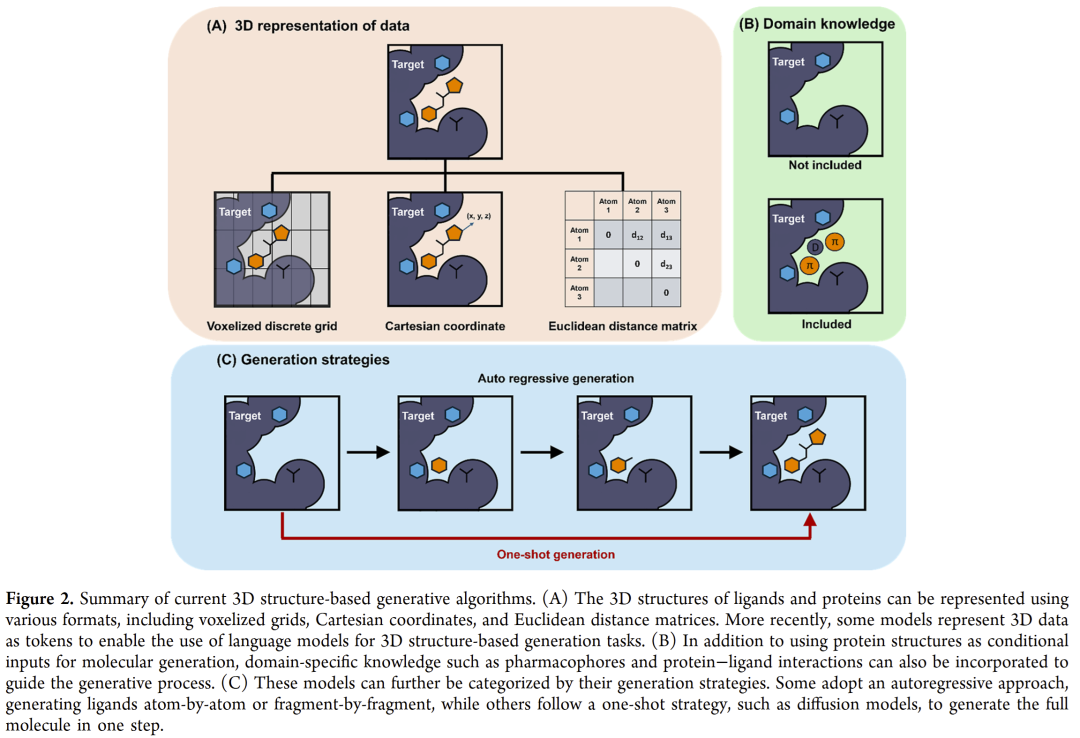
图2 | 现有三维结构生成算法的分类与特征
结果
生成分子的化学合理性分析
研究人员针对七种典型算法(3DSBDD、Pocket2Mol、TargetDiff、DecompDiff、PMDM、DecompOpt、MolSnapper)进行了系统评估,并以三组对照数据(FDA 批准药物、ChEMBL 临床化合物、CrossDocked 数据集)作为参考。
结果表明,生成分子的药物样性普遍低于对照组。通过引入三个指标(ChEMBL 环系统出现频率、ZINC20 与 ZINC22 骨架匹配率),发现超过一半的生成分子未能通过任何一个标准。
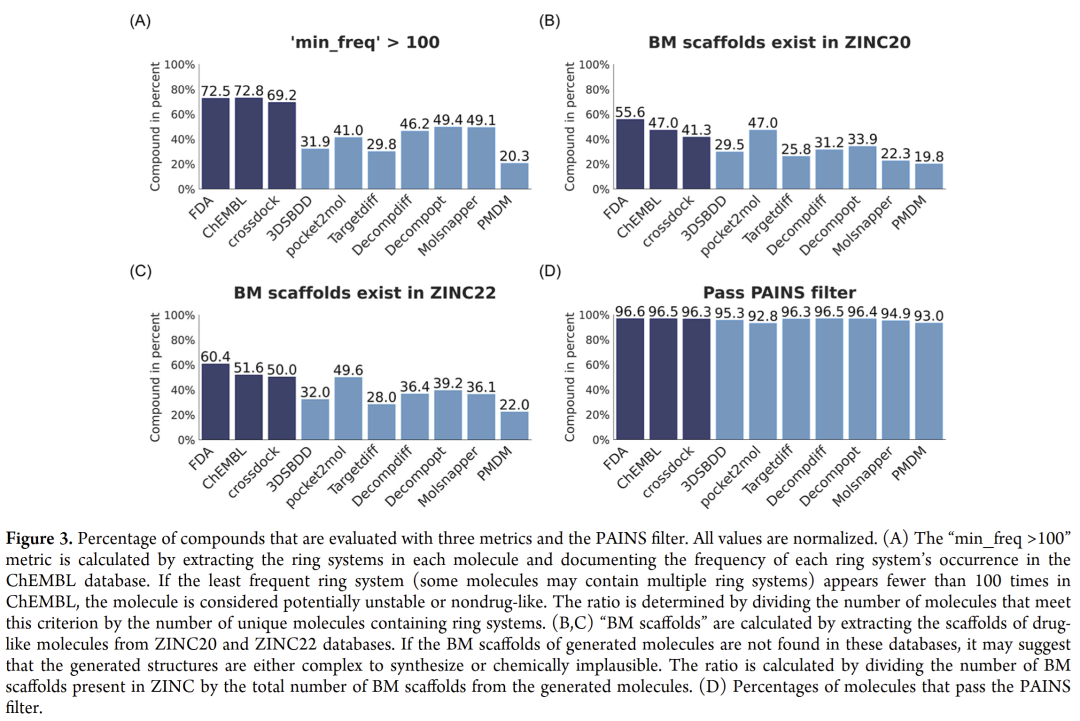
图3 | 生成分子的化学合理性评估指标分布
性质分布差异与结构异常分析
研究人员进一步分析了生成分子的理化性质分布(分子量、环数、手性原子、可旋转键等),并绘制雷达图进行比较。
与真实药物相比,生成分子普遍表现为:
- 芳香环过少而脂环过多;
- 分子量偏低或手性中心过多;
- 含有不合理的键型(如 sp 杂化碳位于五元环中)。
这些现象揭示了模型对化学规律学习不足的问题。
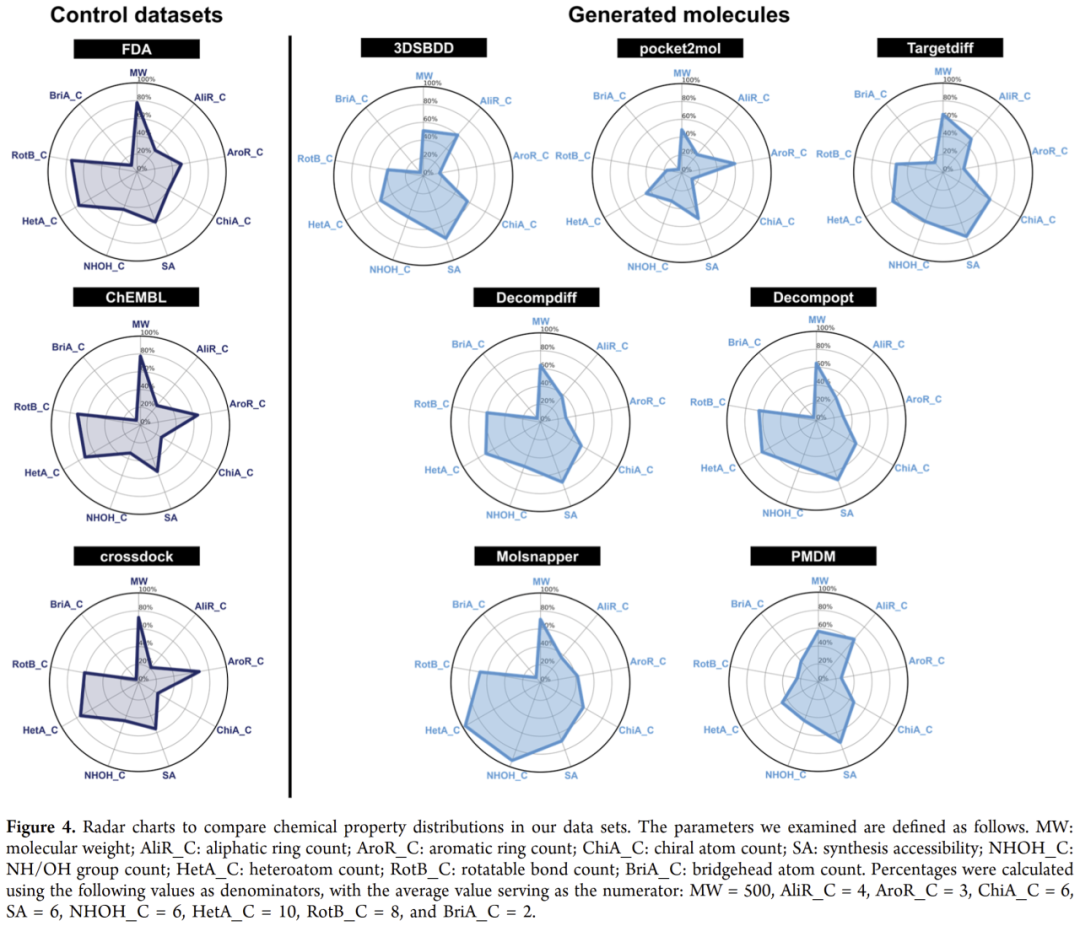
图4 | 分子属性的分布对比雷达图
化学不合理性的来源
研究人员指出三类主要原因:
- 化学不稳定结构的出现(如高张力环或非法杂化键);
- 环系统偏差(过多脂环、缺乏芳香性导致平面性不足);
- 过度复杂的手性中心与氢键供体基团。
这些因素综合导致生成分子虽在对接能量上优异,却在化学合理性与合成可行性方面明显不足。
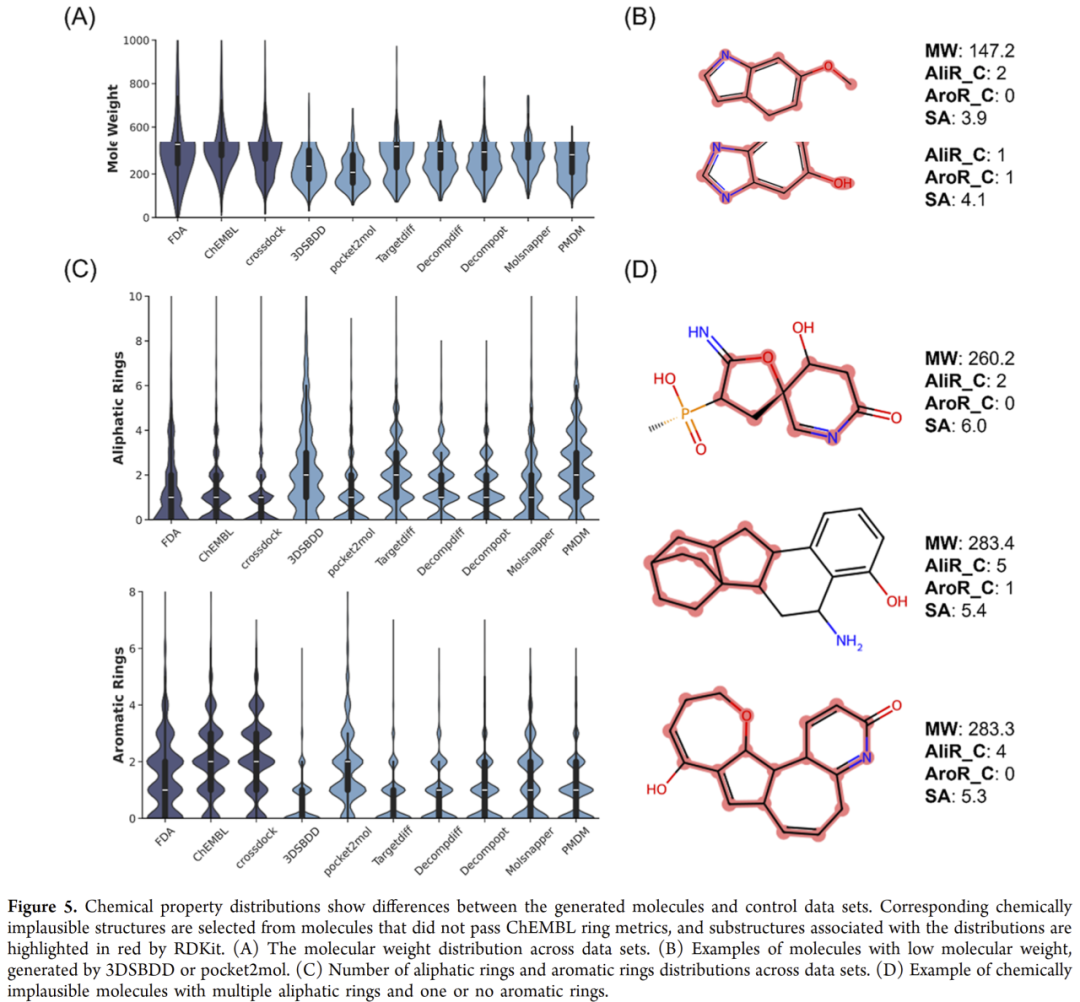
图5 | 分子量与环系统分布的差异与示例
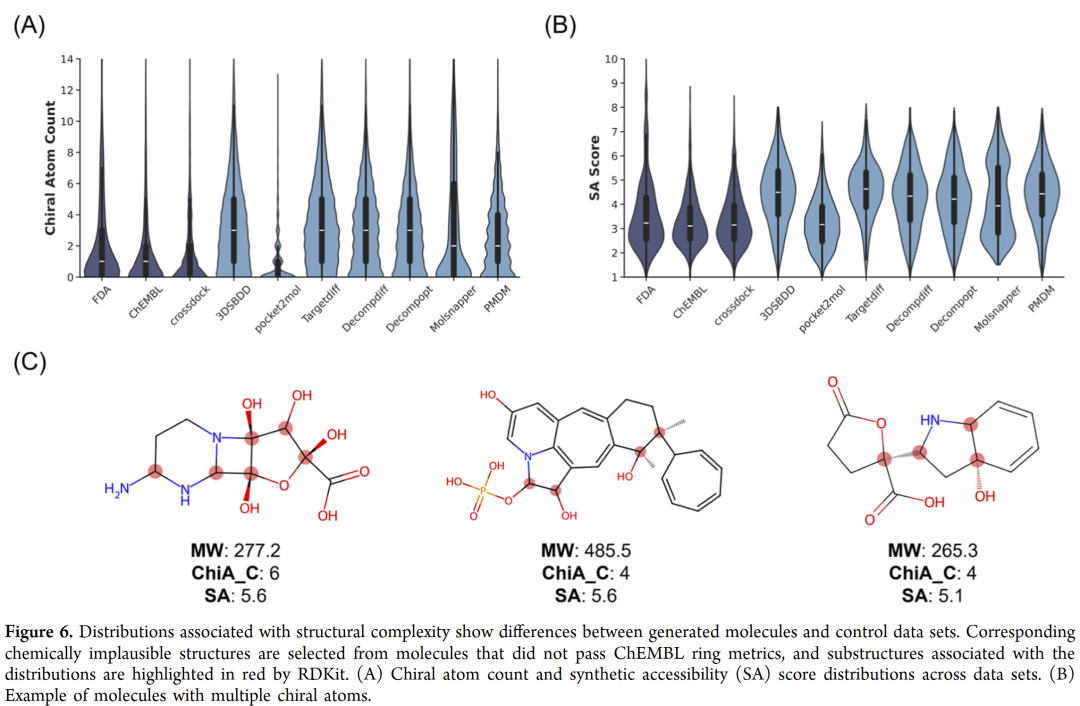
图6 | 结构复杂性与可合成性分析
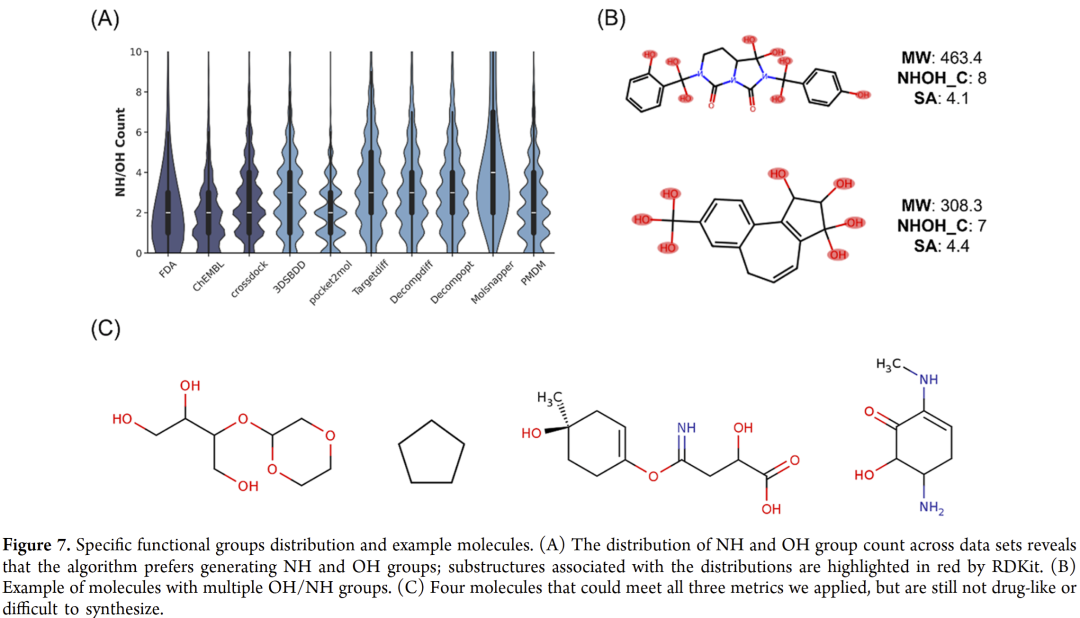
图7 | NH/OH 基团过度富集现象与示例
与高通量虚拟筛选(HTVS)的比较
研究人员选取了三个典型靶点(C-Src、Smoothened、D1 受体),比较生成模型与 HTVS 在对接得分与化学合理性上的表现。结果显示:
- 生成模型在对接得分上略优于平均水平,但劣于 HTVS 前500个命中分子;
- 仅约 55% 的生成分子通过骨架匹配指标,而 HTVS 命中率更高;
- MolSnapper 模型在效率与准确性上略优,尤其在引入药效团信息后。
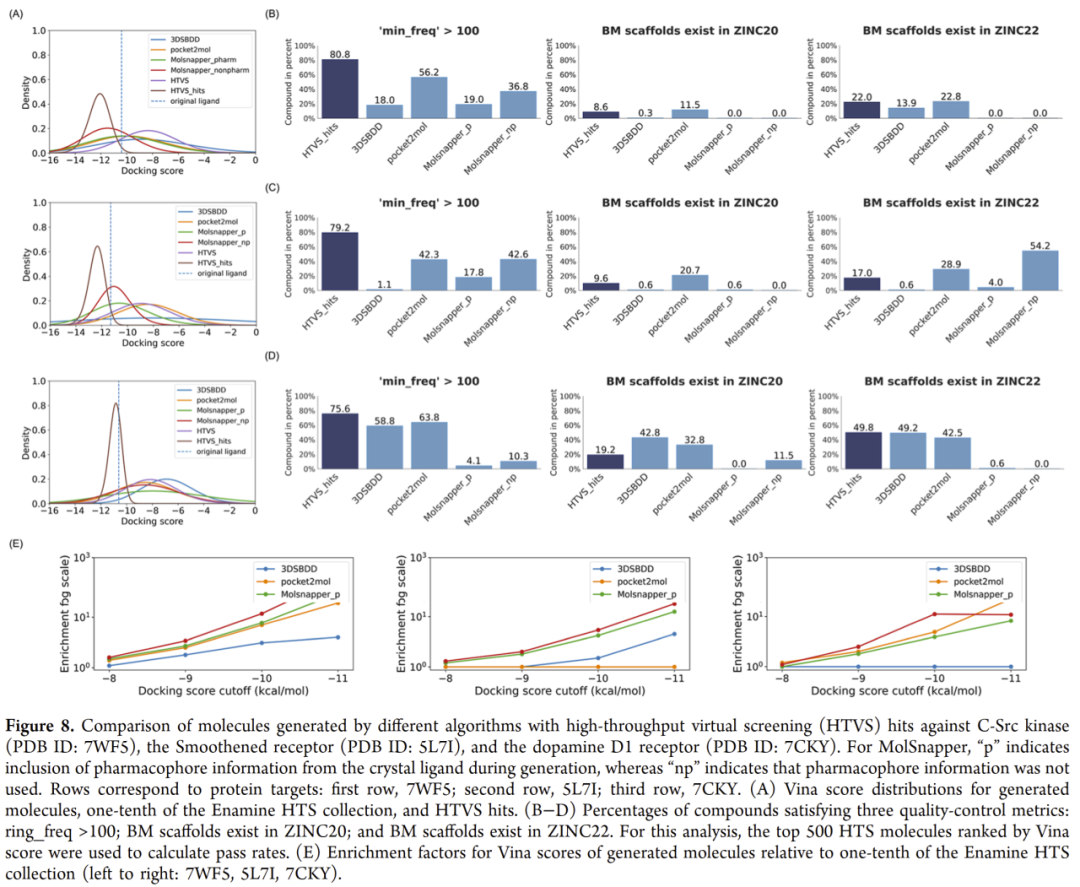
图8 | 生成式设计与虚拟筛选的对比结果
讨论
总体而言,研究人员发现当前三维结构生成模型在化学合理性、药物样性及3D构象质量方面仍存在明显不足:
- 生成分子中存在化学上不稳定或难以合成的结构;
- 常见的 QED 与 SA 指标不足以反映真正的化学可行性;
- 在 CrossDocked 数据集上训练的模型对真实靶点的泛化性能较差;
- 某些生成模型在构象应变能与空间冲突上表现较差。
为改进模型,研究人员提出以下方向:
- 引入化学先验的预训练,使模型学习合成可行分子的分布;
- 使用强化学习与化学合理性指标联合优化,引导生成过程;
- 发展基于片段或反应库的生成策略,平衡化学合理性与探索性;
- 改进训练数据集质量(如采用 BindingNetV2、LSD 数据集);
- 后处理修复模型,纠正无效或不合理结构。
结论
研究人员认为,尽管挑战依旧,三维结构驱动的生成模型在临床前药物发现中具有巨大潜力。通过整合结构信息与化学知识,这些模型可生成多样且具空间特征的分子,扩展化学空间并辅助药物化学家进行创新设计。
研究人员提出的化学合理性评估指标和系统性分析框架,为未来生成算法的改进提供了定量基准,也为药物化学领域实现真正“从结构到分子”的自动化药物设计奠定了基础。
整理 | DrugOne团队
参考资料
Structure-Based Generation of 3D Small-Molecule Drugs: Are We There Yet? Bo Yang, Chijian Xiang, Tongtong Li, Yunong Xu, and Jianing Li, Journal of Medicinal Chemistry Article.
DOI: 10.1021/acs.jmedchem.5c01706
内容为【DrugOne】公众号原创|转载请注明来源
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2025-11-07,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

