细胞免疫疗法TCR-T和空间VDJ测序
原创细胞免疫疗法TCR-T和空间VDJ测序
原创
追风少年i
发布于 2024-02-18 11:09:42
发布于 2024-02-18 11:09:42
作者,Evil Genius
关于单细胞数据分析的TCR已经分享了很多了,其分析的主要方向还是共享克隆以及克隆的多样本,并不能准确定位到具体的VDJ序列和肿瘤或者疾病的关系。所以在VDJ这块儿还是空转上更具优势。
当然单细胞纯肿瘤组织VDJ检测也可以做到,但是实际操作上还是有难度,而且肿瘤内浸润的T细胞数量非常少,单细胞检出效率有限,还有就是肿瘤内存在异质性,特定的VDJ存在具有特定靶点的区域,消除了空间信息之后很难准确定位TCR序列和靶点。
简单复习一下TCR的数据结构,根据TCR组分的不同,T细胞可被分为αβT细胞和γδT细胞。目前,TCR-T细胞领域中研究较多的是αβT细胞。αβT细胞的的TCR由α链和β链组成,以异二聚体的形式识别pMHC。α链和β链的膜外部分各含有2个Ig样结构域,一个为膜近端的恒定区(C区),另一个为膜远端的可变区(V区)。α链和β链的V区共同组成TCR的抗原结合部位。V区可进一步分为互补决定区1(complementarity-determining regions 1,CDR1)、CDR2和CDR3。在TCR识别配体时,多样性程度较低的CDR1和CDR2与pMHC两侧的α螺旋接触,而CDR3则与中央的肽接触。CDR3是决定TCR识别抗原特异性的最关键序列。为了实现对不同pMHC分子的识别,CDR3区具有高度多样性。TCR多样性集中体现在CDR3区的高可变性中。在传统TCR分离过程中,需要鉴定V区全长序列,进而建立抗原特异性TCR-T细胞。随着TCR研究的深入,目前仅需鉴定CDR3序列就能通过生物信息学方法获得有功能的全长TCR V区序列,大大简化了TCR分离过程。
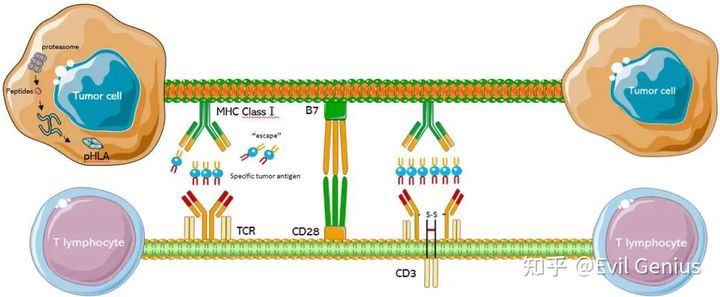
在免疫过程中经过加工的抗原被MHC分子递呈至细胞表面,被具有特异性受体的T细胞所识别。TCR识别抗原的信号主要通过TCR-CD3复合体(包括TCR的α链和β链、CD3γ、CD3δ、CD3ε以及CD3ζ等)转导。抗原呈递细胞(APC)与T细胞短暂结合过程中,若TCR识别特异性抗原肽,则T细胞与APC发生特异性结合,并由CD3分子向胞内传递特异性识别信号,导致T细胞表面黏附分子淋巴细胞功能相关分子-1(lymphocyte function-associated antigen 1,LFA-1)变构,并增强与细胞间黏附分子-1(intercellular cell adhesion molecule-1, ICAM-1)或ICAM-2的亲和力,从而稳定并延长APC与T细胞间的接触,最终有效诱导抗原特异性T细胞的激活和增殖。TCR在特异性识别APC递呈的抗原多肽过程中,T细胞表面的CD4或CD8分子作为共受体,参与同pMHC分子的结合,从而增强TCR与特异性抗原肽-MHC复合物结合的亲和力,并提高T细胞对抗原刺激的敏感性。在TCR-CD3复合体、共受体和细胞因子的共同作用下,识别抗原的T细胞活化,通过克隆增殖产生大量的效应细胞。同时,TCR与pMHC的结合又是可逆的,一个pMHC可激活数十个乃至数百个TCR-CD3复合体,TCR-CD3信号不断积累并持续激活T细胞。因此,APC或靶细胞表面只要有少量配体即可诱导特异性T细胞高效活化并扩增。
TCR-T疗法
TCR-T (T-cell receptor-engineered T cells) 通过基因导入方法,将抗原特异性TCR导入患者T细胞,制备人工TIL。TCR-T更类似于人体中天然的T细胞,实际上,TCR-T构想最初源于TIL(肿瘤浸润T淋巴细胞),一种天然存在于肿瘤组织中的T细胞。由于TIL数量较少,不是任何肿瘤组织中都存在,于是科学家们想到了制备工程化TIL,也即是当前TCR-T的前身。与CAR-T相比,TCR-T不仅能够靶向细胞表面蛋白质,还可以靶向胞内蛋白质。正是这点,使TCR-T更适合应用于实体瘤治疗(扩大靶点选择范围)。
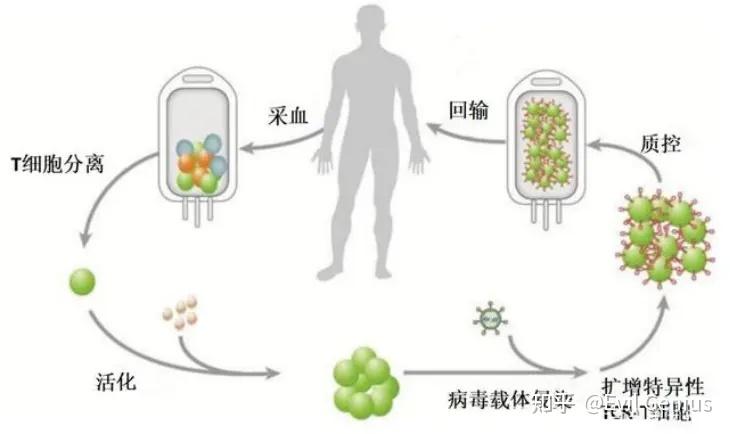
TCR-T制备过程
与CAR-T细胞疗法相似,TCR-T技术在发展过程中也经历了四次迭代: 第一代TCR-T是从患者T细胞中分离出肿瘤抗原特异性识别的T细胞亚群,经体外扩增后回输治疗。由于这种T细胞克隆数量极少,个体差异很大,因此很难产业化。 第二代TCR-T是通过克隆上述肿瘤抗原特异性识别的T细胞,获取其TCR基因序列,再转导至患者的外周T细胞上,这种方法使得TCR-T产业化成为可能。 第三代TCR-T是通过优化TCR的亲和力,使其能够更好地识别肿瘤抗原,再将其转导至患者T细胞上,整体提高TCR-T的成药性。 第四代TCR-T是靶向肿瘤新抗原(neoantigen)的高特异性细胞疗法,肿瘤应答和安全性都大幅提高。
TCR-T与CAR-T的差异
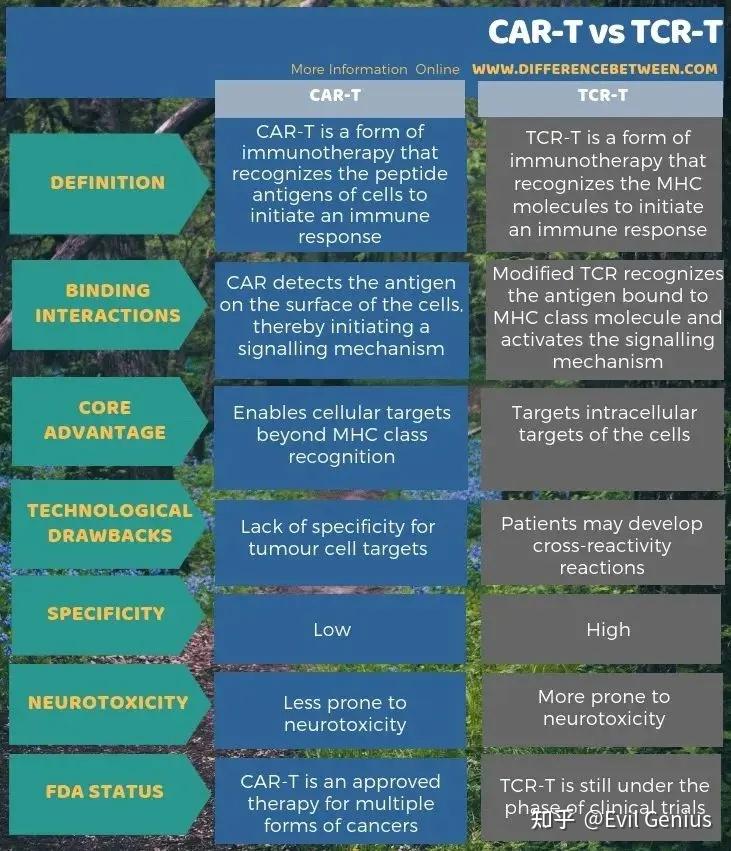
TCR-T疗法具有多方面的优势
- 第一个方面,TCR识别的靶点是HLA分子递呈的抗原肽,来自胞膜、胞浆和胞核中蛋白的抗原肽都可以被HLA呈递至细胞膜表面,从而成为TCR的靶点(细胞表达蛋白的90%以上),而CAR只能识别原来就定位于细胞膜表面的抗原(只占细胞表达蛋白的10%左右)。
- 第二个方面,CAR-T常常难以浸润至实体瘤内部,而TCR-T更容易浸润到实体瘤内部,因此容易获得更好的抗肿瘤活性。
- 第三个方面,针对单个抗原靶点的TCR-T回输后,可以进一步激活患者自身针对其他肿瘤抗原表位的T细胞,具有逆转实体瘤抑制性免疫微环境的作用。
- 第四个方面,CAR-T细胞接触肿瘤细胞后会大量扩增,并导致剧烈的细胞因子释放,后者会引发细胞因子释放综合征(CRS),导致严重的药物不良反应甚至危及患者的生命。相对于CAR-T,目前TCR-T的临床试验出现细胞因子风暴的频率较少,其严重程度较低,这可能与TCR-T保留天然的受体结构和信号通路有关。
目标抗原的选择
人类肿瘤抗原主要可分为两类——肿瘤特异性抗原(例如,新抗原和病毒抗原)和肿瘤相关抗原(例如,癌症/睾丸(CT)抗原、过表达抗原和分化抗原)。尽管TCR-T细胞可以靶向所有肿瘤抗原,但迄今为止确定的具有足够安全性和有效性的靶点数量仍然有限。选择合适的TCR-T细胞治疗靶抗原的首要考虑应该是抗原的高特异性。通常选择在肿瘤中高表达但在正常组织中低水平表达的靶抗原来限制任何潜在的脱靶效应和由破坏表达靶抗原的正常组织引起的剂量限制毒性。迄今为止,大多数TCR-T细胞疗法的临床试验都针对CT抗原和病毒抗原,其中纽约食管鳞状细胞癌1(NY-ESO-1)是最常针对的,占迄今为止试验的37%。
目前,过表达的睾丸抗原和分化抗原是基于TCR的过继细胞免疫治疗最常见的靶点。NY-ESO-1是一种CT抗原,在黑色素瘤和滑膜肉瘤患者中的客观反应率为40-60%。TCR基因治疗中考虑的其他肿瘤特异性抗原包括突变抗原和新抗原,其中大多数是安全的靶标,因为它们在肿瘤细胞中特异性表达。突变抗原在许多肿瘤类型中广泛表达,并且由于其个体化特征,可以通过测序获得新抗原。免疫选择压力可能导致靶抗原表达下调,降低TCR-T细胞治疗的疗效,特别是对于特定的T淋巴细胞。即使在输注过继功能细胞后,靶向肿瘤抗原的丢失也会导致肿瘤复发。靶向在肿瘤存活中具有核心功能的蛋白质可以克服靶抗原的下调;用不同的肿瘤特异性TCR注入多个T细胞克隆;或注入靶向两种或多种肿瘤抗原的T细胞。
TCR只能识别肽-HLA并杀死具有匹配HLA等位基因的癌细胞,因此筛选合适的HLA匹配也是必要的。来自非中国人的TCR-T细胞不能直接应用于中国患者。筛选具有最佳亲和力阈值的TCR仍然很困难。应鉴定对抗原具有高亲和力的TCR以增强免疫反应。然而,亲和力应控制在一定范围内,因为T细胞会受到超出生理功能的TCR亲和力的伤害。表达抗原受体(TCR)的T细胞识别抗原的机制对T细胞免疫很重要,而T细胞对病原体表达的抗原的定量反应能力是T细胞反应的重要指标。然而,这些T细胞必须对宿主组织上的类似抗原保持无反应。转基因T细胞的抗肿瘤活性应通过转化过程增强,将改变它们的亲和力。然而,亲和力应控制在一定范围内,因为太低的亲和力可能对靶向非肿瘤组织有毒,T细胞会攻击表达肿瘤相关抗原或类似配体的宿主非恶性组织。反之,亲和力也不能太高,否则可能导致免疫激活异常,增加引发细胞因子风暴的风险。此外,肽-HLA结合的改变会导致对自身抗原的不可预测的交叉反应,这可能会导致严重的不良事件。
最新一代的TCR-T技术面临着有效识别抗原的挑战。Kite Pharma公司已利用免疫组库(HTS-IR)的高通量测序和计算生物学方法(包括群体和单细胞水平的TraCeR和单细胞TCRseq)来重建TCR并鉴定免疫原性新抗原。流式细胞仪已被用于从患者中筛选出肿瘤抗原特异性T细胞,通过单细胞技术获得识别这些抗原的TCR基因,并将其导入患者的外周T细胞进行治疗。这种探索为分析T细胞的多样性和动态提供了新的工具。需要进一步的生物信息学进展来开发更多新颖的工具。
肿瘤抗原异质性与肿瘤免疫逃逸
肿瘤抗原异质性对TCR-T治疗效果的影响仍不清楚。癌症相关抗原的表达在肿瘤内的不同细胞中有所不同,这使得一些肿瘤细胞能够逃避特定的抗原靶向治疗,并导致一些接受免疫检查点抑制剂(ICIs)和过继性T细胞治疗的患者产生治疗抗性。TCR-T是由慢病毒转染产生的T细胞产物,产生的细胞在患者体内表达针对多种肿瘤抗原的多种TCR。
空间VDJ与TCR-T疗法
空间组学在表征肿瘤组织的空间异质性以及VDJ测序方面具有无可替代的优势,
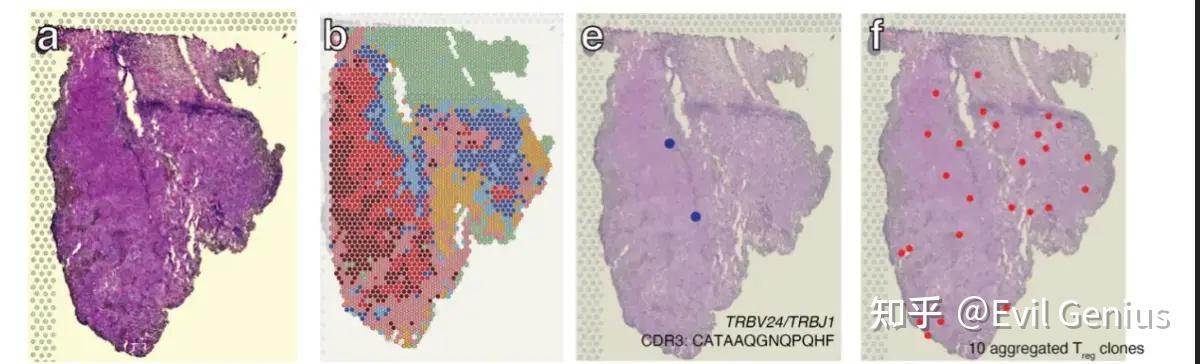
其中不同的空间区域会聚集不同的TCR/BCR序列,结合数据分析可以表征肿瘤异质性和靶点/VDJ选择。
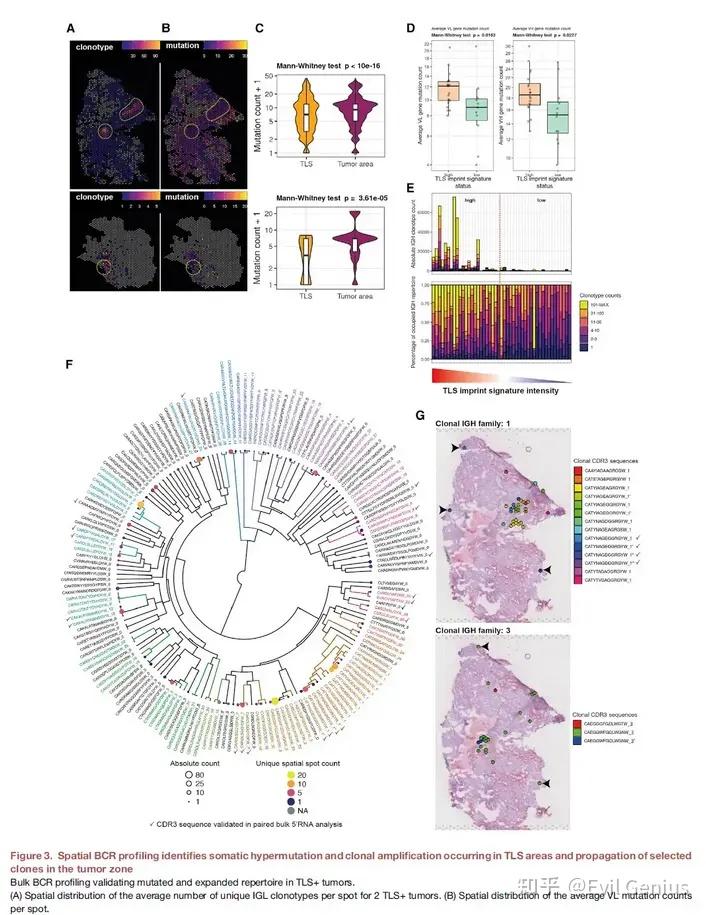
可见TCR-T疗法与空间VDJ有极强的关联性,未来大有可为。
生活很好,有你更好
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
评论
登录后参与评论
推荐阅读
目录

