智药简报 | 从模型走向系统:递送、结构、机制、组合、蛋白设计和制造
智药简报 | 从模型走向系统:递送、结构、机制、组合、蛋白设计和制造

MindDance
发布于 2026-05-09 13:53:24
发布于 2026-05-09 13:53:24
过去谈AIDD,最容易被看到的是模型本身。
模型能不能生成一个更好的分子,能不能预测更高的活性,能不能在benchmark上赢过已有方法。这些问题依然重要,但越接近真实药物研发,答案就越不可能只停留在一个分数上。
药物能不能送到目标组织,天然产物空间能不能被模型更好理解,片段优化时到底该往哪里长,一个突变是否真的改变蛋白互作,药物组合为什么可能产生协同,蛋白能否被从头设计并服务于治疗和生物制造,这些问题都在把AIDD带向更完整的研发链条。
本期智药简报关注新近发表的AIDD相关高水平文章。主线选择6篇,延伸阅读2篇。它们不完全属于同一种类型,有的是原始研究,有的是综述;有的直接面向药物设计,有的更偏递送、机制或生物制造。但放在一起看,可以看到一个清晰趋势:AIDD正在从单点模型,走向研发系统。
一分钟速读
这期的6篇主线文章分别覆盖了AIDD链条中的不同位置。
Nature Biotechnology 的MOLEA把AI用于LNP工程,目标是提升mRNA递送的组织选择性。Nature Machine Intelligence 的NaFM面向天然产物小分子预训练Foundation Model。Nature Communications 的FMOPhore从结构基础药物设计出发,关注fragment-to-lead过程中的hotspot识别。Nature Methods 的eSIG-Net用蛋白互作语言模型解释单点突变对蛋白互作网络的影响。Nature 的de novo protein design综述提供了深度学习时代蛋白设计的全景视角。Briefings in Bioinformatics 的DeepDrugs则将药物联用预测推进到药物—药物—细胞背景的三方关系建模。
延伸阅读选择两篇:一篇是Nature Reviews Drug Discovery关于小分子激酶调控剂设计策略的综述,另一篇是JACS关于机器学习引导P450酶发现、服务天然产物生物合成的工作。
这些文章共同指向一个变化:AIDD不再只是寻找一个候选答案,而是在进入递送、结构、机制、组合、蛋白设计和制造这些更真实的研发节点。
01|AI设计LNP:让mRNA药物更精准地送达目标组织
论文名称:A multiobjective AI model for LNP engineering enhances tissue-selective mRNA delivery
发表期刊:Nature Biotechnology
发表时间:2026-04-28
代码/数据: GitHub: https://github.com/bowenli-lab/MOLEAZenodo: https://doi.org/10.5281/zenodo.18943783
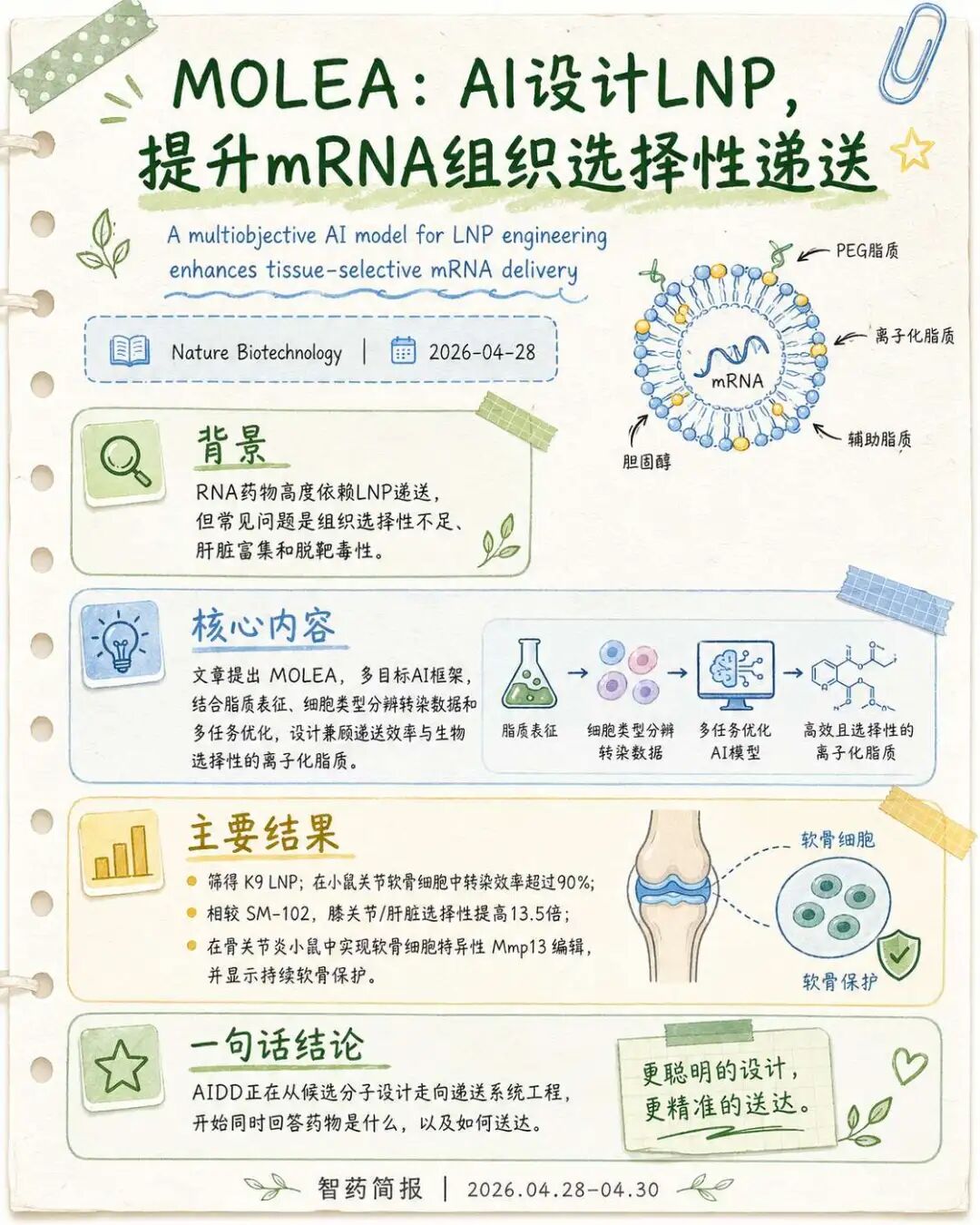
mRNA药物、RNA干扰和基因编辑技术要真正发挥作用,递送始终是绕不开的问题。LNP已经是RNA药物递送中最重要的载体之一,但组织选择性不足、肝脏富集和脱靶毒性仍然限制了其更广泛的治疗应用。也就是说,payload设计得再好,如果无法安全、有效、选择性地抵达目标组织,治疗窗口仍然会被大大压缩。
这项工作提出MOLEA,即multiobjective LNP engineering with artificial intelligence。它将高维脂质表征、细胞类型分辨的转染数据和多任务优化结合起来,用来设计同时具有高递送效力和生物选择性的离子化脂质。作者团队主要来自多伦多大学Leslie Dan Faculty of Pharmacy、Institute of Biomedical Engineering、Princess Margaret Cancer Center和Vector Institute等机构。
研究中,MOLEA被应用到软骨递送场景。作者开发出的K9 LNP在小鼠关节软骨细胞中达到超过90%的转染效率,并相较临床benchmark SM-102实现13.5倍膝关节—肝脏选择性。进一步在骨关节炎小鼠模型中,K9 LNP被用于软骨细胞特异性Mmp13编辑,并表现出持续软骨保护作用,同时抑制了疾病相关的免疫和基质重塑过程。
放在AIDD语境里,这项研究把AI从候选分子发现推进到了递送系统工程。对核酸药物来说,载体设计本身就是药物开发的一部分。药物有没有潜力是一回事,能否抵达正确组织,是另一回事。
MOLEA目前主要展示的是软骨递送场景和小鼠模型结果。更广泛的组织适用性和人体转化还需要后续研究推进。但它传递出的方向很明确:AIDD不只设计药物分子,也可以设计药物抵达身体的方式。
02|天然产物Foundation Model:让模型读懂更复杂的化学空间
论文名称:Pretraining a foundation model for small-molecule natural products
发表期刊:Nature Machine Intelligence
发表时间:2026-04-29
代码/数据: GitHub: https://github.com/TomAIDD/NaFM-Official
代码Zenodo归档:https://doi.org/10.5281/zenodo.18871560
数据figshare:https://doi.org/10.6084/m9.figshare.28980254.v1
模型权重Zenodo:https://doi.org/10.5281/zenodo.15385335
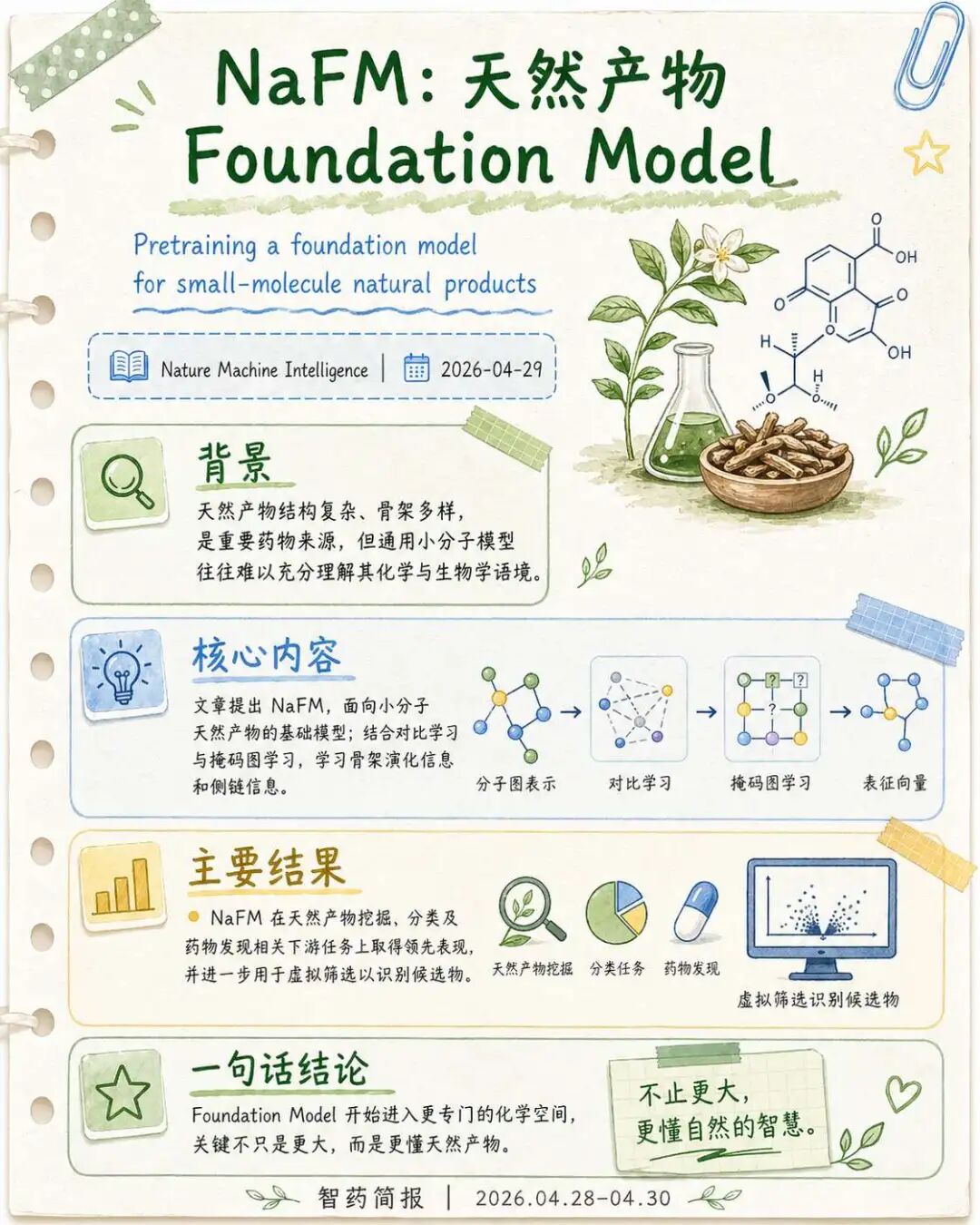
天然产物一直是药物发现的重要来源。它们来自微生物、植物和动物代谢体系,结构复杂、骨架多样,也常常携带独特生物活性。许多经典药物都与天然产物密切相关,但天然产物的复杂性也让建模变得更难。普通小分子模型未必能充分理解天然产物的结构特征、生物合成背景和活性空间。
这项工作提出NaFM,一个面向小分子天然产物的Foundation Model。作者团队包括北京大学天然药物及仿生药物全国重点实验室、华盛顿大学Paul G. Allen School of Computer Science & Engineering、香港中文大学、西安交通大学人工智能与机器人研究所、石河子大学等。
NaFM的核心思路,是把天然产物的特殊结构和演化信息纳入预训练。模型结合contrastive learning和masked graph learning,使模型同时关注分子骨架中的演化信息和侧链信息。在天然产物挖掘、分类和药物发现相关下游任务中,NaFM取得了较强表现,并进一步用于虚拟筛选,展示其天然产物表征在候选物识别中的作用。
这项研究的重要性在于,它没有把天然产物简单当作普通小分子的一个子集,而是为这一类特殊化学空间建立了专门的模型底座。天然产物的结构复杂、来源多样、修饰难度高,模型如果缺乏对应语境,很容易只学到表层结构相似性。
NaFM更适合被理解为天然产物药物发现的基础模型能力。它为天然产物挖掘、分类、活性预测和虚拟筛选提供了更贴近该化学空间的预训练基础。Foundation Model真正有用的地方,不只是规模更大,而是能不能理解自己面对的化学世界。
03|FMOPhore:片段应该往哪里长,不能只靠直觉
论文名称:FMOPhore for hotspot identification and efficient fragment-to-lead growth strategies
发表期刊:Nature Communications
发表时间:2026-04-28
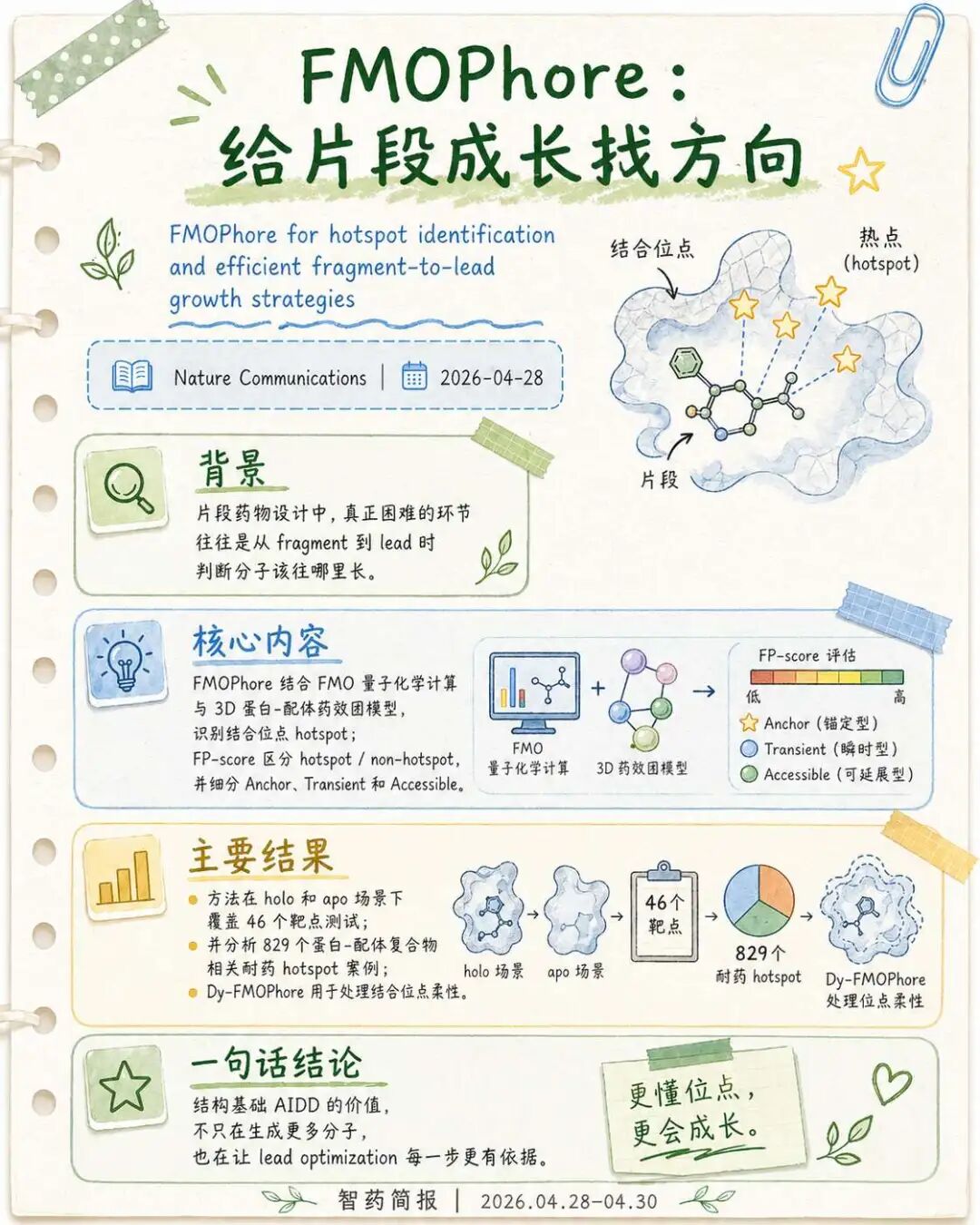
片段药物设计的起点通常很小,片段本身活性有限,真正关键的是后续如何生长成先导物。这个过程里,研究者需要判断哪些结合位点残基值得优先利用,哪些相互作用值得保留,分子从哪个方向扩展更可能带来效力和效率提升。
FMOPhore关注的正是这个问题。文章提出一种结合量子力学Fragment Molecular Orbital计算和3D蛋白—配体药效团模型的方法,用于识别结合位点中的关键hotspot残基。作者来自University of Dundee的Drug Discovery Unit、Wellcome Centre for Anti-Infectives Research和School of Life Sciences等单位。
方法上,FMOPhore使用FP-score将结合位点残基分为hotspot和non-hotspot,并进一步把hotspot划分为Anchor、Transient和Accessible等类别。作者在holo-complex和apo-structure两种场景下测试方法,覆盖46个蛋白靶点,并包含一个围绕829个蛋白—配体复合物的耐药hotspot实验案例。为处理蛋白结合位点柔性,文章还提出Dy-FMOPhore。
这项研究贴近药物化学优化的实际过程。很多生成式分子设计方法可以产生大量候选物,但真正推进到lead optimization时,研究者需要的是更具体的判断:这个片段为什么应该往这里长,哪些相互作用是高价值的,哪些位置可能带来选择性和效力提升。
FMOPhore补上的不是生成数量,而是优化方向。在片段到先导物的过程中,计算方法的价值不只是给出更多结构,也包括让每一步生长更有依据。
04|eSIG-Net:一个突变改变了什么,模型开始从互作网络里找答案
论文名称:eSIG-Net: an interaction language model that decodes the protein code of single mutations
发表期刊:Nature Methods
发表时间:2026-04-29
论文链接:https://www.nature.com/articles/s41592-026-03086-x
代码/数据: GitHub: https://github.com/Stephen-Yi-Laboratory/eSIG-Net
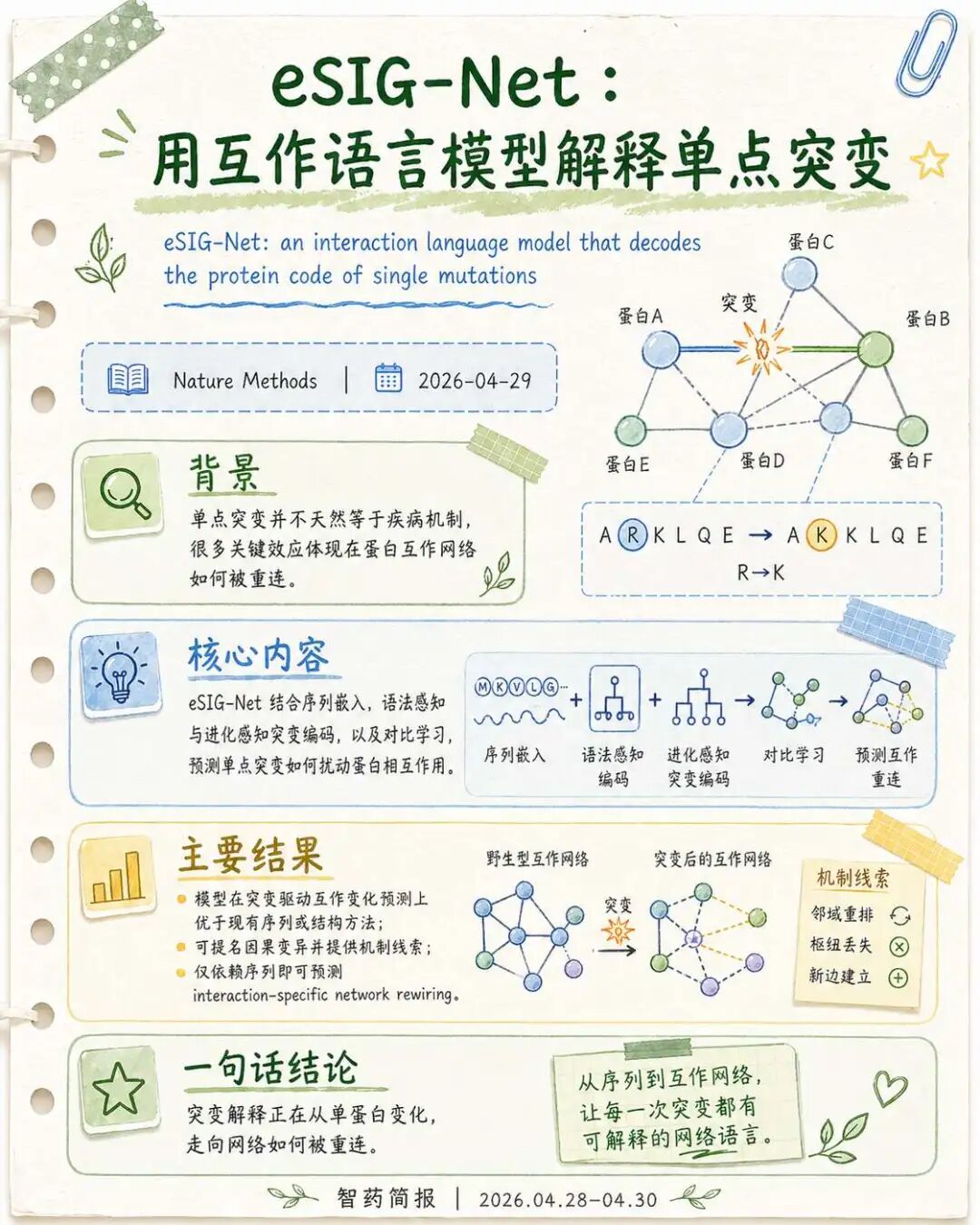
药物发现上游常常需要先判断一个突变是否真的有功能意义。突变本身并不等于疾病机制。有些突变改变蛋白结构,有些影响稳定性,还有一些会更隐蔽地改变蛋白—蛋白相互作用。对很多疾病来说,后者往往非常关键,因为生物功能很少由孤立蛋白完成,而是发生在互作网络中。
这篇Nature Methods Brief Communication提出eSIG-Net,即edgetic mutation sequence-based interaction grammar network。
研究内容上,eSIG-Net将蛋白序列嵌入、语法感知和进化感知的突变编码、对比学习结合起来,预测单点突变如何扰动蛋白相互作用。论文摘要称,eSIG-Net优于现有序列和结构方法,可以提名因果变异并提供机制洞察,并能仅从序列信息预测interaction-specific network rewiring。
这类方法和AIDD的联系,主要在上游机制判断。靶点发现、患者分层、耐药突变解释和精准治疗,都需要回答哪些突变真正改变了生物功能。如果模型能帮助判断突变是否重连了互作网络,就能为后续靶点选择和治疗假设提供更清楚的依据。
eSIG-Net把突变解释从单个蛋白推向了蛋白互作语境。真正的疾病机制往往不在一个孤立节点里,而在网络如何被重连。
05|Nature综述:蛋白设计进入深度学习时代后,问题变成了设计什么
论文名称:The past, present and future of de novo protein design
发表期刊:Nature
发表时间:2026-04-29
论文链接:https://www.nature.com/articles/s41586-026-10328-7
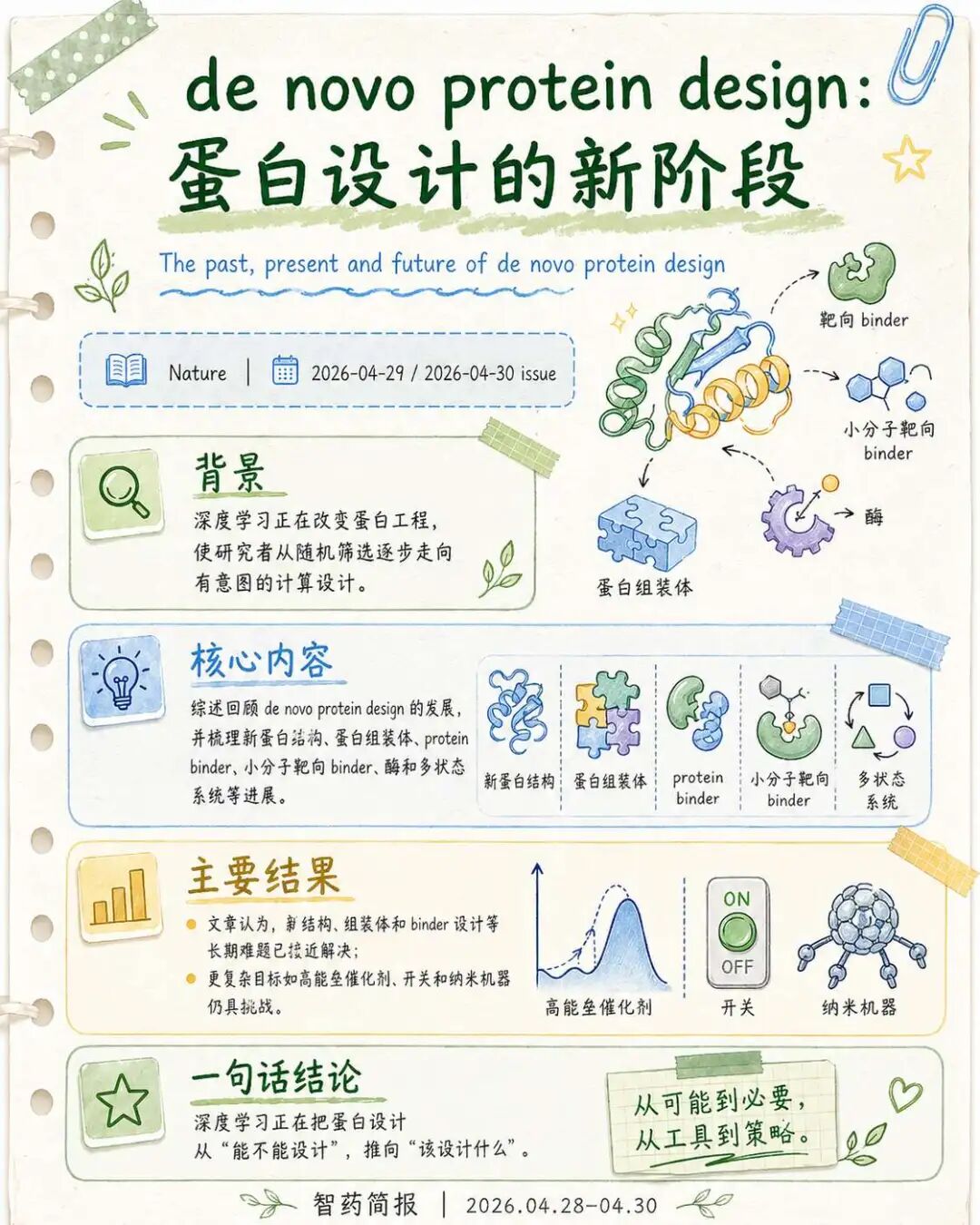
这篇Nature综述来自华盛顿大学等团队,通讯作者为David Baker。文章回顾了全新蛋白设计的发展脉络,也总结了深度学习进入之后,蛋白设计领域正在发生的变化。
过去蛋白工程很大程度依赖筛选、定向进化和经验积累。随着结构预测、序列设计和生成模型的发展,研究者开始从随机搜索走向有意图的计算设计。文章摘要中也明确指出,deep-learning-powered advances正在推动protein engineering从random selection走向intentional computational design。
内容上,综述讨论了全新蛋白设计的现状和未来。文章提到,新蛋白结构、蛋白组装体和protein binder设计这些长期挑战已经接近解决;与此同时,小分子靶向binder、酶和多状态蛋白系统的从头设计也取得了明显进展。当前仍然困难的方向包括高能垒反应催化剂、开关和纳米机器等更复杂功能系统。
这和AIDD的关系不只在蛋白设计本身。蛋白可以是治疗性药物,也可以是递送工具、分子工具、酶催化器、生物材料和合成生物学元件。当蛋白设计越来越可控,AIDD能够设计的对象就不再局限于小分子,而是扩展到更广泛的功能分子和功能系统。
深度学习正在把蛋白设计从能不能设计,推向应该设计什么。 对药物研发来说,这意味着AI可以参与的对象不再只是小分子,也包括更复杂的功能蛋白、分子工具和生物系统。
06|DeepDrugs:药物联用预测,关键是看见药物—药物—细胞的三方关系
论文名称:DeepDrugs: a mechanism-aware tri-linear attention framework for synergistic drug-combination prediction
发表期刊:Briefings in Bioinformatics
发表时间:2026-04-28
论文链接:https://academic.oup.com/bib/article/27/2/bbag205/8663950
代码/数据: GitHub: https://github.com/xingaojia/DeepDrugs
Zenodo: https://doi.org/10.5281/zenodo.18830842
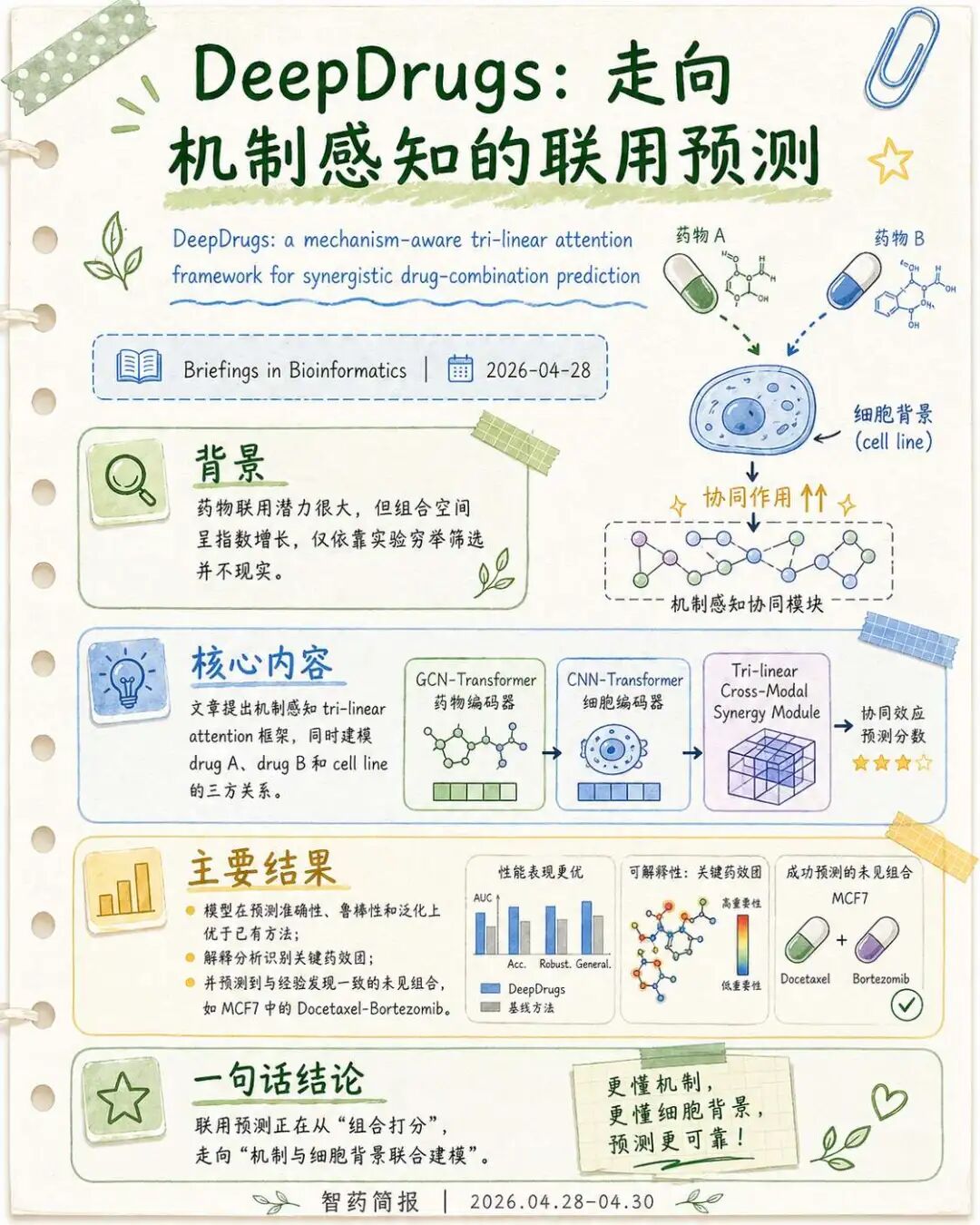
药物联用预测是AIDD里很现实的任务。尤其在肿瘤治疗中,单药常常难以压制多个致病通路,耐药也容易出现。组合疗法可能通过多靶点干预提高疗效、降低毒性或延缓耐药,但真正产生协同的组合并不多,靠实验穷举成本极高。DeepDrugs文章的引言也强调,组合空间呈指数增长,穷尽筛选并不现实,因此计算方法成为探索该空间的重要工具。
DeepDrugs来自山东大学等团队。方法上,DeepDrugs提出机制感知的tri-linear attention framework。作者指出,已有许多方法先分别表征两个药物对细胞系的影响,再在后期合并表示,这可能损失drug A、drug B和cell line同时作用时产生的三方信号。DeepDrugs则直接建模两个药物在特定细胞背景下的共同作用,使用GCN-Transformer药物编码器、CNN-Transformer细胞系编码器和Tri-linear Cross-Modal Synergy Module来预测协同分数。
结果方面,论文摘要称DeepDrugs在预测准确性、鲁棒性和泛化能力上优于state-of-the-art方法。模型解释分析识别出的关键药效团与实验验证一致,并预测了与经验发现相符的未见药物组合,例如MCF7细胞系中的Docetaxel-Bortezomib组合。
DeepDrugs的重点在于把药物联用从简单组合打分,推进到药物—药物—细胞背景的三方关系建模。药物发现里的很多问题并不是二元关系,而是高阶关系。真正有用的AIDD模型,需要逐渐学会处理药物、靶点、细胞状态和疾病背景之间的复杂耦合。
延伸阅读
07|NRDD综述:小分子激酶药物设计,不再只是堵住ATP口袋
论文名称:Contemporary design of small-molecule kinase modulators: orthosteric, allosteric and induced-proximity strategies
发表期刊:Nature Reviews Drug Discovery
发表时间:2026-04-28
论文链接:https://www.nature.com/articles/s41573-026-01411-9
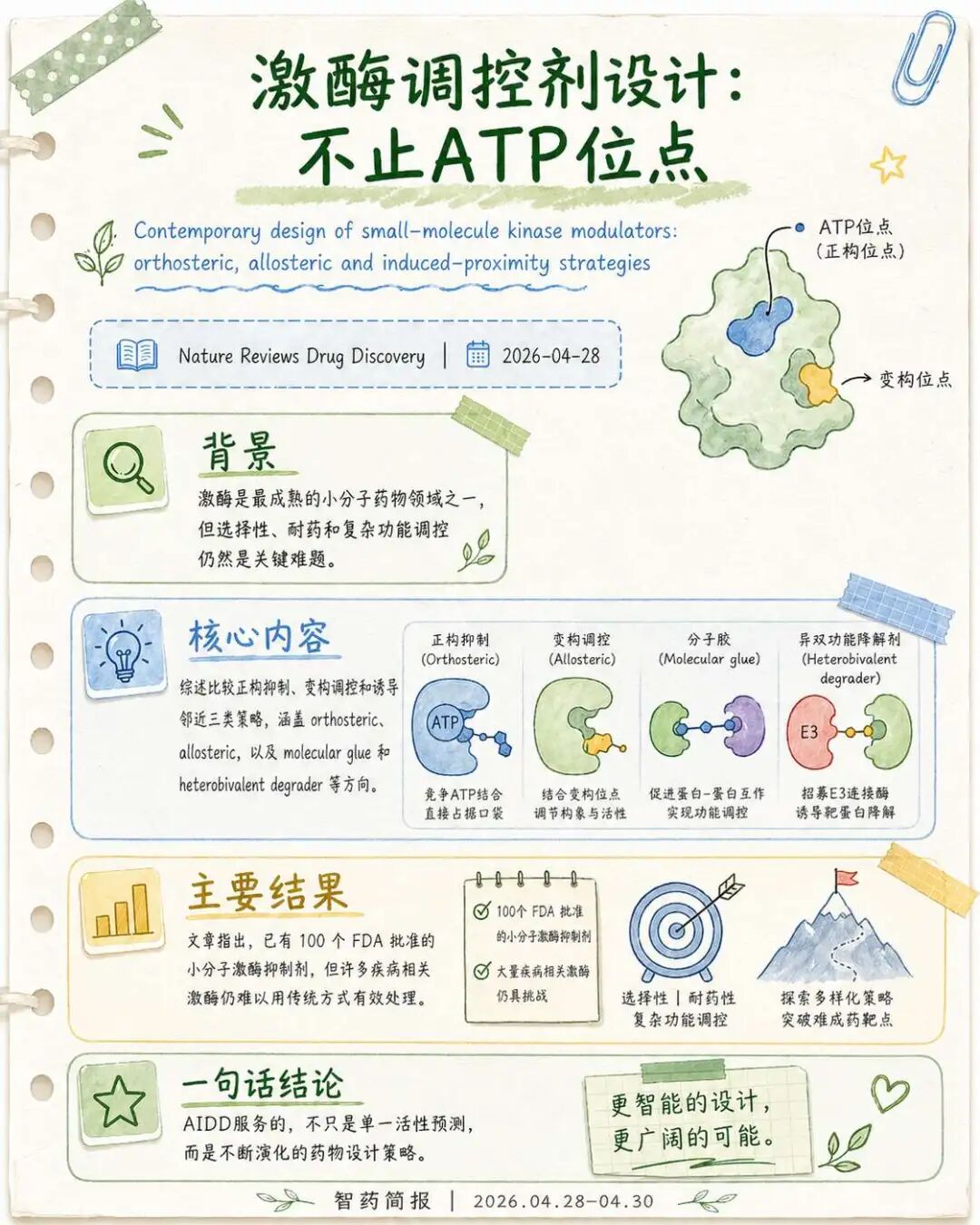
激酶药物是小分子药物研发中最成熟的领域之一,但成熟并不意味着问题已经解决。文章摘要提到,目前已有100个FDA批准的小分子激酶抑制剂,但许多疾病相关激酶仍难以用传统治疗策略处理,关键挑战包括选择性、scaffolding functions调控和耐药。
这篇综述比较了传统ATP位点抑制剂、变构调控剂,以及分子胶和heterobivalent degrader等诱导邻近策略。也就是说,激酶药物设计正在从简单的正构抑制,扩展到更复杂的调控方式。
对AIDD来说,这篇文章提供的是药物设计语境。模型最终不是为了生成一个抽象高分分子,而是要服务于具体设计策略。激酶领域的变化会反过来影响模型该优化什么:选择性、耐药、变构位点、诱导邻近、细胞内功能调控,都可能成为未来AIDD模型需要理解的目标。
AIDD真正要服务的,不只是单一活性预测,而是不断演化的药物设计问题。 激酶领域正好提供了一个很典型的观察窗口。
08|JACS:机器学习辅助发现P450酶,服务天然产物生物制造
论文名称:Machine-Learning-Guided Discovery of Cytochrome P450 Enzymes for Bioproduction of Jolkinolides and Other Labdane-Related Diterpenoids
发表期刊:Journal of the American Chemical Society
发表时间:2026-04-29
论文链接:https://pubs.acs.org/doi/10.1021/jacs.6c05010
代码/数据: GitHub: https://github.com/rickysmile/LRDs-predictor
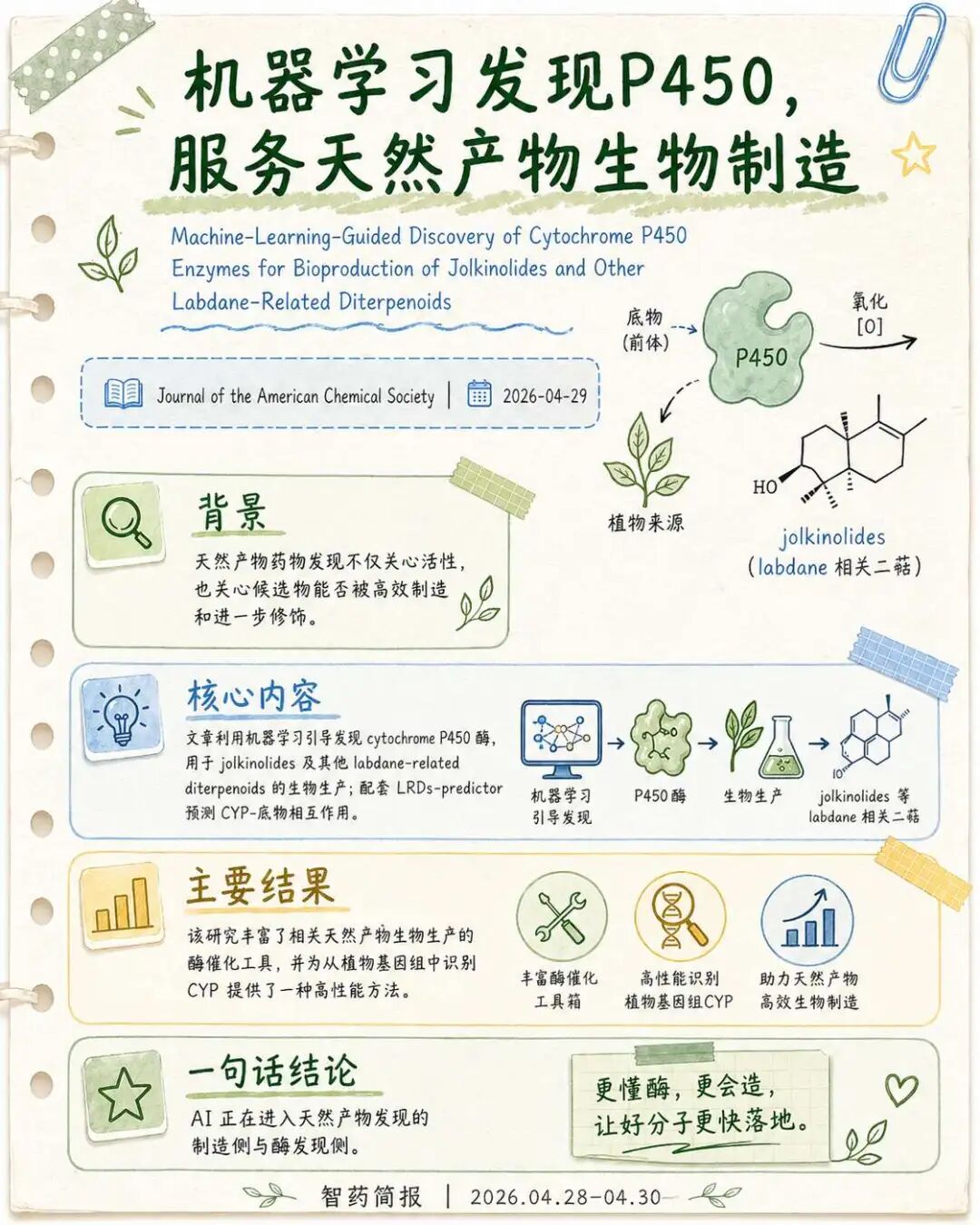
这篇JACS文章更偏天然产物生物制造。Cytochrome P450酶在植物萜类天然产物氧化修饰中非常重要,常见反应包括羟基化和氧化介导的结构转化。该工作关注机器学习引导发现P450酶,用于jolkinolides及其他labdane-related diterpenoids的生物生产。
在天然产物药物发现中,候选物能不能被稳定获得、能不能规模化制备、能不能进一步修饰,常常会影响后续研究推进。对复杂天然产物来说,发现和利用关键生物合成酶,本身就是药物发现链条中的重要一环。
这项工作对应的LRDs-predictor仓库显示,其方法用于预测CYP酶—底物相互作用,结合Multiple Sequence Alignment、底物PCA特征和CatBoost Ranker,并支持训练、预测、交叉验证和特征重要性分析。
AI在天然产物药物发现中的作用,不只发生在活性筛选环节,也可以发生在生物合成路径、酶催化工具和可获得性问题上。 对天然产物来说,能否制造出来,有时和能否发现出来同样重要。
END|AIDD正在从单点模型,走向研发系统
把4月28日至4月30日这几篇文章放在一起看,本期最突出的变化不是某个模型刷新了某个指标,而是AIDD正在进入更分散、更真实的研发节点。
MOLEA进入LNP递送系统设计,回答药物如何更精准送达。NaFM进入天然产物化学空间,回答模型如何理解更复杂的分子来源。FMOPhore进入片段成长和lead optimization,回答片段该往哪里长。eSIG-Net从蛋白互作角度解释突变,回答机制是否站得住。DeepDrugs处理药物组合、细胞背景和协同关系,回答治疗策略如何建模。Nature的蛋白设计综述把视野拉到更高处,提醒我们深度学习正在改变功能分子的设计方式。
这背后有一个清晰趋势:AIDD不再只是寻找一个答案,而是在进入一条路径。
这条路径上,有模型,有数据,有结构,有递送,有机制,有药化,有实验,也有未来可能进入临床和制造的环节。高质量的AIDD研究,越来越不只是展示模型能力,而是要说明自己在药物研发链条中到底解决了哪一个真实问题。
模型当然重要。 但模型之后,还有递送、合成、机制、组合、验证和制造。
能把这些环节连接起来,才是AIDD真正走向药物研发现场的开始。
参考文献
- Zhou, M., Xu, Y., Li, G. et al.A multiobjective AI model for LNP engineering enhances tissue-selective mRNA delivery.Nature Biotechnology (2026). Published: 28 April 2026. DOI: 10.1038/s41587-026-03109-0. URL: https://www.nature.com/articles/s41587-026-03109-0
- Ding, Y., Qiang, B., Li, S. et al.Pretraining a foundation model for small-molecule natural products.Nature Machine Intelligence (2026). Published: 29 April 2026. DOI: 10.1038/s42256-026-01226-8. URL: https://www.nature.com/articles/s42256-026-01226-8
- Ibrahim, P. E. G. F., Altmann, S., Zachariae, U. et al.FMOPhore for hotspot identification and efficient fragment-to-lead growth strategies.Nature Communications (2026). Published: 28 April 2026. DOI: 10.1038/s41467-026-72384-x. URL: https://www.nature.com/articles/s41467-026-72384-x
- Pan, X., Shrawat, A., Raghavan, S. et al.eSIG-Net: an interaction language model that decodes the protein code of single mutations.Nature Methods (2026). Published: 29 April 2026. DOI: 10.1038/s41592-026-03086-x. URL: https://www.nature.com/articles/s41592-026-03086-x
- Yang, W., Wang, S., Lee, G. R. et al.The past, present and future of de novo protein design.Nature652, 1139–1152 (2026). Published: 29 April 2026; issue date: 30 April 2026. DOI: 10.1038/s41586-026-10328-7. URL: https://www.nature.com/articles/s41586-026-10328-7
- Xin, G., Zhu, Y., Li, Q. et al.DeepDrugs: a mechanism-aware tri-linear attention framework for synergistic drug-combination prediction.Briefings in Bioinformatics27(2), bbag205 (2026). Published: 28 April 2026. DOI: 10.1093/bib/bbag205. URL: https://academic.oup.com/bib/article/27/2/bbag205/8663950
- Rudolph, J., Hoeflich, K. P. & Dar, A. C. Contemporary design of small-molecule kinase modulators: orthosteric, allosteric and induced-proximity strategies.Nature Reviews Drug Discovery (2026). Published: 28 April 2026. DOI: 10.1038/s41573-026-01411-9. URL: https://www.nature.com/articles/s41573-026-01411-9
- Lu, K., Zhang, R., Gao, K. et al.Machine-Learning-Guided Discovery of Cytochrome P450 Enzymes for Bioproduction of Jolkinolides and Other Labdane-Related Diterpenoids.Journal of the American Chemical Society (2026). Published: 29 April 2026. DOI: 10.1021/jacs.6c05010. URL: https://pubs.acs.org/doi/10.1021/jacs.6c05010
- 文章图片由AI生成
往期内容
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-05-01,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读
目录

