Nat. Commun. | MechFind: 用于酶催化机制从头预测的计算框架
Nat. Commun. | MechFind: 用于酶催化机制从头预测的计算框架

DrugAI
发布于 2026-05-08 19:56:22
发布于 2026-05-08 19:56:22
酶催化机制的逐步解析对于酶工程、人工酶设计以及生物催化开发至关重要。然而,目前公开数据库中真正具有完整机理注释的酶反应不到一千个,大量已知生化反应仍缺乏详细机制描述。
在本研究中,研究人员提出了 MechFind,一种能够仅基于反应计量关系(reaction stoichiometry)实现酶催化机制从头预测的计算框架。与依赖蛋白结构或活性位点信息的方法不同,MechFind通过“化学基团(moiety)变化”抽象反应步骤,并自动生成满足元素与电荷守恒的候选机制。
该框架首先寻找最简约(parsimonious)的机制路径,随后利用与已知机制的相似性对候选方案重新排序。结果显示,MechFind能够在72%的训练集案例中于前十个预测结果内恢复已验证机制,并在多个未见过的新酶机制中成功完成间接验证。进一步地,研究人员将MechFind应用于Rhea数据库中的14,931个反应,成功为57%的反应生成合理机制,总计产生超过18,000个机制假设。研究人员认为,该资源将显著扩展现有酶机制知识图谱,并为de novo酶设计与酶工程提供关键反应步骤信息。

酶几乎参与所有生命体系中的化学反应,从能量代谢到大分子合成都离不开酶催化。由于其高度选择性和高效催化能力,酶也被广泛用于生物制造、药物合成以及绿色化学。
传统酶工程往往依赖随机突变与定向进化,但这些方法成本高、周期长。近年来,随着AlphaFold、RoseTTAFold以及ProteinMPNN等蛋白设计模型的发展,研究人员开始尝试从头设计新型酶。
然而,酶设计的关键在于“过渡态稳定化(transition state stabilization)”。要想构建有效活性位点,研究人员必须知道反应的详细催化机制,包括电子转移、键断裂与键形成过程。
目前最大的障碍在于所谓的“机制鸿沟(mechanism gap)”:虽然Rhea、KEGG、BRENDA等数据库记录了数万条酶反应,但真正带有完整逐步机制注释的案例却极少。M-CSA数据库中也仅有734个完整机制条目。
此前的机制预测工具,如MechSearch和EzMechanism,通常依赖高分辨率蛋白结构或人工指定活性位点,因此难以大规模推广。研究人员因此提出MechFind,希望在无需结构信息的条件下,仅根据反应本身推断酶机制。
方法
MechFind的核心思想是将酶反应抽象为“化学基团变化(moiety changes)”。
研究人员首先对M-CSA数据库中的734个完整机制进行人工整理与校正,以确保所有步骤满足元素和电荷守恒。随后,将每一个反应步骤表示为特定化学基团的“增加”或“减少”,并构建规则库。
在机制预测阶段,MechFind只需要输入整体反应的底物和产物结构。模型首先利用混合整数线性规划(MILP)寻找能够解释该反应的最少步骤集合,即“最简机制”。随后,再通过OrderRules模块寻找合理的步骤顺序,以保证中间体在生成之前不会被提前消耗。
由于单纯的“最少步骤原则”并不总能得到真实机制,研究人员进一步设计了基于相似性的重排序方法。该方法将候选机制与M-CSA数据库中的已知机制逐一比较,并根据共享反应步骤的相似度重新排序。
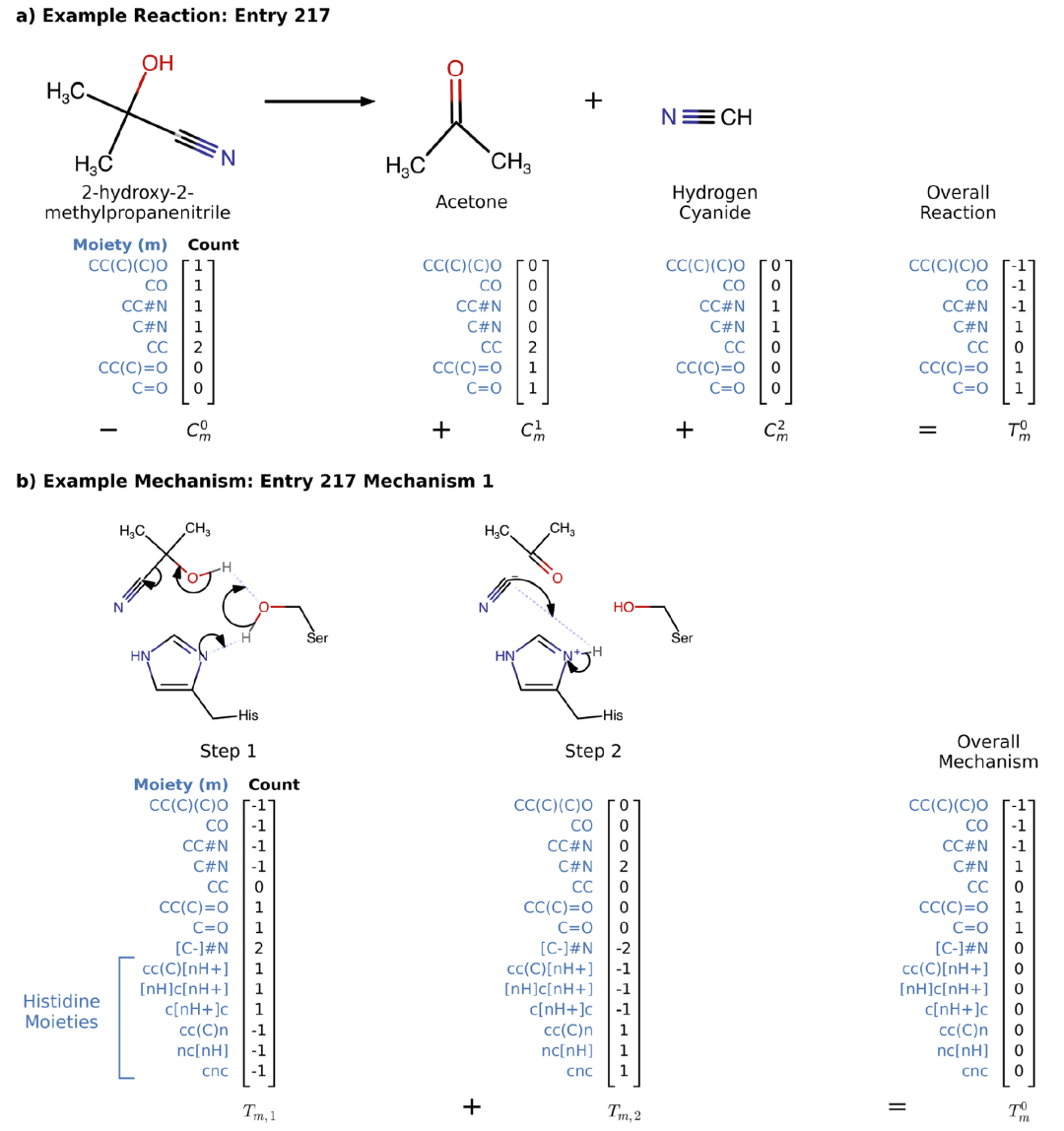
图1:MechFind基于化学基团变化的酶机制预测框架。
结果
基于化学基团的反应表示
研究人员首先展示了MechFind如何将复杂酶反应转换为“化学基团向量”。
在这一框架中,每个非氢原子根据其局部键连接环境被编码为特定“moiety”。整个反应则表示为这些moiety的净变化。
例如,在(S)-羟基腈裂解酶反应中,研究人员将每一步中的键变化转化为moiety增减,并证明所有步骤累积后能够严格恢复整体反应计量关系。
这一抽象方式使MechFind无需三维结构即可处理复杂催化过程。
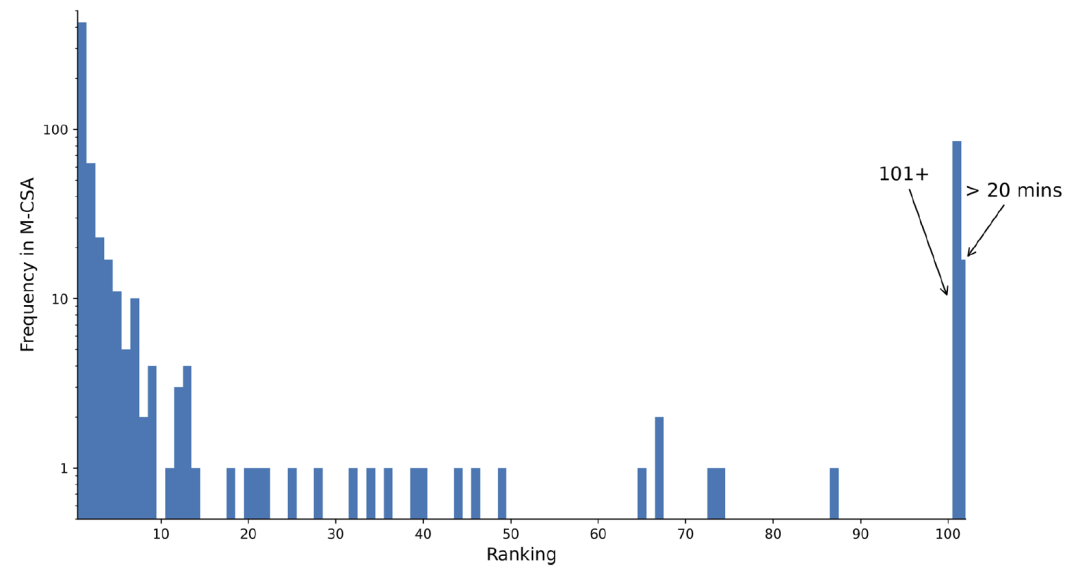
图2:基于moiety变化的反应编码示意图。
在M-CSA数据库上的机制恢复能力
研究人员随后在661个可用于输入的M-CSA机制上测试MechFind性能。
结果显示,仅依赖“最简原则”,MechFind即可在64%的案例中将真实机制排在第一位;若考虑前十个预测,则恢复率达到85%。
研究人员指出,这意味着只需保留少量最优候选机制,就有很高概率包含真实机制。
不过,在约11%的案例中,模型未能恢复正确机制。这通常发生在真实机制较长,而存在许多更短但同样化学合理的替代路径时。
对未见机制的间接验证
为了验证模型真正具备“发现能力”,研究人员选取了六个不在训练集中的最新酶机制进行测试。
结果显示,MechFind在所有六个案例中均成功将真实机制排入前六位预测。
其中,一个人类泛素连接酶(ubiquitin-conjugating enzyme)的机制预测尤为典型。虽然模型并不知道泛素具体结构,但它识别出了与乙酰辅酶A中的硫酯和赖氨酸氨基类似的反应基团,并成功组合已有规则推断出正确连接方式。
研究人员认为,这说明不同物种之间存在某种“通用化学语法(universal chemical grammar)”。
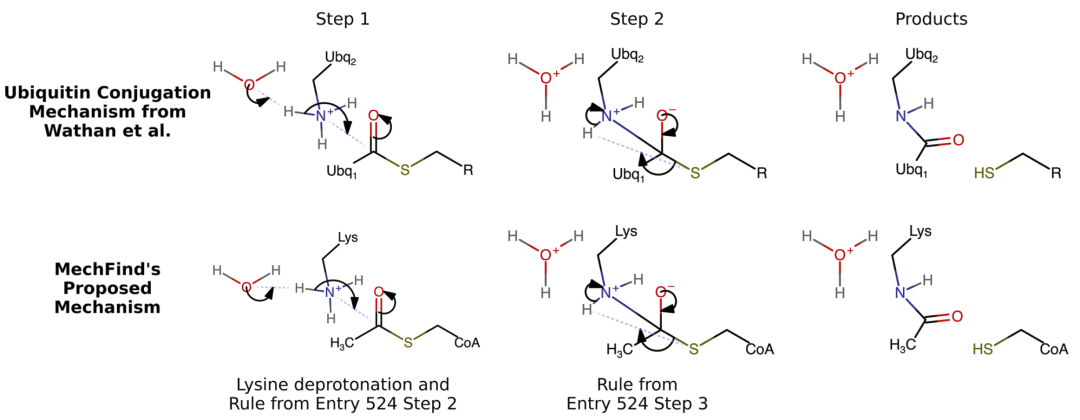
图3:MechFind预测的人类泛素连接酶机制与真实机制比较。
大规模机制注释
研究人员随后将MechFind扩展到Rhea和MetaNetX数据库。
在14,931个Rhea反应中,MechFind为8,452个反应成功生成至少一种合理机制,占56.6%;在MetaNetX中,成功率达到59.1%。
总体而言,研究人员生成了超过18,000个机制假设,相比此前MechSearch仅能处理约942个Rhea反应,实现了数量级提升。
这一结果意味着,MechFind首次能够以高通量方式系统扩展酶机制数据库。
与现有方法的比较
研究人员进一步将MechFind与MechSearch进行直接比较。
最大的区别在于输入需求。MechSearch需要用户提供活性位点残基,而MechFind仅需要整体反应计量关系,因此适用于更广泛的酶反应。
同时,MechFind的规则库来源于734个M-CSA机制,几乎是MechSearch使用规则数量的两倍。
在Rhea数据库测试中,MechFind成功率达到57%,远高于MechSearch报道的11%。
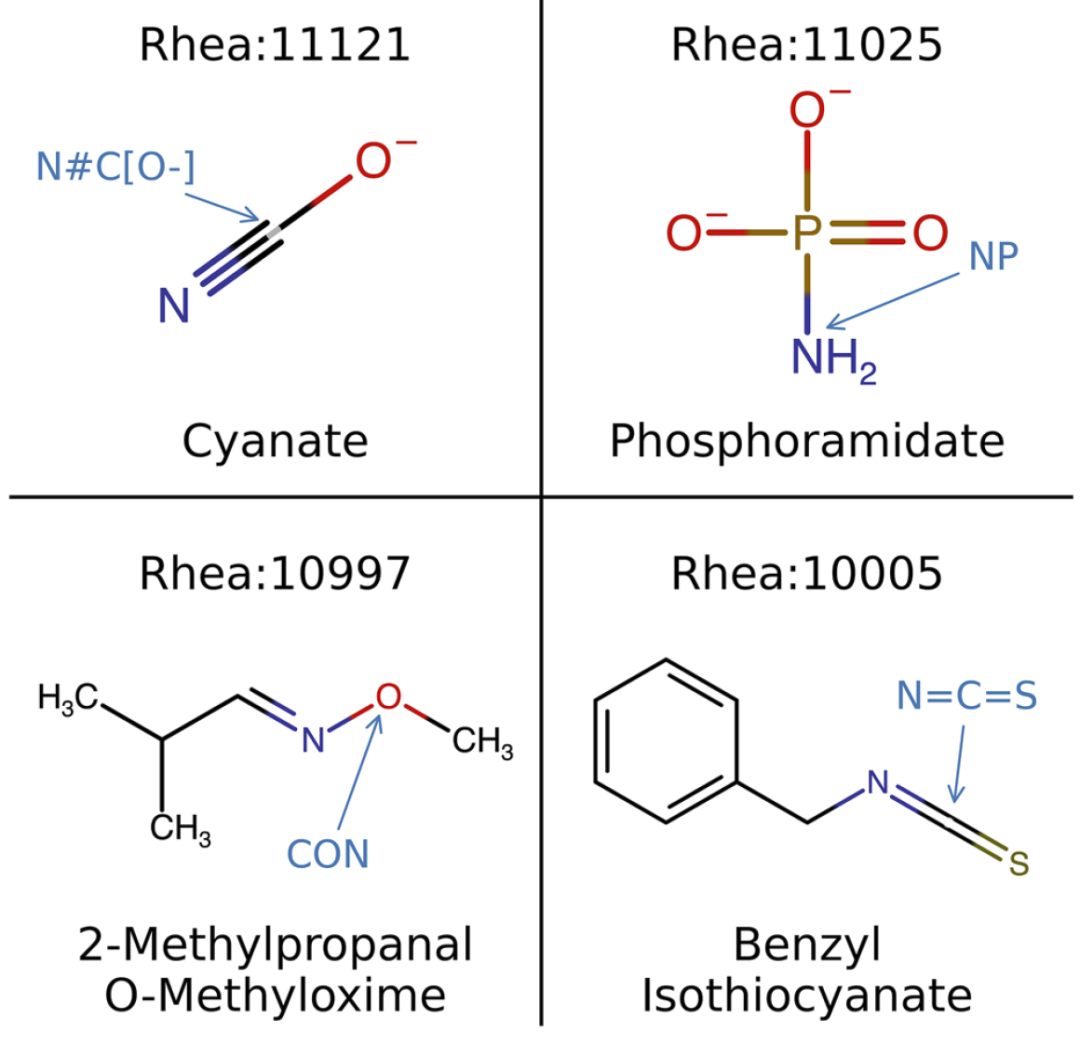
图4:MechFind与MechSearch在输入需求与预测能力上的比较。
探索机制多样性
除了寻找“最优机制”,MechFind还能够生成同一反应的多个合理催化路径。
研究人员以经典酯酶反应为例,构建了由前十个预测机制组成的“机制网络”。结果发现,同一反应可能存在多种合理策略,例如通过丝氨酸共价中间体进行催化,或通过水分子直接亲核攻击完成反应。
研究人员认为,这种机制多样性对于de novo酶设计尤其重要,因为不同机制对应不同过渡态,而不同过渡态又对应不同活性位点设计策略。
因此,MechFind不仅是预测工具,更是一个机制探索引擎。
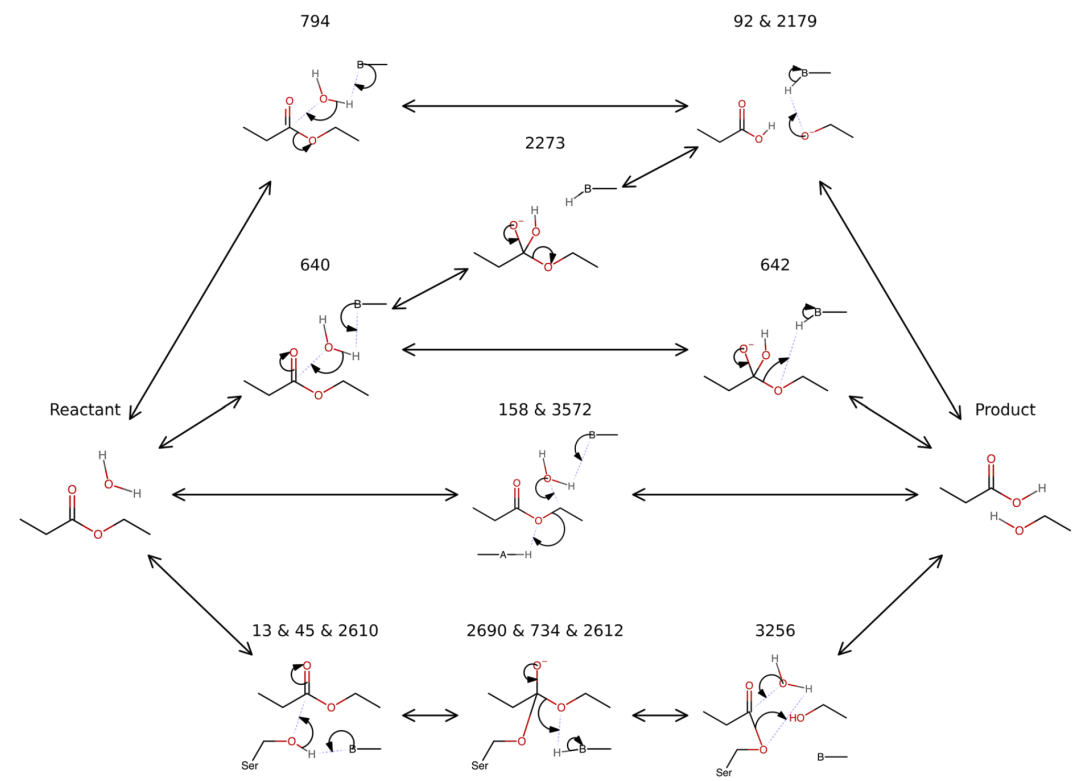
图5:经典酯酶反应的多机制网络。
讨论
研究人员认为,MechFind最大的突破在于摆脱了对蛋白结构和活性位点信息的依赖,从而首次实现真正意义上的高通量酶机制预测。
通过化学基团抽象,模型能够识别不同物种、不同分子背景下共享的催化逻辑。这意味着酶催化并非无限复杂,而可能由相对有限的一组基本化学规则组合而成。
研究人员进一步提出,这种“通用化学语法”可能成为未来AI驱动酶设计的重要基础。
与此同时,MechFind也存在明显局限。例如,约17%的Rhea反应因为排序优化问题超时失败;另有26%的反应包含训练集中未出现的新化学基团,因此无法预测机制。
此外,目前框架尚未完整处理立体化学,仅使用构造异构体进行表示。未来如果加入立体专一规则,将能够处理更加复杂的酶机制。
研究人员最后强调,MechFind真正的重要意义,可能在于它与新一代蛋白生成模型形成闭环。
例如,RFdiffusion All-Atom和ProteinMPNN已经能够生成高质量蛋白结构,但这些模型需要明确的过渡态目标。而MechFind生成的机制假设恰恰能够提供这些关键过渡态信息。
因此,研究人员认为,MechFind有望成为未来“自动化酶设计(automated enzyme design)”流程中的核心组成部分。
整理 | DrugOne团队
参考资料
Hartley, A.D., Upadhyay, V., Boorla, V.S. et al. MechFind: a computational framework for de novo prediction of enzyme mechanisms. Nat Commun 17, 3903 (2026).
https://doi.org/10.1038/s41467-026-71957-0

本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-05-07,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

