【染色质可及性】ATAC-seq实验方案1-经典版文章介绍与解读
【染色质可及性】ATAC-seq实验方案1-经典版文章介绍与解读
三兔测序学社
发布于 2026-05-08 10:06:00
发布于 2026-05-08 10:06:00
编者语:博二研究生期间,博导发给我这篇文章,让我试着做一下ATAC-seq,当时我是课题组第一个尝试做ATAC-seq的研究生,没想到第一次做就做出来了,数据质量不错,没想到是新手运气效应,第2-3次再重复时候,数据背景噪音很大,实验失败。再后来反复研读文章,优化实验条件,增加分选细胞活力,实验才得以再一次成功。
ATAC-seq: A Method for Assaying Chromatin Accessibility Genome-Wide
文章来源
Buenrostro JD, Wu B, Chang HY, Greenleaf WJ. ATAC-seq: A Method for Assaying Chromatin Accessibility Genome-Wide. Curr Protoc Mol Biol. 2015 Jan 5;109:21.29.1-21.29.9. doi: 10.1002/0471142727.mb2129s109. PMID: 25559105; PMCID: PMC4374986.
背景信息
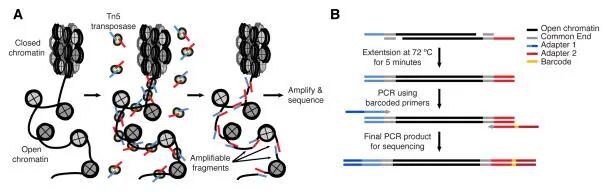
ATAC-seq 方法依赖于使用超活化转座酶 Tn5 的文库构建。Tn5 是一种原核生物转座酶,通过“切入-粘合”机制起作用,要求对包含 19 个碱基对倒位重复序列的位点进行特异性切除。有测序接头的 Tn5 转座酶可以形成一个活跃的二聚转座复合体。这种转座酶优先将测序接头插入裸露的 DNA 区域,因此可以作为测量基因组范围内染色质可接近性的一种探针。
试剂耗材设备
Phosphate Buffered Saline (PBS)
Molecular biology grade IGEPAL CA-630 (解读:就是NP-40)
Lysis buffer (10 mM Tris-HCl, pH 7.4, 10 mM NaCl, 3 mM MgCl2, 0.1% IGEPAL CA-630)
2x TD (2x reaction buffer, Illumina Cat #FC-121-1030)
TDE1 (Nextera Tn5 Transposase, Illumina Cat #FC-121-1030)(解读:国内诺唯赞,翌圣等厂家具有同等产品)
Qiagen MinElute PCR Purification Kit(解读:Qiagen MinElute PCR Purification Kit可以回收>70bp的DNA片段,用Qiagen PCR Purification Kit也可以,回收100bp以上DNA,不推荐其他品牌PCR回收试剂盒)
NEBNext High-Fidelity 2x PCR Master Mix (New England Labs Cat #M0541)
25 uM Custom Nextera PCR Primer 1
25 uM Custom Nextera PCR Primer 2
100x SYBR Green I (Invitrogen Cat #S-7563)
0.2-ml PCR tubes
PCR Thermal cycler
qPCR consumables, products are specific to the instrument(解读:需要qPCR仪器)
细胞准备
1.Harvest cells, protocol to be defined by the user. Cells should be intact and in a homogenous single cell suspension.(解读:细胞活力很重要,否则细胞DNA游离出来,造成非特异性DNA背景)
2.Spin down 50,000 cells at 500 ×g for 5 min, 4°C. The number of cells at this step is crucial as the transposase to cell ratio sets the distribution of DNA fragments generated. See Critical Parameters.
3.Wash once with 50 μl of cold 1x PBS buffer. Spin down at 500 ×g for 5 min, 4°C.
4.Gently pipette to resuspend the cell pellet in 50 μl of cold lysis buffer. Spin down immediately at 500 ×g for 10 min, 4°C. This step provides lysis of cells with non-ionic detergent and generates of a crude nuclei preparation.
5.Discard the supernatant, and immediately continue to transposition reaction.
转座反应
1.Make sure the cell pellet is set on ice.
2.To make the transposition reaction mix, combine the following: 25 μl TD (2x reaction buffer) 2.5 μl TDE1 (Nextera Tn5 Transposase) 22.5 μl Nuclease Free H2O
3.Resuspend nuclei in the transposition reaction mix.
4.Incubate the transposition reaction at 37°C for 30 min.(解读:金属加热仪器上进行) Gentle mixing may increase fragment yield.
5. Immediately following transposition, purify using a Qiagen MinElute PCR Purification Kit.
6. Elute transposed DNA in 10 μl Elution Buffer (10 mM Tris buffer, pH 8).(解读:实际用 30 μl Elution Buffer溶解比较合理)
7. Purified DNA can be stored at −20°C. This is a convenient stopping point. Please note that these DNA fragments are not PCR amplifiable if melted at this point.
PCR 扩增
1.To amplify transposed DNA fragments, combine the following in a 0.2 ml PCR tube:
10 μl Transposed DNA
10 μl Nuclease Free H2O
2.5 μl 25 μM Custom Nextera PCR Primer 1
2.5 μl 25 μM Custom Nextera PCR Primer 2
25 μl NEBNext High-Fidelity 2x PCR Master Mix A complete list of primers is available in Buenrostro et al. Care should be taken to ensure that samples are barcoded appropriately for subsequent pooling and sequencing.
2.Thermal cycle as follows:
1 cycle of 72°C for 5 min, 98°C for 30 sec
5 cycles of 98°C for 10 sec, 63°C for 30 sec, 72°C for 1 min
This first 5 minute extension at 72°C is critical to allow extension of both ends of the primer after transposition, thereby generating amplifiable fragments . This short pre-amplification step ensures that downstream quantitative PCR (qPCR) quantification will not change the complexity of the original library.
3. To reduce GC and size bias in PCR, the appropriate number of PCR cycles is determined using qPCR allowing us to stop amplification prior to saturation. To run a qPCR side reaction, combine the following in qPCR compatible consumables(解读:根据qPCR获得扩增曲线,得到合理的扩增循环数):
5 μl of previously PCR amplified DNA
4.41 μl Nuclease Free H2O
0.25 μl 25 μM Customized Nextera PCR Primer 1
0.25 μl 25 μM Customized Nextera PCR Primer 2
0.09 μl 100x SYBR Green I
5 μl NEBNext High-Fidelity 2x PCR Master Mix
4.Using a qPCR instrument, cycle as follows:
1 cycle of 98°C for 30 sec
20 cycles of 98°C for 10 sec, 63°C for 30 sec, 72°C for 1 min
5.To calculate the additional number of cycles needed, plot linear Rn versus cycle and determine the cycle number that corresponds to ¼ of maximum fluorescent intensity。
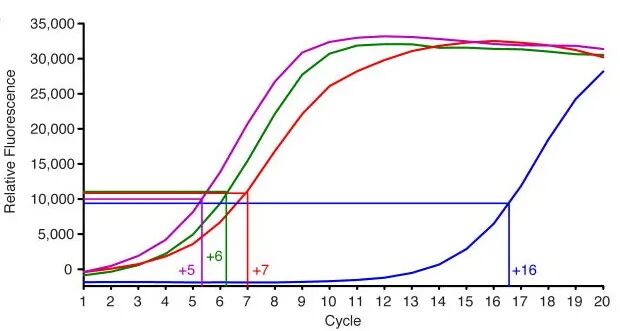
The purpose of this qPCR step is to generate libraries that are minimally PCR amplified. Most PCR bias comes from later PCR cycles that occur during limited reagent concentrations. This determination of the optimal number of cycles to amplify the library reduces artifacts associated with saturation PCR of complex libraries(解读:由于qPCR仪器扩增效率高于PCR仪器,Santbiolabs经验是选择最大荧光强度1/2处对于循环数作为接下来的扩增循环数).
6.Run the remaining 45 μl PCR reaction to the cycle number determined by qPCR. Cycle as follows:
1 cycle of 98°C for 30 sec
N cycles of 98°C for 10 sec, 63°C for 30 sec, 72°C for 1 min
Cycle for an additional N cycles, where N is determined using qPCR.
7.Purify amplified library using Qiagen MinElute PCR Purification Kit. Elute the purified library in 20 μl Elution Buffer (10 mM Tris Buffer, pH 8). Be sure to dry the column before adding elution buffer.
The concentration of DNA eluted from the column ought to be approximately 30 nM, however 5-fold variation is possible and not detrimental(解读:通常直接用Qbit微量DNA检测试剂检测浓度).
关键参数
细胞数目 ATAC-seq 对细胞数目的变化通常较为稳健(例如,大约 25k 到 75k 细胞)。一般来说,细胞数过少会导致染色质过度消化,并使得大量测序读取映射到基因组的不可接近区域(即噪音);而细胞数过多则会导致消化不足,产生高分子量片段,可能难以进行测序。然而,细胞总数还决定了测序文库的基本多样性(即唯一 DNA 片段的数量)。我们注意到,为了获得更复杂的文库,可以使用更大的反应体积,或者使用相同反应体积进行串联反应。
细胞收集 细胞收集方法有所不同,并且可能需要根据 ATAC-seq 优化。我们发现固定液会降低转座频率,因此不推荐使用。同时,机械剪切方法会显著减少信号噪声。采用高纯度的方法,生产完整细胞并形成均一的单细胞悬浮液,通常能获得最佳的数据集。
PCR 和片段分布 所描述的 PCR 方法旨在减少文库构建过程中的大小和 GC 偏差。这些方法对 ATAC-seq 特别有效,因为其片段大小高度多样。我们发现,含有过多大片段(>1 kb)的样品较难定量,并且在测序时会降低聚类效率。如果文库中长片段过多,可以通过调整每个反应中的细胞数量来优化文库的片段化。或者,在测序之前可以进行大小选择,去除这些可能影响结果的长片段。尽管常见的做法是选择狭窄的片段区间进行大小选择,但我们推荐选择一个较大的片段大小窗口(100–1000 bp),以保持高文库复杂度,并从完整的片段大小分布中提取更多丰富的信息。所描述的 PCR 方法还有一个附加的好处,即作为文库复杂度的估算。如果需要超过 6 个额外的循环(>11 总循环),文库复杂度可能会成为一个问题。通过优化输入细胞数目或通过制作技术重复的文库,可以改善文库复杂度(解读:实际文库大小选择使用了磁珠分选,另外,总文库扩增循环次数往往大于11个循环数,因此增加技术重复与生物学重复,在下游生物信息学分析中减少组内差异)。
文库定量 我们使用基于 qPCR 的方法来定量 ATAC-seq 文库。我们发现,其他方法,如 Qubit,可能会因片段大小分布的差异而给出误导性和不准确的结果。我们推荐使用 KAPA Library Quant Kit for Illumina Sequencing Platforms(KAPABiosystems)来定量文库。或者,可以使用 Bioanalyzer 蛋白质分析仪的集成痕迹来近似估算文库浓度。
测序 ATAC-seq 和 Nextera 工作流是为使用 Illumina 高通量测序仪而设计的。在测序 ATAC-seq 文库时,必须使用 Nextera 版本的测序引物和试剂。根据测序仪的不同,这可能需要修改标准的测序工作流程。对于核小体映射,推荐使用双端测序。50 个循环的双端读取通常能够提供准确的比对并保持合理的成本。为了推断人类样本中开放染色质的差异,我们通常使用 >50M 的比对读取,而对于转录因子足迹分析,则使用 >200M 的比对读取(Neph 等,2012)。数据产量有时会受到大量线粒体读取的影响。对于聚类密度和测序质量的问题,请参考 Illumina 的技术支持人员。
故障排除 假设目标细胞在开始程序之前健康且完好无损,最大的问题来源通常是细胞数目的变化。一般来说,添加过多的细胞会导致“转座不足”(即大部分为长片段),而添加过少的细胞则会导致“转座过度”,产生大量短片段,这会在胶上产生难以辨识的带型,甚至可能完全消失。在将此方案应用于非人类细胞时,我们看到根据物种不同,所需细胞数差异较大;不过,结果的变化也可能来自不同的细胞类型。如果使用标准方案的结果不理想,一种有效的优化方法是将反应规模缩小 10 倍,并优化裂解方法和细胞数量,从每反应 5000 细胞开始。图 2 中所示的核小体带型与高质量文库相关。
预期结果 在测序人类文库后,我们通常发现大约一半的读取是亚核小体长度的(大约小于 150 bp),另外一半的读取则较长。一般来说,我们发现与 DNase-seq 方法高度一致,并且在开放染色质区域具有富集,约 20% 的读取集中在大约 2% 的基因组区域内。我们估计,一次 50 µl 反应体积可以生成大约 50–100M 个唯一可放大的片段。
时间考虑 ATAC-seq 设计时考虑到了速度;我们已将实验方案优化至总时间为 3 小时。上述实验方案中的细胞核提取需 30 分钟,转座和纯化需要 45 分钟,PCR 和纯化则需要 1 小时 45 分钟。QC 和文库定量方法可能会有所不同。转座和DNA纯化后有一个自然的中断点,此时 DNA 片段可以在 PCR 扩增之前无限期冷冻。
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-05-06,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读
目录

