文献分享--解析乳腺癌脑转移的细胞结构揭示了预后不同的免疫景观
原创文献分享--解析乳腺癌脑转移的细胞结构揭示了预后不同的免疫景观
原创
追风少年i
发布于 2026-04-29 09:13:07
发布于 2026-04-29 09:13:07
作者,Evil Genius
马上五一了,大家有什么打算么?买到票的可以回家住几天,决定留在单位的,周围可以转转,别去那些景点,放假的时候是个景点都人满为患,科研人员没安排的话,精心梳理梳理之前的科研工作,复盘也是非常重要的一部分。
希望大家早日不为生计发愁。
今天我们分享文献

知识积累
乳腺癌(BC)是女性最常见的恶性肿瘤,也是一种高度异质性的疾病。全身治疗需根据主要亚型——管腔型乳腺癌、人表皮生长因子受体2(HER2)过表达型乳腺癌及三阴性乳腺癌(TNBC)——进行精准定制。
高达32%的转移性乳腺癌患者会发生脑转移(BCBM)。 BCBM的治疗策略包括手术、放疗和全身治疗。然而,与其他部位转移的患者相比,BCBM患者中位生存期仅16个月,预后最差。
肿瘤浸润淋巴细胞(TIL)的数量在BC各亚型中具有预后价值,且新辅助化疗后TIL的增加与病理学肿瘤缓解相关,这强调了BC中免疫反应的临床重要性。
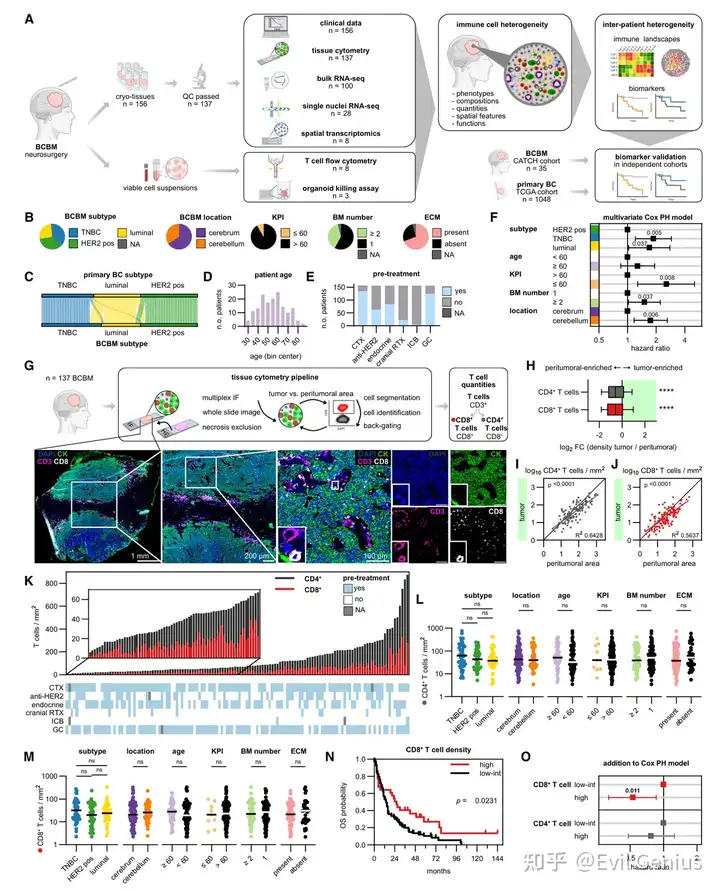
结果1、CD8⁺ T细胞浸润BCBM可预测总生存期,且独立于临床预后变量
BCBM中CD8⁺ T细胞的浸润密度是一个强有力的生存预后指标,且其预测价值独立于已知的临床因素(如亚型、KPI、转移灶数量和小脑位置)。
小脑BCBM预后极差,是未被现有GPA评分包含的新发现。
T细胞在瘤周和瘤内区域的数量呈正相关,表明血脑屏障是T细胞进入的关键限制步骤,而脑内微环境并不主动排斥T细胞浸润肿瘤。
CD4⁺ T细胞浸润与临床参数或生存期无显著关联,突出了CD8⁺ T细胞在抗肿瘤免疫控制中的核心地位。
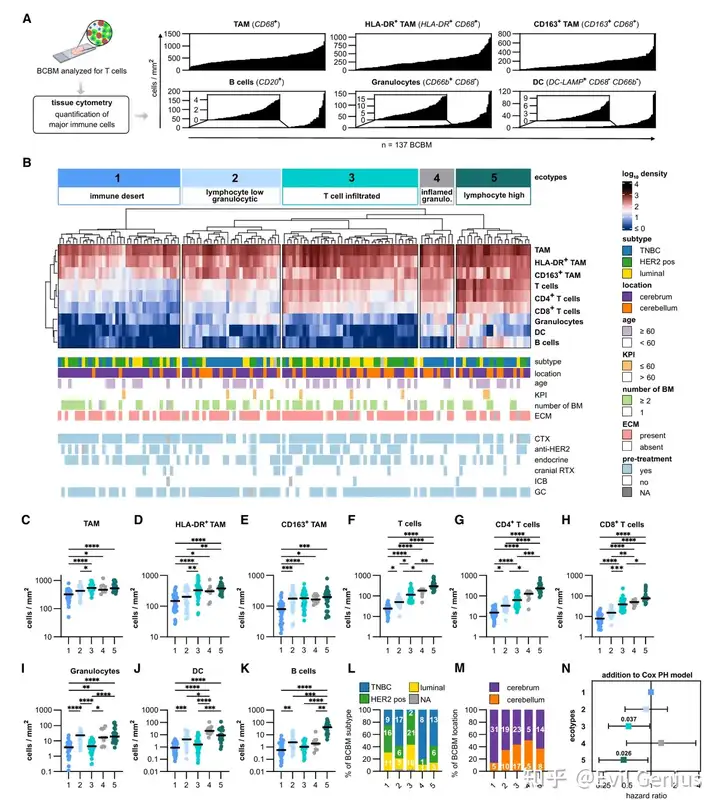
结果2、BCBM免疫浸润以细胞类型整合方式形成免疫生态型
对BCBM中多种免疫细胞丰度的整合聚类,识别出五种免疫生态型:
生态型1(免疫沙漠型):免疫细胞稀少,在小脑中最不常见,暗示不同脑区免疫细胞进入能力不同。
生态型2:低淋巴细胞伴高粒细胞,TNBC亚型多见。
生态型3(T细胞/TAMs为主型):与更长生存期独立相关,提示T细胞和免疫刺激性TAMs共同介导肿瘤控制。
生态型4:以粒细胞等更广谱炎症细胞为特征,也常见于TNBC。
生态型5(B细胞丰富型):B细胞高浸润,是另一个独立良好预后标志,说明B细胞可能在抗肿瘤免疫中发挥重要作用。
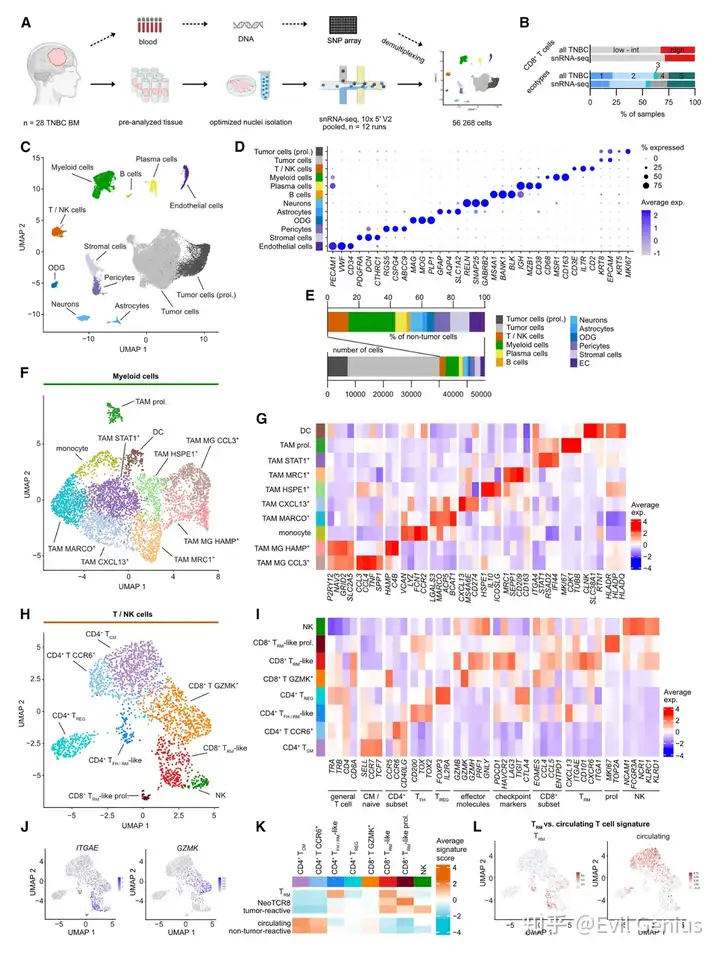
结果3、snRNA-seq分析揭示TNBC脑转移的细胞组成架构
细胞图谱:共解析出12种主要细胞类型,肿瘤细胞占71%,非肿瘤部分包括脑驻留细胞、血管细胞和多种免疫细胞,其中髓系细胞比例最高。
TAM亚群细分:髓系细胞包含8个TAM亚群,不遵循简单的M1/M2分类,而是呈现多种功能状态,包括免疫刺激性和免疫抑制性两种表型。
预后相关TAM亚群:四个高表达HLA-DR和抗原呈递相关基因的TAM亚群(STAT1⁺、HSPE⁺及两个MG样亚群)与良好预后相关,尤其是两个MG样TAM亚群的基因签名在独立数据中验证了生存获益。
免疫抑制性TAM:另一类TAM(如MRC1⁺、MARCO⁺、CXCL13⁺)高表达免疫抑制分子(如PD-L1),可能参与免疫逃逸。
这些单细胞数据与组织细胞计数结果相互印证,深入揭示了TNBC脑转移中髓系细胞的功能异质性和临床相关性。
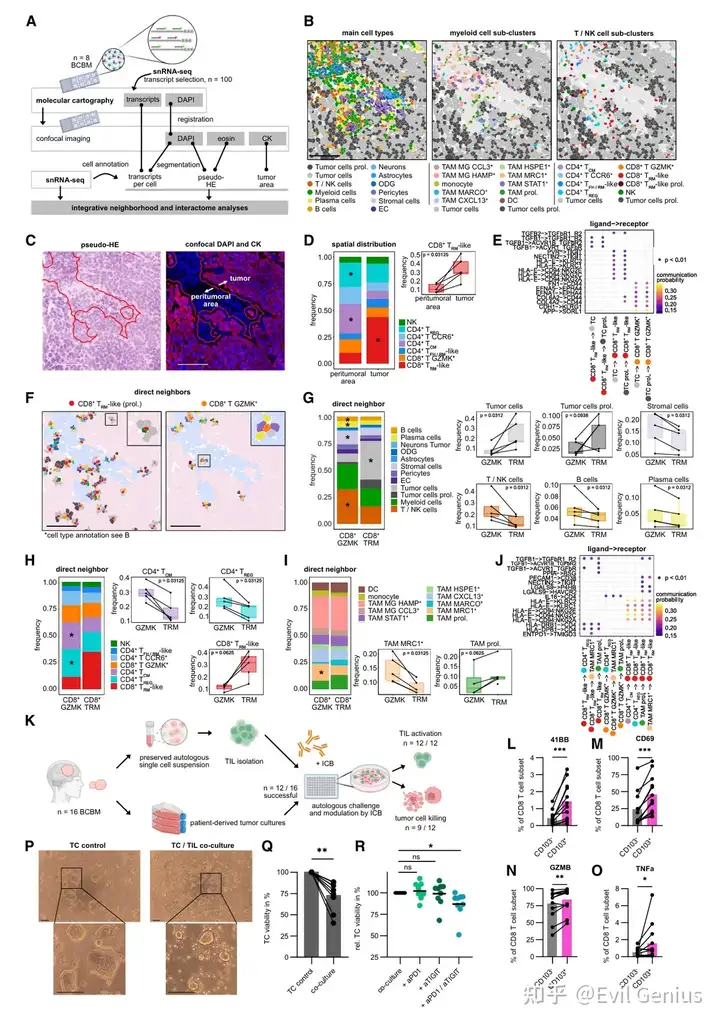
结果4、BCBM富含高表达活化和功能标志物、并展现肿瘤杀伤能力的CD8⁺ TRM样细胞
通过单细胞核RNA测序对BCBM中的T/NK细胞进行亚群解析,主要发现:
CD4⁺ T细胞异质性:包括中央记忆T细胞(TCM)、CCR6⁺ T细胞以及含滤泡辅助/驻留特征的亚群;其中20%为调节性T细胞(TREG),这解释了整体CD4⁺ T细胞浸润无预后价值的原因。
CD8⁺ T细胞两大亚群:
CD8⁺ TRM样细胞:高表达PD-1、效应分子(GZMB、GZMH、PRF1)及组织驻留标志物(CD103),并具增殖活性和肿瘤反应性T细胞特征,是抗肿瘤免疫的潜在核心执行者。
CD8⁺ T GZMK⁺细胞:免疫检查点表达较低,以GZMK高表达为特征。
NK细胞:数量稀少,其特异性基因特征未显示预后关联。
结果突显了CD8⁺ TRM样细胞在BCBM免疫控制中的关键功能角色,与组织细胞计数中CD8⁺ T细胞总体密度的良好预后作用相呼应。
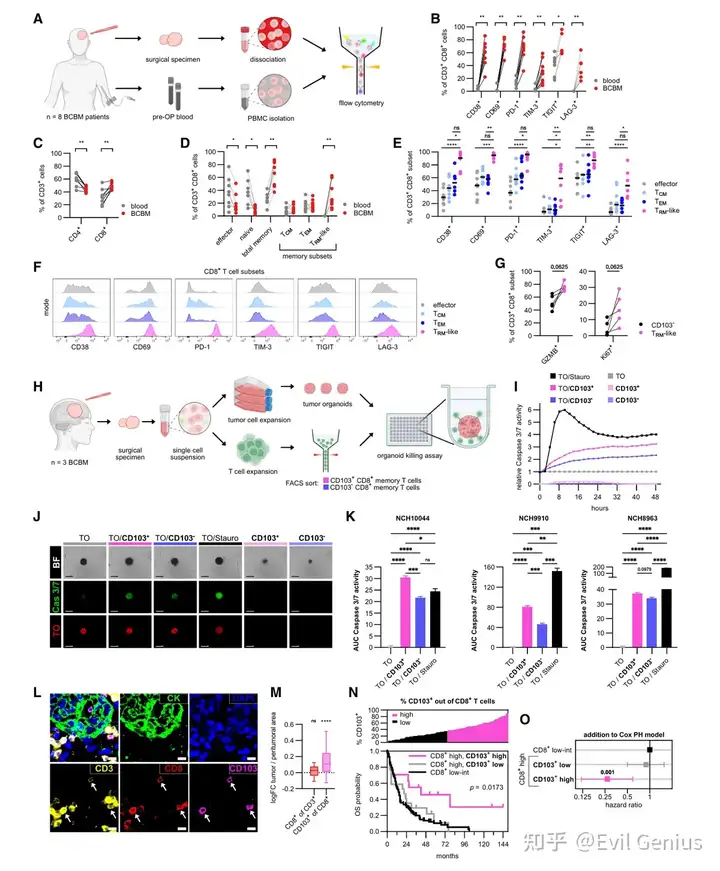
结果4、高比例的CD8⁺ TRM样细胞与良好的患者预后相关
流式细胞术验证CD8⁺ T细胞表型及活化状态
来源:选取8例新鲜切除BCBM样本,与患者术前外周血配对比较。
主要发现:
BCBM浸润的CD8⁺ T细胞与外周血T细胞表型显著不同,整体呈现更高的活化标志物和免疫检查点分子表达。
BCBM中富集CD8⁺ 记忆T细胞,特别是CD103⁺ 的CD8⁺ TRM样细胞,这些细胞具有抗原经历表型(CD45RO⁺ CD45RA⁻ CCR7⁻)。
与其他记忆/效应亚群相比,CD8⁺ TRM样细胞高表达CD38、CD69、PD-1、TIM-3、TIGIT、LAG-3等活化及抑制性受体,并呈现更高的GZMB和Ki-67水平趋势,表明其兼具活化、效应和增殖潜能。
自体肿瘤类器官杀伤实验证实CD8⁺ TRM样细胞的强效杀伤功能
方法:建立完全自体来源的肿瘤类器官-T细胞共培养体系,比较分选的CD8⁺ TRM样细胞与CD8⁺ 非TRM样记忆T细胞的杀瘤能力。
结果:
两种CD8⁺ T细胞亚群均能诱导肿瘤细胞凋亡,具有肿瘤控制功能。
CD8⁺ TRM样细胞的杀伤能力显著强于CD8⁺ 非TRM样记忆T细胞,从功能上证实了其在抗肿瘤免疫中的核心地位。
CD8⁺ TRM样细胞的预后价值与空间分布特征
队列验证:在137例BCBM全组织队列中,通过组织细胞计数(CD8/CD103双染)定量分析。
空间富集:CD8⁺ TRM样细胞在肿瘤岛内的比例显著高于瘤周区域,这种瘤内富集与其需要接触并杀伤肿瘤细胞的生物学功能高度吻合。
独立预后意义:在CD8⁺ T细胞高浸润的BCBM中,CD8⁺ TRM样细胞比例高仍可在单变量和多变量模型中独立预测更长的总生存期。这表明即使整体CD8浸润程度相同,TRM样细胞占比也能进一步区分预后优劣。
TRM免疫景观的提出及其泛化性
定义:基于上述发现,研究团队定义了一种“CD8⁺ TRM样细胞相关免疫景观”,存在于约11%的BCBM样本中。
特征:此景观除富含CD8⁺ TRM样细胞外,还伴有高评分的抗原呈递相关基因签名,提示CD8⁺ TRM样细胞与抗原呈递细胞(如特定TAM亚群)之间存在功能协同。
分布广度:该景观不仅限于某个特定免疫生态型,而是分布在所有高T细胞浸润的生态型(3、4、5型)中,并且跨越不同BCBM亚型、患者年龄及既往治疗方式,具有普遍性意义。
结果5、CD8⁺ TRM样细胞在肿瘤内区域呈空间富集,而GZMK⁺ CD8⁺ T细胞则邻近具有免疫抑制表型的免疫细胞
空间富集模式截然不同
CD8⁺ TRM样细胞特异性富集于肿瘤区域内部,与肿瘤细胞空间位置邻近,支持其直接杀伤肿瘤的功能。
GZMK⁺ CD8⁺ T细胞则主要位于基质区域,邻近具有免疫抑制表型的细胞,如MRC1⁺ TAMs和TREG细胞。
与肿瘤细胞的预测互作机制迥异
CD8⁺ TRM样细胞:通过双向TGF-β信号(与TRM细胞维持相关)、HLA-E-CD94/NKG2C活化轴以及PVR/NECTIN2-TIGIT抑制轴与肿瘤细胞互作。
GZMK⁺ CD8⁺ T细胞:主要涉及细胞迁移相关的相互作用,如肿瘤细胞上的FN1/胶原蛋白与T细胞CD44结合,以及EFNA5/EFNA1-EPHA4轴。
微环境邻居组成不同
CD8⁺ TRM样细胞的邻近细胞以肿瘤细胞为主,并有较多增殖性TAMs。
GZMK⁺ CD8⁺ T细胞周围则富集基质细胞、B细胞、浆细胞、CD4⁺ TCM和CD4⁺ TREG。
与免疫抑制细胞的关联差异
GZMK⁺ CD8⁺ T细胞附近显著更多存在MRC1⁺ TAMs(免疫抑制性巨噬细胞)和TREG。
预测CD8⁺ TRM样细胞更多地与具有抗原呈递或促炎潜能的细胞(如增殖性TAMs)相邻。
关键分子互作预测
CD8⁺ TRM样细胞接收来自邻近细胞的HLA-E信号,通过NK相关受体(KLRC1、KLRC2、CD94)传导,可能协同活化或抑制。
GZMK⁺ CD8⁺ T细胞通过分泌IL-16作用于TREG和MRC1⁺ TAMs表面的CD4,可能主动招募或调节这些免疫抑制细胞。
功能意义
两种CD8⁺ T细胞亚群占据不同的空间微环境,预示着CD8⁺ TRM样细胞直接执行瘤内杀伤,而GZMK⁺ CD8⁺ T细胞可能与免疫抑制细胞交互,处于相对受调控或功能受限的状态,这很可能导致了它们在抗肿瘤免疫中的不同角色。
PD-1和TIGIT双重免疫检查点阻断可增强自体BCBM患者来源模型中的肿瘤细胞杀伤
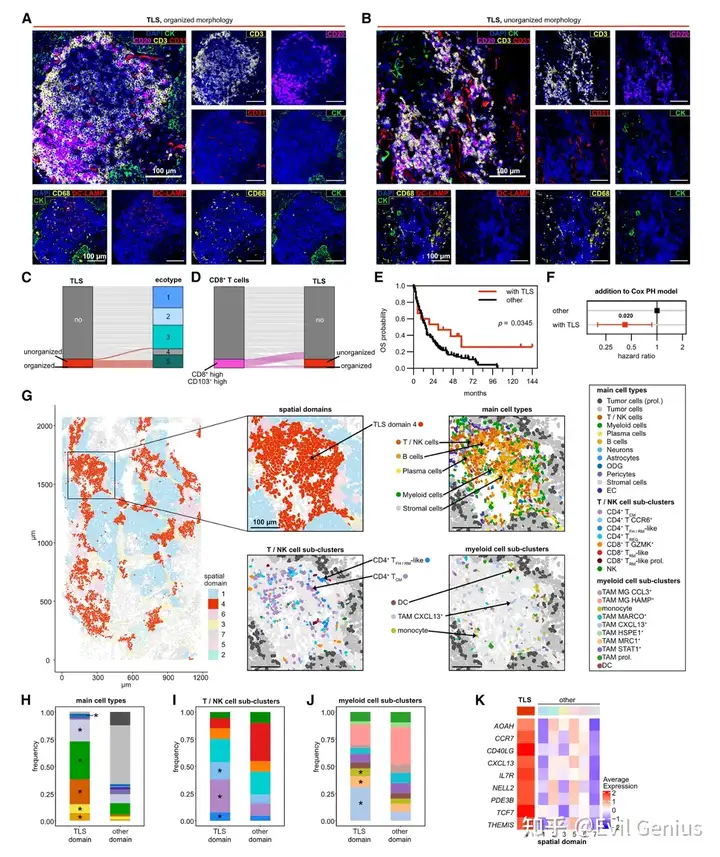
结果6、三级淋巴结构是BCBM中第二个有利的免疫景观特征,具有独特的基因表达特征
TLS的发现与检出率:在约11%的全部BCBM和59%的生态型5病例中,观察到T细胞和B细胞形成大的血管周围聚集体,符合TLS特征。所有TLS均含有成熟的DC-LAMP⁺ DC,且TLS主要存在于TNBC和HER2过表达型BCBM中。
独立且更强的预后价值:TLS的存在能预测更长的患者总生存期,其风险比优于整个生态型5,表明TLS所代表的抗肿瘤免疫过程在功能上尤为重要,是一种独立的良好预后标志。
与CD8⁺ TRM景观几乎不重叠:富集CD8⁺ TRM样细胞的BCBM与含TLS的BCBM极少重叠,提示两者反映了抗肿瘤免疫的不同机制或不同时间阶段。
空间转录组学解析TLS构成:基于细胞注释的空间区域分析证实,TLS区域高度富集T/NK、B、浆细胞、髓系和基质细胞等。其中包含CD4⁺ TCM和具有滤泡辅助性T细胞表型的CD4⁺ TFH/TRM样细胞,后者的高数量在全队列中与良好预后独立相关。
关键细胞亚群和基因签名:TLS区域由高表达B细胞趋化因子CXCL13的TAM亚群主导。差异基因分析进一步得到了一个BCBM特异性的TLS基因签名,包含CXCL13、CD40L、CCR7等特征上调基因,为TLS的功能评估提供了分子标志物。
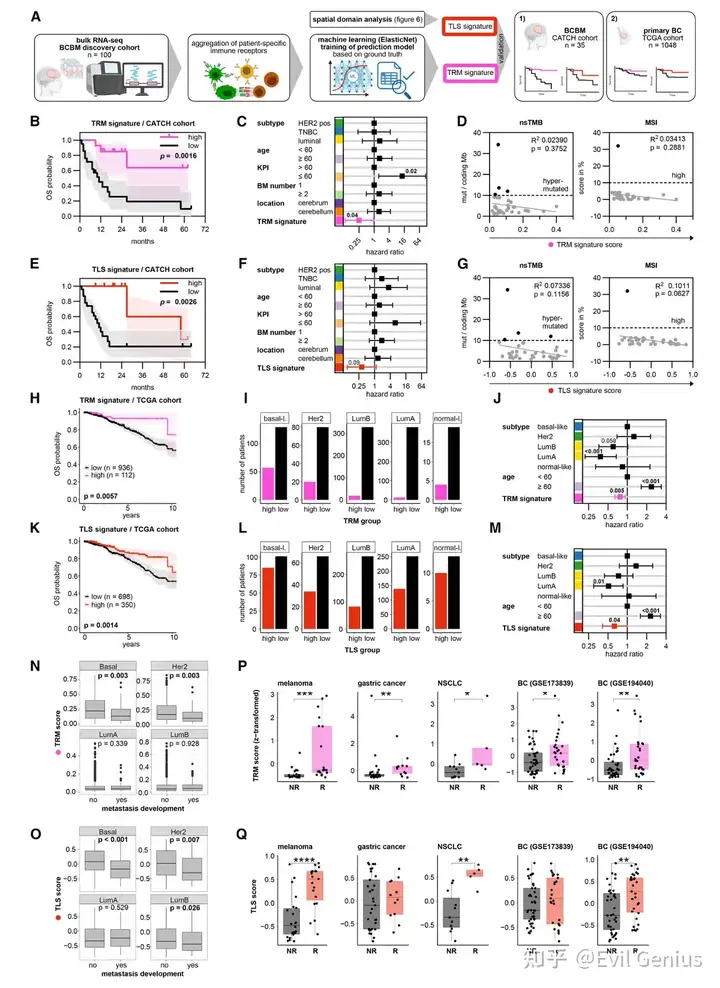
结果7、新型BCBM特异性TRM和TLS特征可预测独立BCBM及原发性BC队列中的患者生存率
TRM特征:以组织细胞计数数据为金标准,利用机器学习从bulk RNA-seq数据中建立,可预测BCBM中TRM免疫景观的存在。
TLS特征:来源于空间转录组学分析,鉴定出TLS特异性上调基因(如CXCL13、CD40L、CCR7)。
在独立BCBM队列(CATCH)中的验证:
TRM特征:高评分与更长总生存期显著相关,且独立于临床变量;与TMB、MSI不相关,提示其提供额外预后信息。
TLS特征:同样展现与更长生存期相关的强烈趋势,且具有独立性。
多重染色验证:证实特征评分可准确预测对应免疫景观及预后。
在原发性乳腺癌(TCGA及大型转移队列)中的验证:
均可扩展至原发BC:TRM和TLS评分在TCGA中均能独立预测更长生存期。
亚型分布:基底样型(对应TNBC)中两种评分的预测患病率最高,管腔型最低;但BCBM中各亚型分布更均衡,提示转移过程中免疫原性可能改变。
转移保护作用:在4088例大型原发BC队列中,未发生转移的患者TRM和TLS评分更高,尤其在基底样型和HER2型中,暗示这两种免疫景观可预防转移。
预测免疫治疗(ICB)疗效:
跨癌种验证:在黑色素瘤、胃癌、肺癌及两个乳腺癌ICB治疗队列中,治疗应答者的TRM评分均显著高于无应答者;TLS评分在黑色素瘤、肺癌和一个乳腺癌队列中也显示类似关联。
ICB特异性潜力:ROC分析显示,联合ICB治疗组的AUC值高于单纯化疗组,提示这两个特征有望成为预测乳腺癌ICB疗效的特异性生物标志物。
最后,我们来看看方法


生活很好,有你更好。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
评论
登录后参与评论
推荐阅读
目录

