STTT 综述 | 重新定位多肽药物,从活性序列到可设计平台
STTT 综述 | 重新定位多肽药物,从活性序列到可设计平台

MindDance
发布于 2026-04-28 19:31:34
发布于 2026-04-28 19:31:34
多肽药物这几年重新变得很热,但这个热并不只是因为 GLP-1 药物卖得好。
更深一层看,多肽药物正在经历一次重新定位。过去我们更多把多肽理解成天然激素、抗菌肽、受体配体,或者某些生物活性片段的药物化利用。它的优势很清楚:靶向性好、活性强、毒性通常较低,也比抗体和蛋白药更容易化学合成。但它的短板也同样明显:容易被蛋白酶降解,体内半衰期短,膜通透性差,很多情况下只能注射给药。
所以,多肽药物长期处在一个有点尴尬的位置。它比小分子更像生物调控分子,比抗体更轻、更容易修饰,但真正进入临床时,又绕不开稳定性、递送和给药方式这些硬问题。
这篇发表在 Signal Transduction and Targeted Therapy 的综述 Advance in peptide-based drug development: delivery platforms, therapeutics and vaccines,我觉得最值得看的地方,不是它列出了多少多肽药物,而是它把多肽药物的几个关键变化放在了同一条线上:市场端的 GLP-1 爆发,技术端的结构修饰和递送系统,肿瘤方向的 peptide-drug conjugates,免疫方向的多肽疫苗,以及发现端的展示库和 AI 设计。

换句话说,多肽药物现在不再只是小分子和抗体之间的中间选项。它正在变成一个可以被设计、被修饰、被递送、被组合的平台型药物空间。
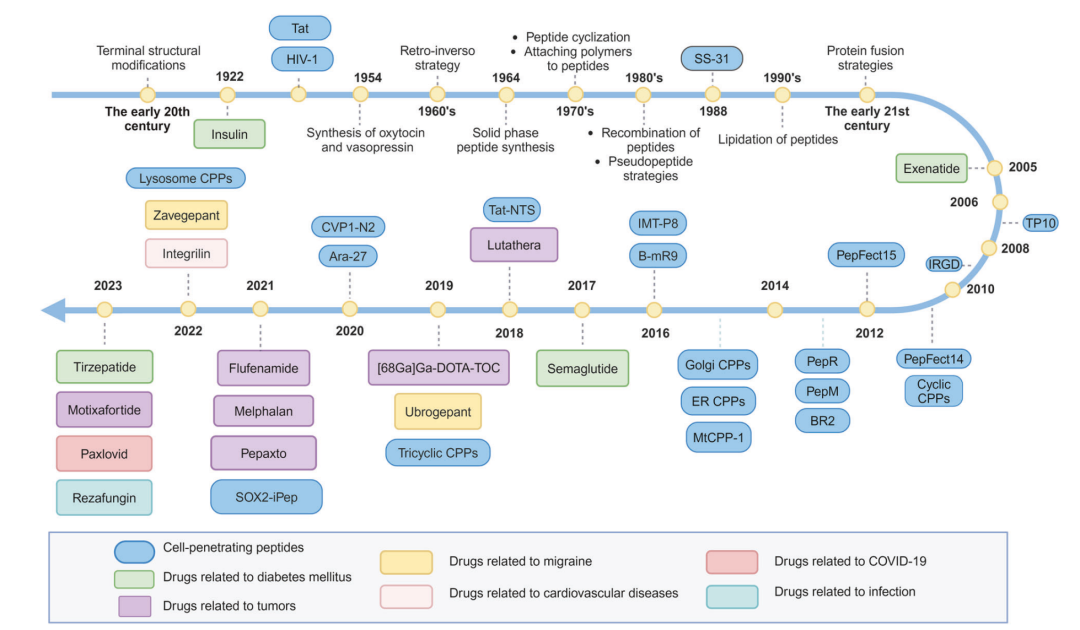
多肽药物发展时间线。上图以时间线形式展示了胰岛素、Lutathera、Semaglutide、Tirzepatide、Paxlovid、Rezafungin、Motixafortide 等代表性多肽相关药物,同时标注了 peptide cyclization、lipidation、protein fusion、cell-penetrating peptides 等结构优化和递送策略的发展节点。
多肽药物发展时间线。上图以时间线形式展示了胰岛素、Lutathera、Semaglutide、Tirzepatide、Paxlovid、Rezafungin、Motixafortide 等代表性多肽相关药物,同时标注了 peptide cyclization、lipidation、protein fusion、cell-penetrating peptides 等结构优化和递送策略的发展节点。
多肽药物的核心矛盾:活性很好,成药性不够自然
多肽有一个很独特的药物学位置。它通常比小分子大,能够覆盖更复杂的蛋白相互作用界面;又比抗体和蛋白药小,在组织渗透、合成成本和结构修饰方面更灵活。对于一些小分子难以处理的靶点,比如蛋白-蛋白相互作用界面、受体配体识别、细胞外基质或某些免疫表位,多肽确实有天然优势。
但它的问题也正来自这种生物分子属性。天然多肽本来就是体内信号的一部分,身体也天然准备好了清除和降解它们的系统。蛋白酶会切它,肾脏会清除它,胃肠道会破坏它,细胞膜也未必让它进去。除少数例外,多数多肽口服后的生物利用度很低,这也是为什么很多商业化多肽药物仍以皮下注射或静脉给药为主。
所以,多肽药物开发的真正难点不是有没有活性序列,而是如何把这个活性序列变成一个体内可用的药物。它需要结构修饰来增加稳定性,需要递送系统来解决到达问题,需要制剂策略来改善给药体验,也需要药代工程来延长作用时间。
下图很适合帮助理解这个矛盾。它把 peptides、small molecules 和 biologics 放在一起比较。这个图真正想表达的不是多肽比谁更好,而是多肽药物必须在生物活性和成药性之间做工程化平衡。
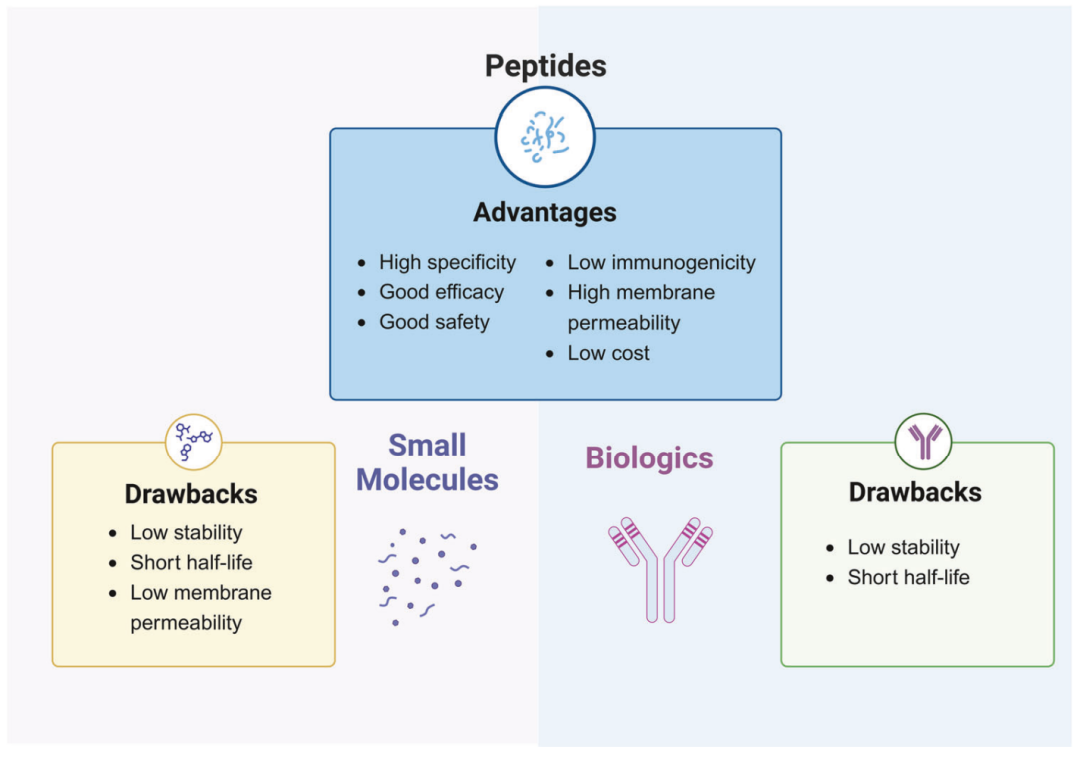
多肽药物的优势与局限。该图比较了多肽、小分子和生物大分子三类治疗分子。多肽兼具高特异性、较好疗效、较低免疫原性和较低生产成本等优势,但也受到稳定性差、半衰期短和膜通透性不足的限制。
多肽药物的优势与局限。该图比较了多肽、小分子和生物大分子三类治疗分子。多肽兼具高特异性、较好疗效、较低免疫原性和较低生产成本等优势,但也受到稳定性差、半衰期短和膜通透性不足的限制。
这轮增长,首先是由 GLP-1 把市场重新打开了
如果只看当前市场,多肽药物最无法绕开的就是 GLP-1 和 incretin 相关药物。
综述中提到,全球已有接近 100 个多肽药物获批,过去二十年多肽药物批准数量持续增长。下图显示,2004 到 2024 年间 FDA 批准的多肽药物数量在不同阶段有所波动,其中 2020–2023 年是批准数量较高的阶段。与此同时,这张图也展示了适应症、给药方式和 III 期临床管线的分布,可以看到内分泌代谢、肿瘤、罕见病和诊断相关方向都占有重要位置。
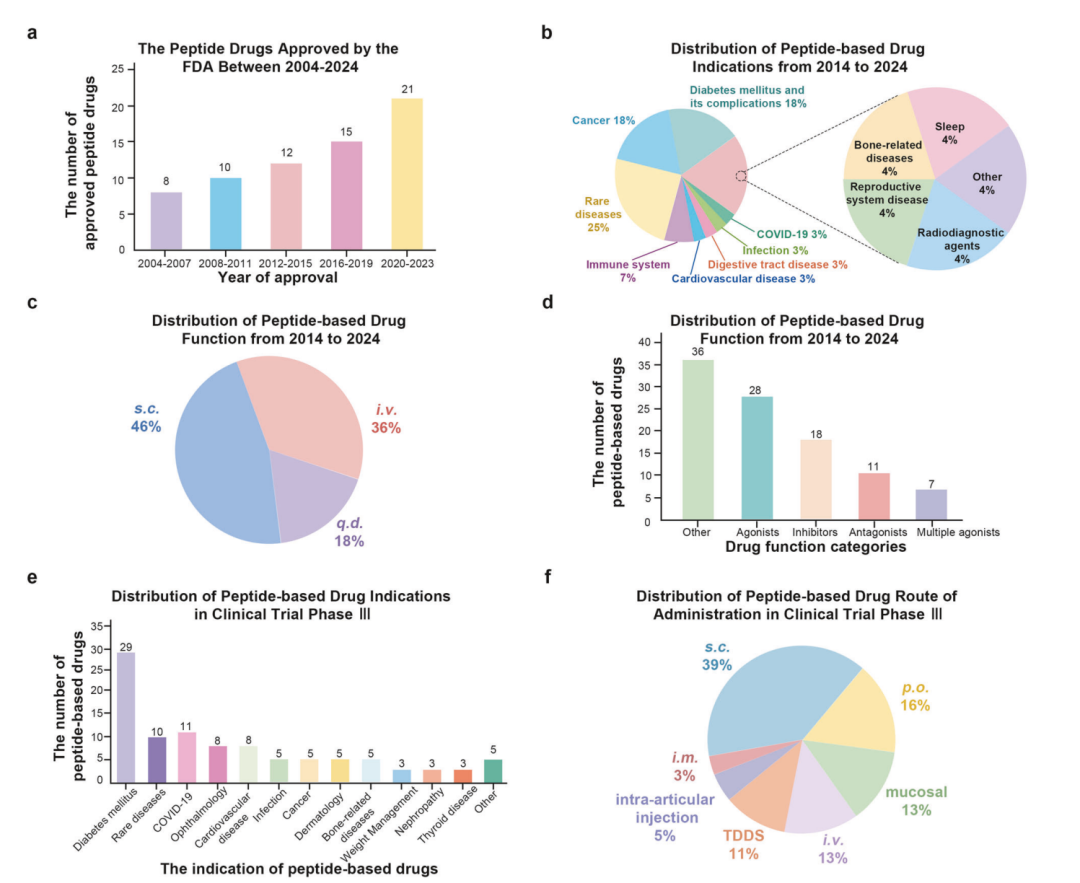
多肽药物市场与临床试验分析
多肽药物市场与临床试验分析
真正把多肽药物推到公众和资本视野中心的,还是 GLP-1 receptor agonists。Semaglutide、dulaglutide、tirzepatide、liraglutide 等药物不仅改变了糖尿病和体重管理的治疗格局,也让多肽药物第一次以非常强势的商业形态进入慢病大市场。
下表列出了 2023 年上半年销售额排名前十的多肽药物。这个表很直观:排名前列基本被糖尿病和体重管理相关药物占据,包括 semaglutide、dulaglutide、tirzepatide、insulin aspart、insulin lispro、liraglutide 等。也就是说,多肽药物市场的扩张,目前很大程度上是由代谢疾病和 GLP-1 / incretin 药物牵引的。
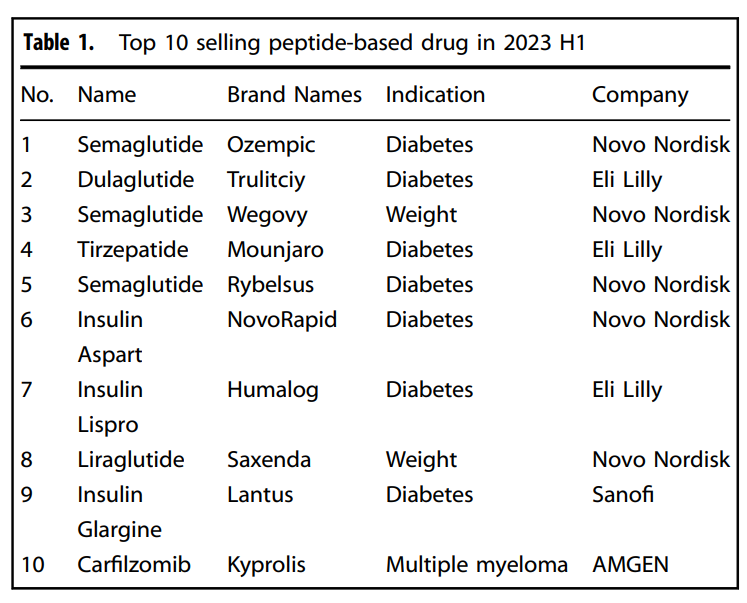
2023 年上半年销售额排名前十的多肽药物
2023 年上半年销售额排名前十的多肽药物
但这里有一个需要保持清醒的地方:GLP-1 的成功不能简单外推到所有多肽药物。它的成功有非常特殊的生物学基础和适应症基础。GLP-1 通路本身具有强临床相关性,慢病人群规模足够大,且结构修饰和长效化策略已经比较成熟。Semaglutide 和 tirzepatide 的成功,并不是天然多肽活性好这么简单,而是生物学、结构工程、药代设计和给药策略一起成立。
所以,GLP-1 更像是多肽药物的一个成熟样板。它告诉我们:当靶点生物学足够扎实,结构工程足够成熟,药代和给药方式足够可接受,多肽完全可以成为主流药物 modality。
结构修饰,是多肽从序列走向药物的第一步
如果说 GLP-1 药物展示的是多肽的临床和商业潜力,那么结构修饰展示的就是多肽成药的底层逻辑。
天然多肽往往不是直接可用的药物。它需要被改造。这里的改造不是简单为了延长一点半衰期,而是系统地改变多肽在体内的命运:让它更难被酶切,让它更容易维持有效构象,让它更适合穿过屏障,让它在血液中停留得更久,也让它更准确地到达目标组织。
下图总结了几类典型策略,包括 cyclization、conjugation、N-terminal modification、C-terminal modification、side chain modification 和 backbone modification。这个图可以看作多肽药物化学的工具箱。
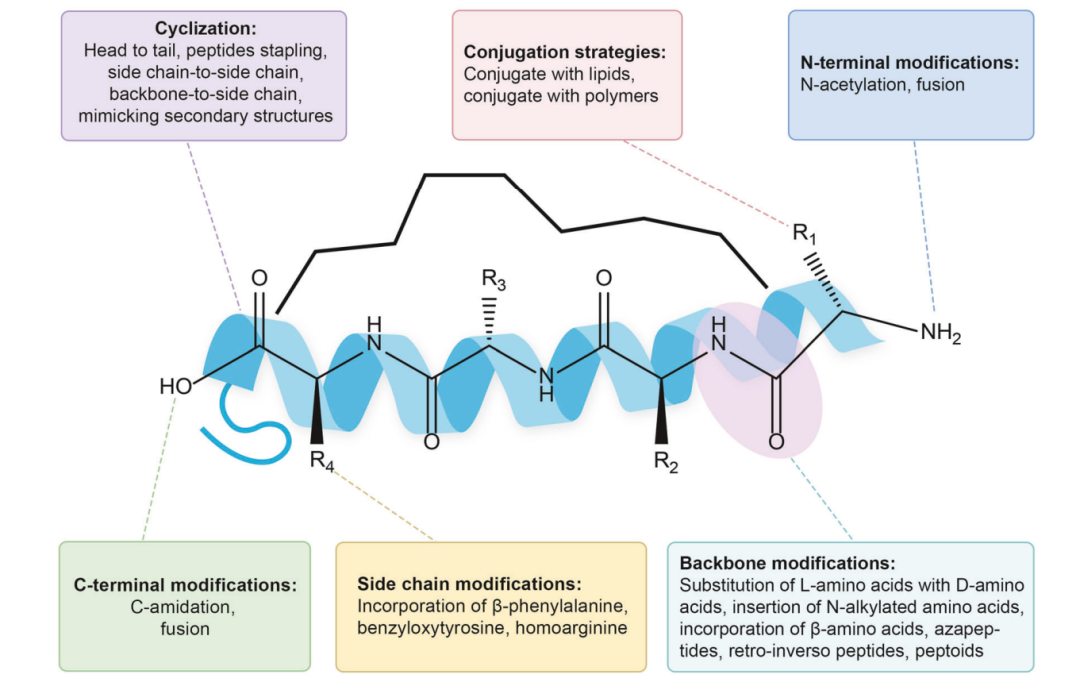
改善多肽药物理化性质的结构修饰策略。该图总结了环化、偶联、N 端修饰、C 端修饰、侧链修饰和骨架修饰等方法。
改善多肽药物理化性质的结构修饰策略。该图总结了环化、偶联、N 端修饰、C 端修饰、侧链修饰和骨架修饰等方法。
Backbone modification 的思路,是改造肽链主链,让蛋白酶不那么容易识别。D-氨基酸替换、N-alkylated amino acids、β-amino acids、retro-inverso peptides、peptoids 等都属于这一类。它们的目标并不是让分子更复杂,而是让天然降解系统失去一部分识别能力。
Cyclization 则是多肽药物里非常重要的一条路。环化能够减少构象自由度,提高稳定性,也常常有助于改善膜通透性。综述中特别提到,2023 年获批的 Rezafungin、Motixafortide 和 Zilucoplan 都是 cyclic peptide drugs。这说明环肽已经不只是理论上有吸引力,而是正在成为临床可用的结构类型。
Conjugation 的意义更接近药代工程。脂肪酸修饰、PEGylation、白蛋白融合等策略,可以增加分子体积、改变疏水性、减少肾清除、延长循环时间。GLP-1 药物的长效化,很大程度上就依赖这些策略。Semaglutide 和 tirzepatide 不是天然 GLP-1 或 GIP 的简单复制品,而是被精心设计过的长效多肽分子。
这也是我觉得多肽药物最关键的一点:真正重要的不只是找到一个有效序列,而是找到一个能够承受工程化改造、并最终变成药物的序列。
GLP-1 药物真正展示的是多肽工程的成熟
GLP-1 相关药物在这篇综述里占了很大篇幅,但它们不是单纯作为销售案例出现,而是作为多肽工程成熟的代表。
Semaglutide 的设计就很典型。它通过关键位点替换增强对 DPP-4 降解的抵抗,又通过脂肪酸侧链延长体内作用时间。Tirzepatide 则进一步把多肽从单一 GLP-1 receptor agonist 推向 GIP / GLP-1 dual agonist。Retatrutide 这样的候选药物则继续向 GLP-1 / GIP / glucagon 三靶点方向探索。
这说明多肽药物在代谢疾病中的角色正在改变。它不再只是模拟一个天然肽类激素,而是被设计成多受体、多通路的代谢调节器。多肽的序列可调性、修饰空间和药代工程能力,使它特别适合做这类复杂生理网络的调节分子。
下图展示了 2023 年销售额排名前五的 GLP-1 相关药物及其组成和结构特征。这个图很值得放在正文里,因为它能直观体现一点:这些药物不是天然序列的简单复制,而是经过氨基酸替换、脂肪酸修饰、融合结构等策略优化后的药物分子。
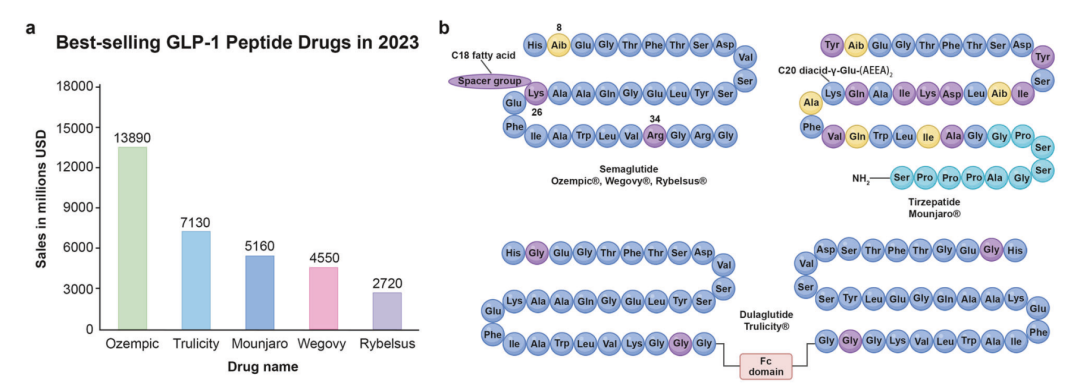
销售额排名前五的 GLP-1 激动剂及其结构特征。上图左侧展示 Ozempic、Trulicity、Mounjaro、Wegovy、Rybelsus 的销售情况;右侧展示这些 GLP-1 / incretin 药物的氨基酸组成、连接顺序和特征结构。
销售额排名前五的 GLP-1 激动剂及其结构特征。上图左侧展示 Ozempic、Trulicity、Mounjaro、Wegovy、Rybelsus 的销售情况;右侧展示这些 GLP-1 / incretin 药物的氨基酸组成、连接顺序和特征结构。
不过,这里仍然不能把 GLP-1 叙事过度泛化。GLP-1 是多肽药物的强样本,但不是所有多肽药物都能复制它的商业路径。很多多肽药物面对的是更小的适应症、更复杂的递送难题,或者更难验证的机制。因此,GLP-1 的真正启发不是多肽都能成为爆款,而是多肽在合适的生物学问题上,可以通过结构工程被推到非常高的药物成熟度。
PDC 让多肽从药物本体变成递送逻辑
Peptide-drug conjugates,也就是 PDC,是这篇综述里另一个非常值得关注的方向。
PDC 的基本结构并不复杂:一个 cell-targeting peptide,一个 linker,再加一个 payload。它和 ADC 的逻辑相似,都是通过靶向模块把有效载荷送到更合适的位置。但 PDC 用短肽替代抗体,因此分子量更小,化学修饰更灵活,理论上也可能获得更好的肿瘤渗透。
这类设计的核心,不在于多肽本身是否杀伤细胞,而在于多肽能不能承担导航头的角色。对于很多高毒性 payload,比如 MMAE、DM1、doxorubicin、paclitaxel、radionuclides,直接给药的治疗窗往往有限。PDC 试图通过靶向肽把 payload 带到肿瘤组织或特定受体高表达细胞,从而扩大治疗窗。
下表列出了临床阶段的 PDC 药物,包括 ANG1005、BT1718、BT5528、BT8009、NGR015、Zoptarelin doxorubicin、AEZS-108 等。它们的差异不仅在 payload,也在 cell-targeting peptide、linker、适应症和临床阶段。
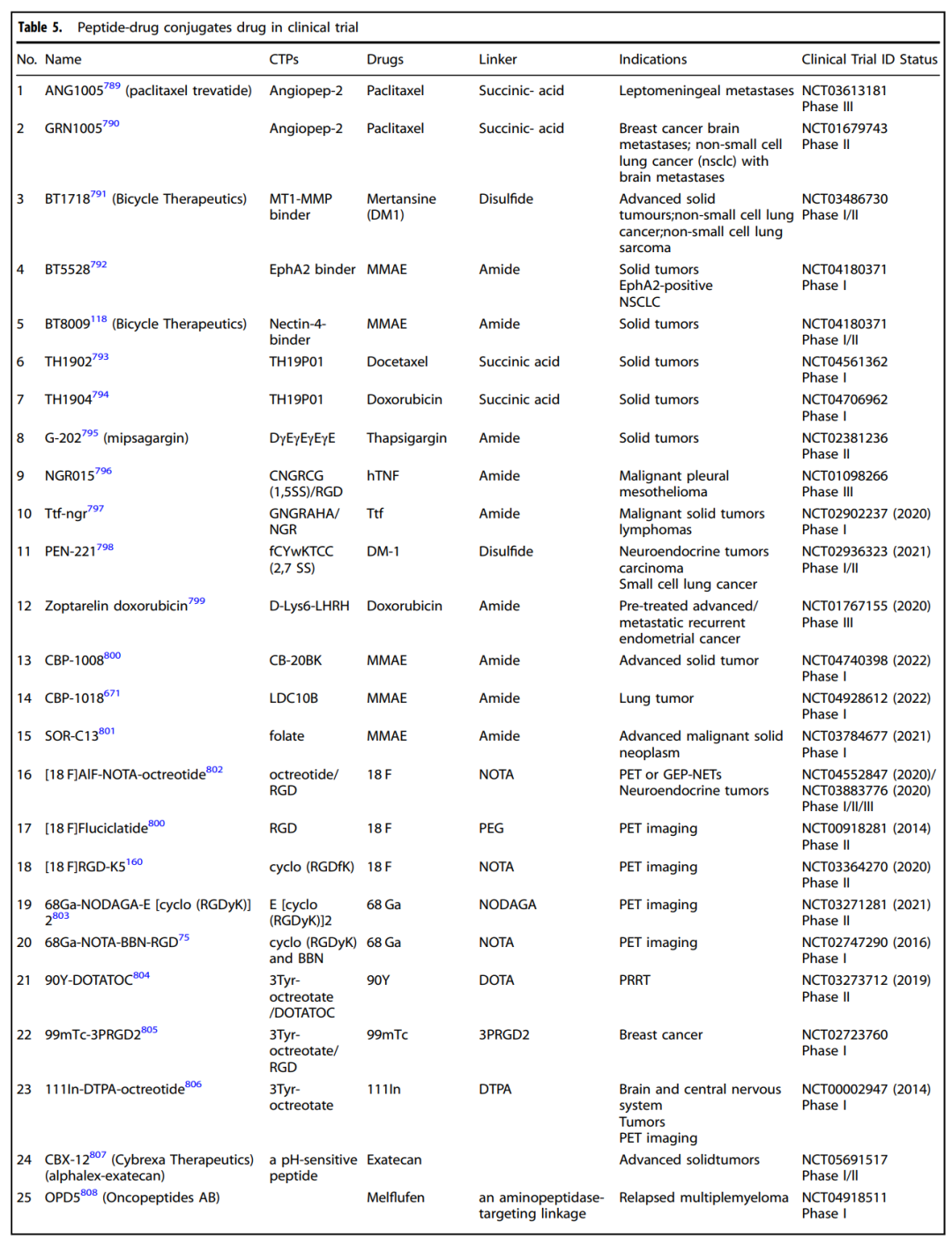
临床阶段的 peptide-drug conjugates。上表列出了 ANG1005、BT1718、BT5528、BT8009、NGR015、Zoptarelin doxorubicin、AEZS-108 等 PDC 药物,并标注了 cell-targeting peptide、payload、linker、适应症、临床试验编号和临床阶段。
临床阶段的 peptide-drug conjugates。上表列出了 ANG1005、BT1718、BT5528、BT8009、NGR015、Zoptarelin doxorubicin、AEZS-108 等 PDC 药物,并标注了 cell-targeting peptide、payload、linker、适应症、临床试验编号和临床阶段。
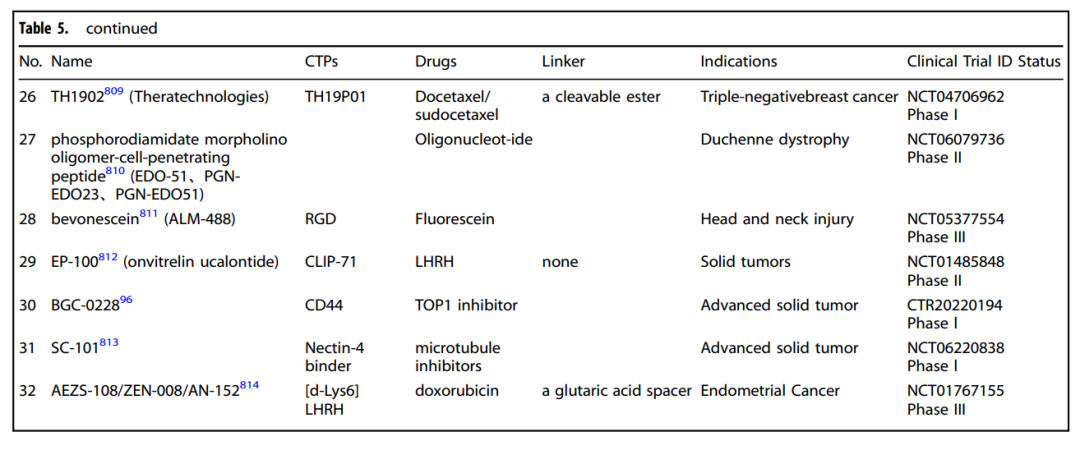
临床阶段的 peptide-drug conjugates。上表列出了 ANG1005、BT1718、BT5528、BT8009、NGR015、Zoptarelin doxorubicin、AEZS-108 等 PDC 药物,并标注了 cell-targeting peptide、payload、linker、适应症、临床试验编号和临床阶段。
临床阶段的 peptide-drug conjugates。上表列出了 ANG1005、BT1718、BT5528、BT8009、NGR015、Zoptarelin doxorubicin、AEZS-108 等 PDC 药物,并标注了 cell-targeting peptide、payload、linker、适应症、临床试验编号和临床阶段。
这里需要注意一点:PDC 不是 ADC 的简单替代品。它更小、更灵活,但也可能更快清除,体内稳定性和靶向效率未必总是优于 ADC。PDC 更像是给靶向递送增加了一条新的设计路线。它适合哪些 payload、哪些靶点、哪些肿瘤类型,还需要通过更多临床数据来判断。
我觉得 PDC 最有意思的地方,是它改变了多肽在药物中的角色。多肽不再只是一个活性治疗分子,也可以是定位模块、成像探针、payload 载体,甚至是诊疗一体化系统中的一部分。这个变化让多肽药物从分子本体扩展到了递送逻辑。
递送不是进细胞这么简单,而是一整条路径
多肽递送里有两个概念需要区分:cell-penetrating peptides 和 targeting peptides。
CPP 解决的是怎么进入细胞。Targeting peptide 解决的是去哪里。前者关注穿膜和内吞,后者关注组织、细胞或受体特异性。一个好的多肽递送系统,往往需要同时考虑这两件事。
下图把 peptide-based delivery system 的逻辑画得比较直观:一类多肽帮助 cargo 进入细胞,另一类多肽识别疾病相关靶点或组织环境。Cargo 可以是 nanoparticles、nucleic acids、proteins,也可以是 chemotherapeutic compounds。
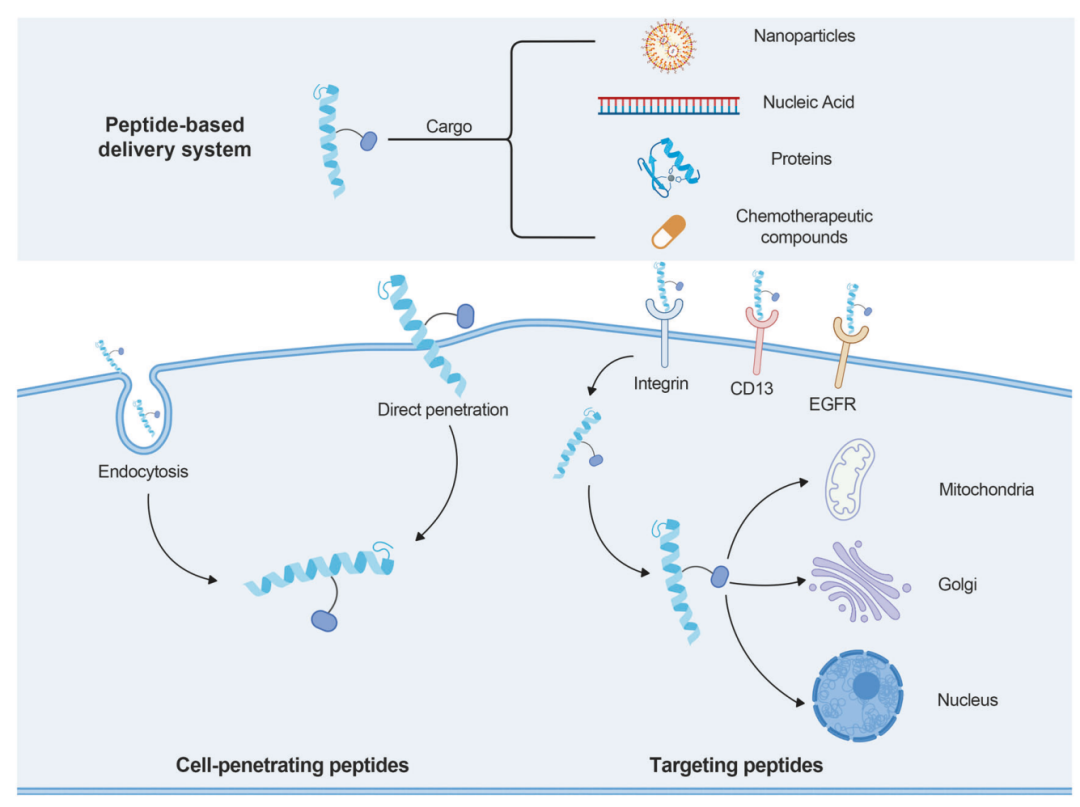
多肽递送系统中的 targeting peptide 与 cell-penetrating peptide。上图展示了 peptide-based delivery system 如何携带 nanoparticles、nucleic acids、proteins 和 chemotherapeutic compounds,并通过 integrin、CD13、EGFR 等靶点进入细胞,进一步递送到 mitochondria、Golgi、nucleus 等细胞器。
多肽递送系统中的 targeting peptide 与 cell-penetrating peptide。上图展示了 peptide-based delivery system 如何携带 nanoparticles、nucleic acids、proteins 和 chemotherapeutic compounds,并通过 integrin、CD13、EGFR 等靶点进入细胞,进一步递送到 mitochondria、Golgi、nucleus 等细胞器。
进一步看,CPP 的细胞摄取路径也并不简单。下图展示了 CPP 可以通过 clathrin-mediated endocytosis、caveolin-mediated endocytosis、macropinocytosis 等内吞路径进入细胞,也可能通过 pore formation、carpet-like model、inverted micelle model 等直接穿膜机制进入细胞。但进入细胞并不是终点。进入内吞体之后,cargo 还需要 endosomal escape;如果目标在细胞器里,还需要进一步定位到 mitochondria、lysosome、endoplasmic reticulum、Golgi 或 nucleus。
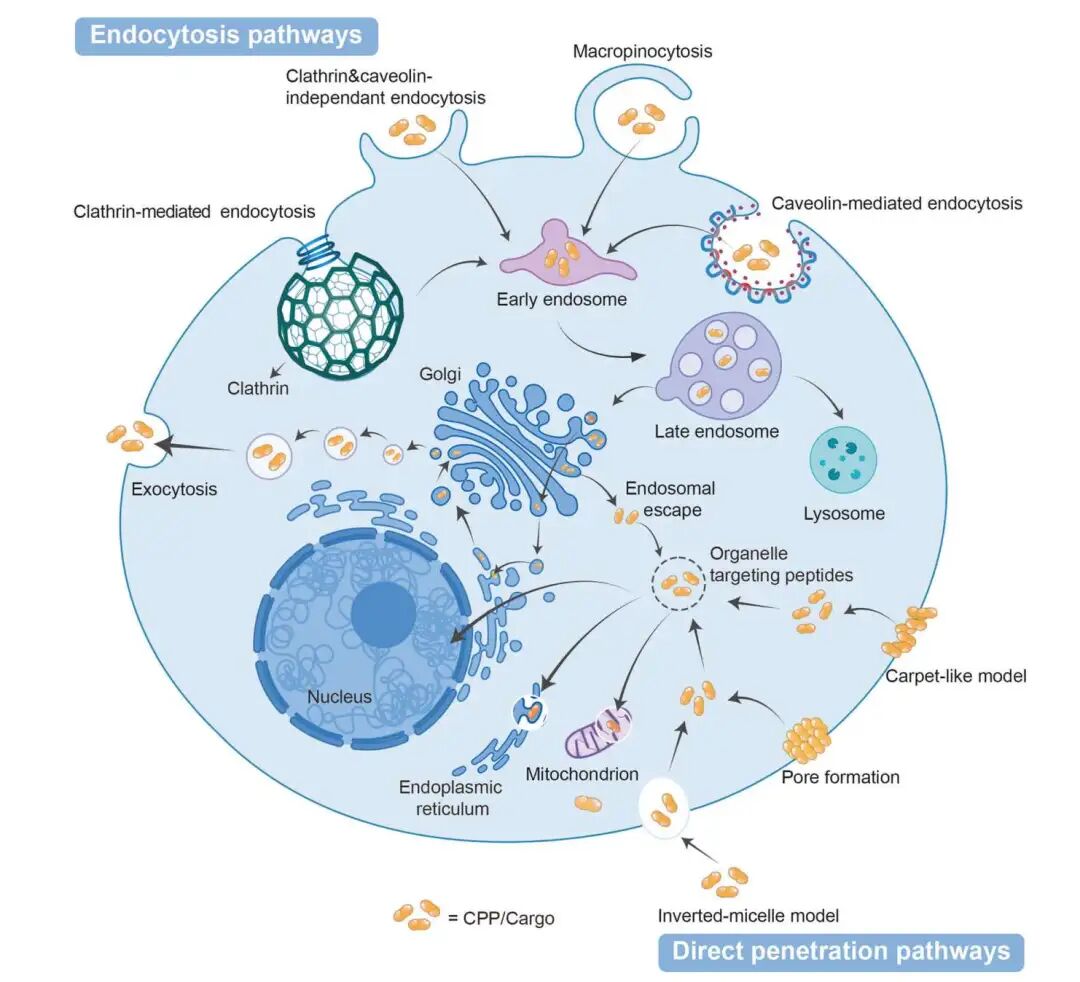
多肽递送策略的细胞摄取路径。上图展示了 CPP 进入细胞的两类主要机制:endocytosis pathways 和 direct penetration pathways。前者包括 clathrin-mediated endocytosis、caveolin-mediated endocytosis、macropinocytosis 等;后者包括 pore formation、carpet-like model、inverted micelle model 等。
多肽递送策略的细胞摄取路径。上图展示了 CPP 进入细胞的两类主要机制:endocytosis pathways 和 direct penetration pathways。前者包括 clathrin-mediated endocytosis、caveolin-mediated endocytosis、macropinocytosis 等;后者包括 pore formation、carpet-like model、inverted micelle model 等。
这也是递送问题真正困难的地方。很多时候,药物不是没进细胞,而是进去了却停在不该停的地方,或者在内吞体里被困住,最后无法释放到目标空间。
CPP 还有一个重要局限:它能增强跨膜,但不一定具备足够特异性。能让 cargo 更容易进入细胞,不等于能让 cargo 只进入病灶细胞。综述也提到,目前 FDA 尚未批准单独 CPP 或 CPP/drug combination,这在某种程度上反映了 CPP 平台从能递送到能精准递送之间仍有距离。
因此,未来多肽递送更可能是模块化组合:targeting peptide 负责定位,CPP 负责跨膜,endosomal escape motif 负责释放,organelle-targeting peptide 负责亚细胞定位。递送不是一个点,而是一条路径。
口服多肽是最有价值、也最不容易被简单解决的问题
多肽药物如果只能注射,在很多慢病和长期治疗场景中都会受到限制。口服多肽的吸引力非常明显:患者依从性更好,给药更方便,商业价值也更高。但口服多肽之所以难,是因为它面对的是一连串屏障,而不是单一吸收问题。
首先,多肽会在口腔、胃和小肠中遭遇酶和酸性环境。其次,它需要穿过覆盖在肠上皮表面的黏液层。之后,它还要跨越上皮细胞屏障和紧密连接。即使进入肠上皮细胞,也可能被代谢酶处理,或者被 P-glycoprotein 等转运系统外排。最终,还要面对首过效应。
下图把这些障碍分成 biochemical barriers 和 physical barriers。这个图很适合放在口服多肽小节,因为它能直观说明:口服多肽不是靠一个吸收促进剂就能彻底解决的问题,而是需要同时处理降解、黏液阻隔、上皮通透性、代谢和外排。
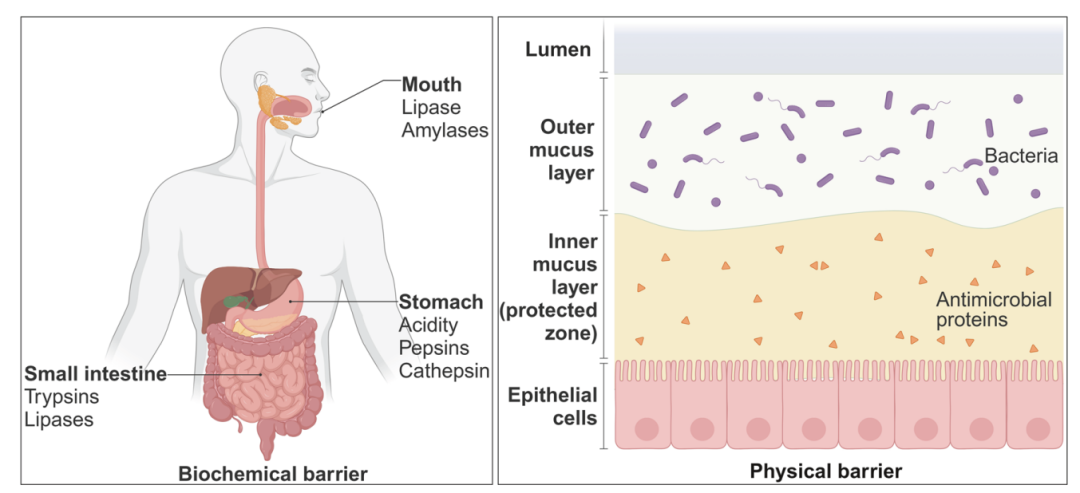
多肽药物口服吸收的主要屏障。该图展示了口服多肽面临的 biochemical barriers 和 physical barriers。左侧标出口腔、胃和小肠中的 lipases、amylases、pepsin、trypsins 等酶和酸性环境;右侧展示肠道黏液层和上皮细胞屏障。
多肽药物口服吸收的主要屏障。该图展示了口服多肽面临的 biochemical barriers 和 physical barriers。左侧标出口腔、胃和小肠中的 lipases、amylases、pepsin、trypsins 等酶和酸性环境;右侧展示肠道黏液层和上皮细胞屏障。
下面的表格列出了已获批口服多肽药物及其递送策略,包括 cyclosporine A、desmopressin acetate、voclosporin、octreotide 和 semaglutide。Rybelsus 的成功尤其值得注意,因为它证明 GLP-1 receptor agonist 也可以通过 SNAC 这样的 absorption enhancer 实现口服给药。
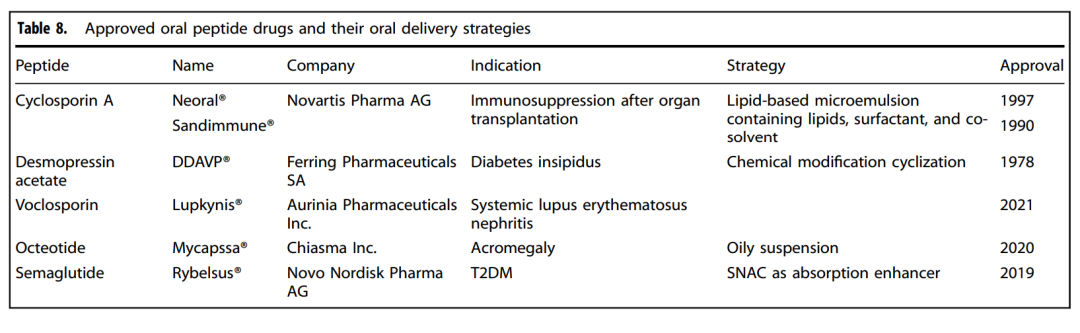
已获批口服多肽药物及其口服递送策略
已获批口服多肽药物及其口服递送策略
但 Rybelsus 的成功不能被解读为口服多肽时代已经全面到来。它更像是一个关键 proof-of-concept:在合适分子、合适制剂、合适剂量和合适适应症下,口服多肽可以成立。对于更广泛的多肽药物,口服递送仍然是一个需要药物化学、材料、制剂、生理屏障和工程技术共同解决的问题。
多肽疫苗的逻辑很清晰,但临床转化并不轻松
多肽疫苗看起来是一类很干净的疫苗形式。它使用明确的抗原表位,结构可控,合成相对容易,质量控制也比复杂生物制品更清楚。相比全病原体疫苗或复杂细胞疫苗,多肽疫苗理论上可以避免一些不必要的抗原成分,也更容易做个体化设计。
但它的问题也正来自这种简洁。单个 peptide epitope 的免疫原性往往不够强,HLA 限制会影响适用人群,肿瘤抗原异质性会导致免疫逃逸,抗原选择、佐剂和递送系统都会影响最终免疫反应强度。
下图展示了多肽疫苗的设计过程和免疫反应机制:从 biopsy、sequencing、in vitro peptide testing、in vivo peptide testing 到 manufacturing,再到 APC 摄取、MHC I 或 MHC II 通路呈递,最终激活 CD8+ T cell、CD4+ T cell、B cell 和 memory cell。这个图很好地呈现了多肽疫苗从设计到免疫激活的完整路径。
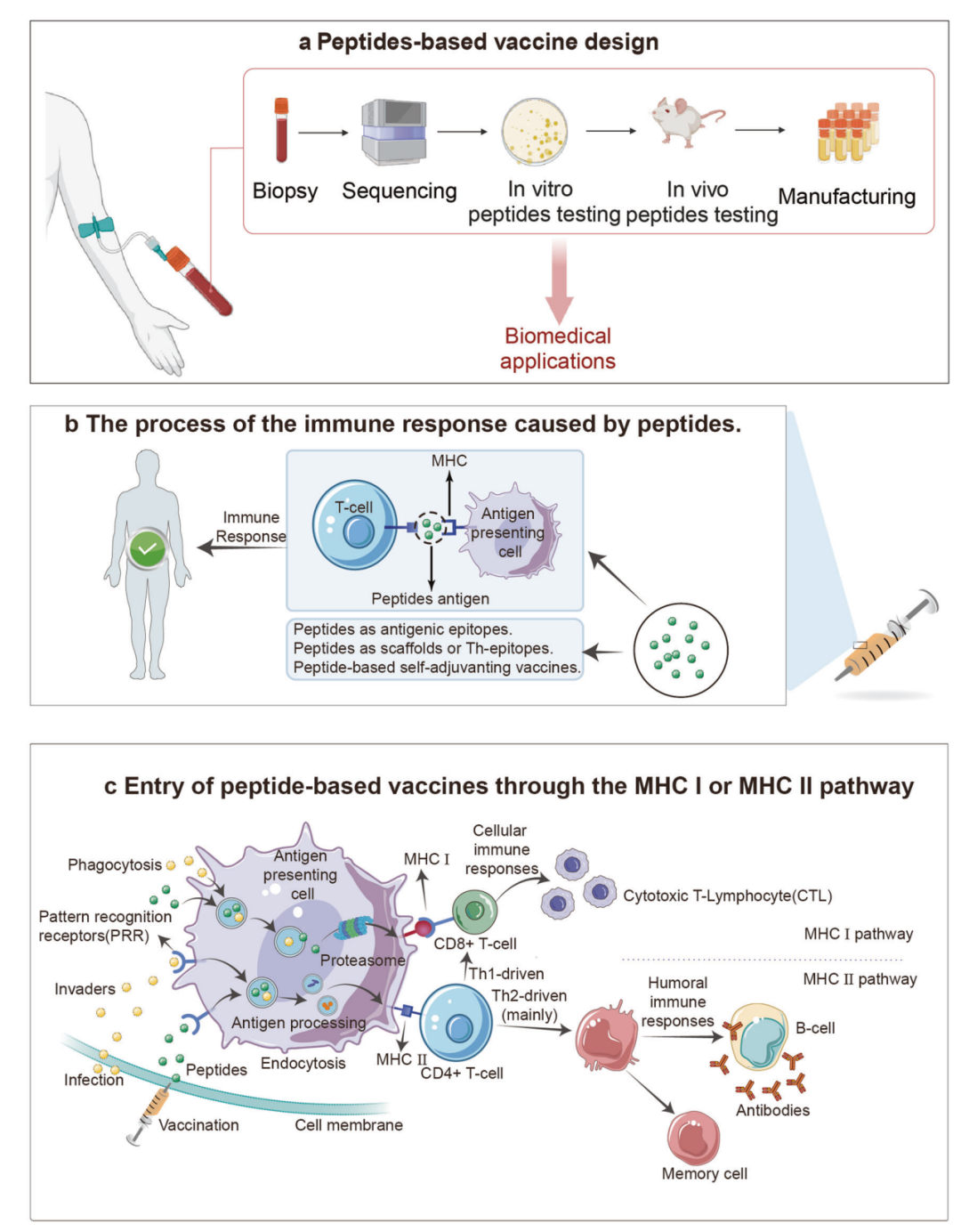
多肽疫苗的设计流程与免疫应答机制。
多肽疫苗的设计流程与免疫应答机制。
综述中也明确提到,目前 peptide-based vaccines 尚未获批上市,但已有多种候选物进入 III 期临床,其中肿瘤是核心方向之一。下表列出了 III 期临床阶段的多肽疫苗,包括 NeuroVax、galinpepimut-S、IO-102/IO-103、GLSI-100、nelipepimut-S 等。
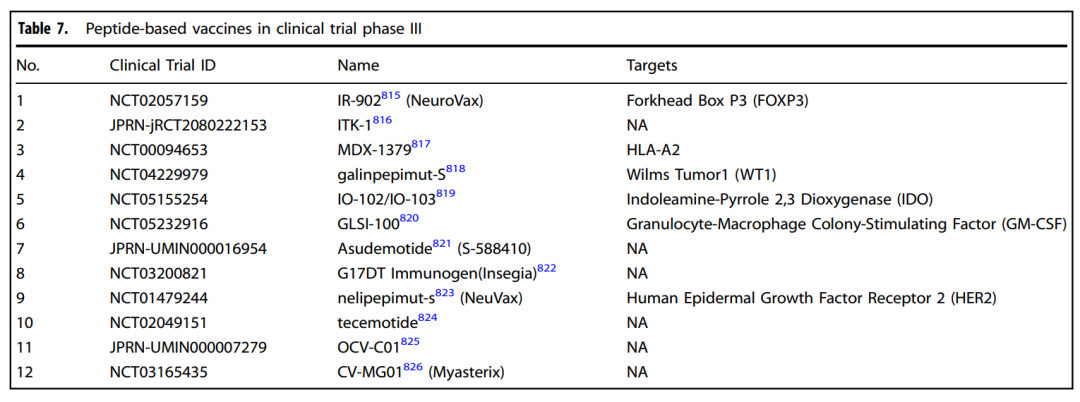
III 期临床阶段的多肽疫苗。
III 期临床阶段的多肽疫苗。
我觉得多肽疫苗真正有潜力的地方,是它和肿瘤 neoantigen 的结合。肿瘤测序可以找到个体化突变,算法可以预测 HLA 结合表位,多肽合成可以快速制备候选疫苗,再与免疫检查点抑制剂或其他治疗联合。这条路线还很难,但它把多肽的可定制性发挥到了最直接的地方。
AI 和展示库正在改变多肽发现的入口
多肽发现过去很大程度上依赖筛选。天然来源、毒液、微生物、噬菌体展示库、mRNA display、yeast display、bacterial display、mammalian display、cell-free display,这些技术本质上都是在巨大序列空间里寻找能结合目标或具备特定功能的短肽。
展示库技术的重要性在于,它把 peptide phenotype 和 DNA / RNA genotype 连接起来。一个多肽能不能结合目标,可以通过筛选得到;它的序列又可以通过对应遗传编码读回来。这样,随机序列空间不再是完全不可探索的黑箱。
但展示库也有自己的局限。Phage display 受宿主系统和库容量影响;yeast 和 mammalian display 更接近真核表达环境,但通量和成本更复杂;cell-free display 容量更大,也更容易引入非天然氨基酸,但库构建和稳定性仍有挑战。
AI 的加入,则把多肽发现从筛出来进一步推向设计出来。下图展示了 deep learning 在 peptide drug design 中的基本流程:模型可以使用 peptide sequence、SMILES、molecular weight、H-bond donor / acceptor、AlogP、activity type and value 等信息进行训练,然后用于 de novo peptide generation 或 target-based peptide design。
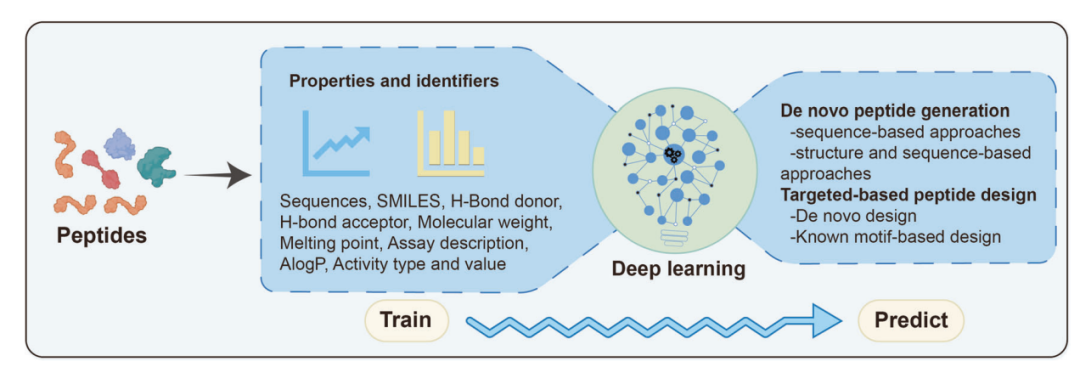
深度学习在多肽药物设计中的应用流程。上图展示了 peptide sequence、SMILES、molecular weight、H-bond donor / acceptor、AlogP、activity type and value 等输入特征如何进入 deep learning 模型,并用于 de novo peptide generation 和 target-based peptide design。
深度学习在多肽药物设计中的应用流程。上图展示了 peptide sequence、SMILES、molecular weight、H-bond donor / acceptor、AlogP、activity type and value 等输入特征如何进入 deep learning 模型,并用于 de novo peptide generation 和 target-based peptide design。
这里有两个方向值得关注。一个是 de novo peptide generation,也就是从已有多肽数据中学习序列模式,生成新的候选序列。另一个是 target-based peptide binder design,也就是围绕特定蛋白靶点或结合界面设计 peptide binder。后者已经开始和 AlphaFold、结构预测、inverse folding、motif-based design 等方向发生交叉。
但这里需要非常明确:AI 设计出一个binder,不等于发现了一个多肽药物。结合只是起点。后面还有稳定性、膜通透性、半衰期、毒性、免疫原性、制剂、递送和生产工艺。AI 更现实的价值,是帮助我们缩小候选空间,提出更好的初始序列,并和展示库、合成、修饰和实验验证形成闭环。
对 AIDD 的启发:多肽药物不是一个单点生成任务
从 AI 药物设计的角度看,这篇综述最有启发的一点,是它提醒我们多肽药物开发不是一个单点任务。
如果只把问题定义成生成一个 peptide sequence,就会漏掉真正困难的部分。一个多肽序列能结合靶点,只是第一步。它还需要稳定,需要有合适构象,需要能进入目标组织或细胞,需要有可接受的半衰期和暴露量,还要能被合成、纯化、储存和给药。
所以多肽药物特别适合 AI + 实验闭环,但这个闭环必须覆盖多个层级。AI 可以生成序列、预测结构、优化 binder、评估性质;展示库可以提供真实筛选数据;合成平台可以快速制备候选;结构修饰可以改善药代和稳定性;递送系统决定它能否到达目标位置;功能实验和动物模型再反过来校准模型判断。
这和小分子生成或蛋白设计都有相似之处,但多肽的特殊性在于它位于中间地带。它既有序列可设计性,又有小分子化学修饰空间;既要考虑生物功能,又要面对药代和递送障碍。因此,多肽药物不是一个单纯的生成问题,而是一个跨越序列、结构、修饰、递送和临床使用场景的系统设计问题。
这可能也是未来多肽药物最适合 AI 参与的地方。不是让 AI 一步生成最终药物,而是让 AI 在每一轮设计中更快地提出候选、更合理地筛掉不合适分子,并和实验结果形成迭代。
多肽不是万能 modality
这篇综述整体对多肽药物很乐观,但多肽不是万能 modality。
多肽不天然等于安全。虽然多肽降解产物通常是氨基酸,免疫原性相对较低,但具体药物仍可能出现毒性、免疫反应、脱靶效应或给药相关问题。
多肽也不天然等于可口服。绝大多数多肽仍然需要注射。Rybelsus 是重要案例,但它不能代表口服多肽已经普遍成熟。
PDC 也不天然优于 ADC。PDC 更小、更灵活,但也可能更快清除,payload 释放和靶向效率同样需要仔细设计。它是一条补充路线,而不是 ADC 的简单替代。
多肽疫苗的核心困难也不是合成,而是免疫。表位能合成出来,不代表能在人体内诱导足够强、足够持久、足够特异的免疫反应。
AI 设计多肽更不能被理解成 AI 直接发现药物。模型可以生成候选序列,但药物开发最终仍要回到稳定性、递送、毒性、制造和临床疗效这些现实问题。
所以,更稳妥的判断是:多肽药物正在变得越来越重要,但它不是为了替代小分子、抗体或核酸药物,而是在它们之间形成一个独立而有弹性的药物设计空间。
END:多肽药物正在进入平台化设计阶段
我会把这篇综述的主线理解成一句话:
多肽药物正在从天然活性序列的利用,走向工程化、多模块、可递送、可定制的平台化开发。
胰岛素证明了多肽可以成为药物。GLP-1 证明了多肽可以成为大适应症慢病药。PDC 证明了多肽可以成为靶向递送模块。CPP 和 targeting peptide 证明了多肽可以参与细胞进入和组织定位。多肽疫苗证明了多肽可以参与个体化免疫治疗。展示库和 AI 则改变了我们发现和设计多肽的方式。
当然,多肽药物还有很多问题没有解决。口服依然困难,递送依然复杂,稳定性和半衰期仍需要工程化,临床转化仍会被成本、制造、毒性和真实疗效反复检验。
但趋势已经很清楚:多肽不再只是小分子不够、抗体太大时的折中选择。它正在成为一个独立的药物设计空间。
未来真正有价值的多肽药物,可能不会只是一条活性序列,而会是一个经过精密设计的系统:有稳定骨架,有递送逻辑,有靶向模块,有可控释放,也可能有 AI 参与设计和实验反馈优化。
如果说过去多肽药物的关键词是天然活性,那么未来的关键词更可能是:
可设计、可递送、可组合。
这才是多肽药物真正值得继续关注的地方。
参考文献
Xiao, W., Jiang, W., Chen, Z. et al. Advance in peptide-based drug development: delivery platforms, therapeutics and vaccines. Sig Transduct Target Ther 10, 74 (2025). https://doi.org/10.1038/s41392-024-02107-5
推荐阅读
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-04-27,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读
目录

