Sci. Adv.|时毅团队开发AF3-TurboAb:让库规模抗体结构预测首次兼具速度与可靠性
Sci. Adv.|时毅团队开发AF3-TurboAb:让库规模抗体结构预测首次兼具速度与可靠性

DrugAI
发布于 2026-04-28 10:29:04
发布于 2026-04-28 10:29:04
DRUGONE
抗体药物已成为现代医学的重要支柱,但要真正看清一个抗体如何识别靶标,往往需要高分辨率复合物结构。长期以来,这一步主要依赖X射线晶体学和冷冻电镜,周期长、成本高、通量有限,难以支撑大规模抗体发现与表位导向设计。近日,纽约西奈山医学院时毅团队联合凯斯西储大学研究团队开发出AF3-TurboAb。该研究由桑哲、向宇菲为共同第一作者。AF3-TurboAb基于AlphaFold3优化而来,可在单张 GPU 上实现库规模抗体-抗原复合物的高通量结构预测。该平台不仅适用于纳米抗体,也适用于全长 IgG 抗体,显示出较好的通用性。更重要的是,这一平台不仅显著提速,还通过系统 benchmark 和实验验证,证明其预测结果具有很高可靠性。

为什么这项工作重要?
结构信息之所以关键,是因为它直接决定我们能否理解抗体识别的是哪个表位、如何结合、以及后续该如何进行理性工程优化。可惜的是,传统高分辨率结构方法往往需要数周甚至数月才能完成一个抗体-抗原复合物,远远跟不上真实抗体发现项目的节奏。即使是最先进的AI结构预测工具,过去也很难真正支撑“库规模”抗体筛选。
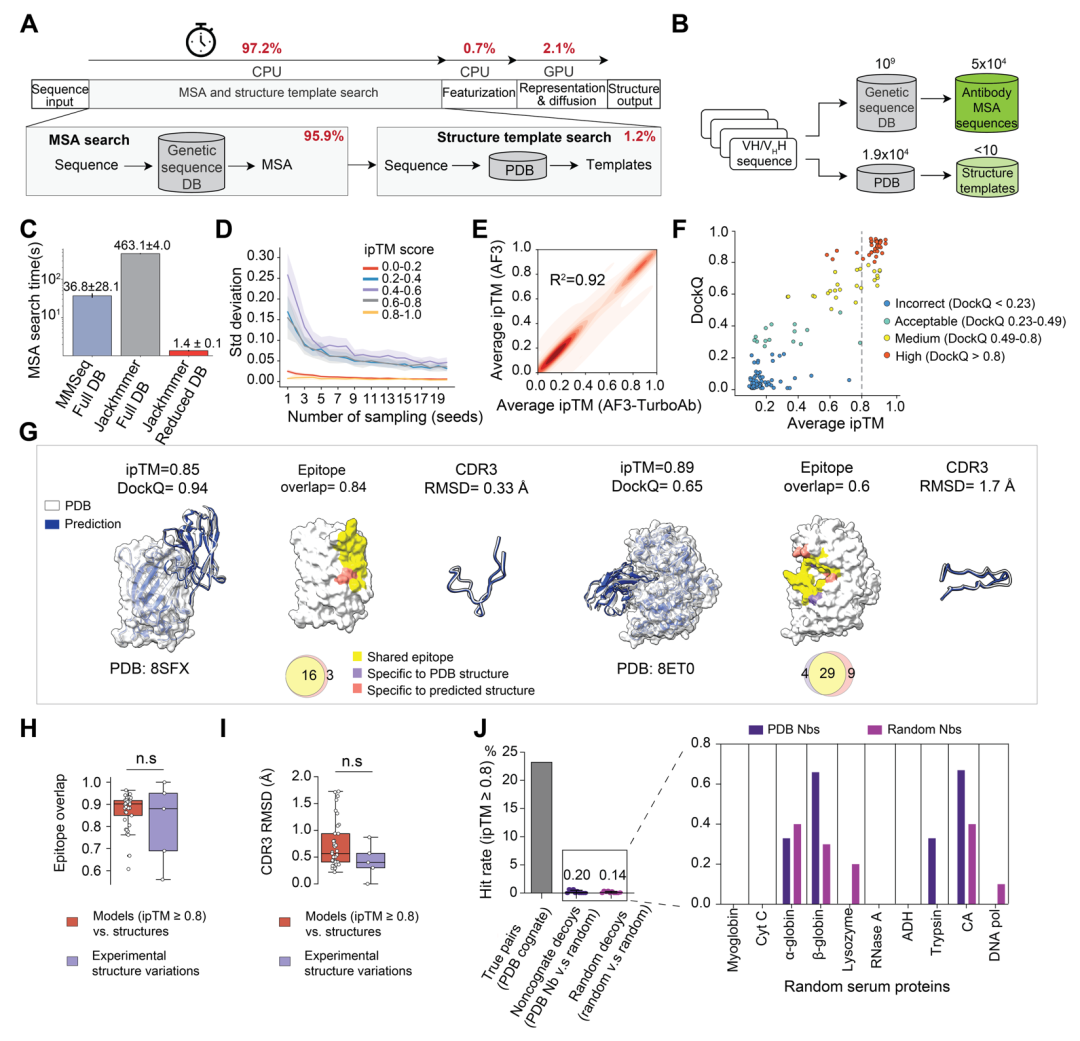
图1:AF3-TurboAb框架总览图图。
AF3-TurboAb突破了什么?
AF3-TurboAb 的核心突破,是让过去难以实现的库规模抗体结构解码成为现实。平台将端到端建模时间压缩至约 35 秒/seed,整体速度提升约 418 倍。按这一效率估算,在 40 张 GPU 上完成 100 万个纳米抗体建模约需 8.4 天,而标准流程则需要约 33.6 年。这意味着,过去只有极少数高资源平台才能完成的任务,如今学术实验室也有机会独立完成。
三个核心数字:418倍:数据库搜索速度显著提升,端到端建模压缩至约 35 秒/seed。275,371:应用于超过 27.5 万个免疫来源、抗原特异性纳米抗体进行预测。28,013:获得高置信度抗体-抗原复合物结构模型。
它不只是更快,更是“快且可靠”
这项工作真正重要的地方,不只是“更快”,而是快且可靠。团队不仅在约 1,000 个已发表结构基准上进行了系统 benchmark,还通过 12 个新解析的冷冻电镜纳米抗体-抗原结构进行了实验验证,显示 AF3-TurboAb 的高置信度预测可达到接近实验结构的准确度。除了在纳米抗体数据集上表现优异外,团队还在 744 个后训练 IgG-抗原复合物结构上观察到可比性能,说明 AF3-TurboAb 不仅适用于纳米抗体,也具备推广到 IgG 抗体的能力。
为了严格检验模型性能,研究团队基于预测结果预先挑选了 12 个识别不同表位的人血清白蛋白纳米抗体,并解析了全部 12 个复合物的冷冻电镜结构,分辨率为 3.1 到 3.8 Å。结果显示,所有表位均被正确识别,其中 10 个复合物与预测结果高度吻合,DockQ 为 0.59 到 0.91。即使面对超长 CDR3 环,模型依然表现稳定。
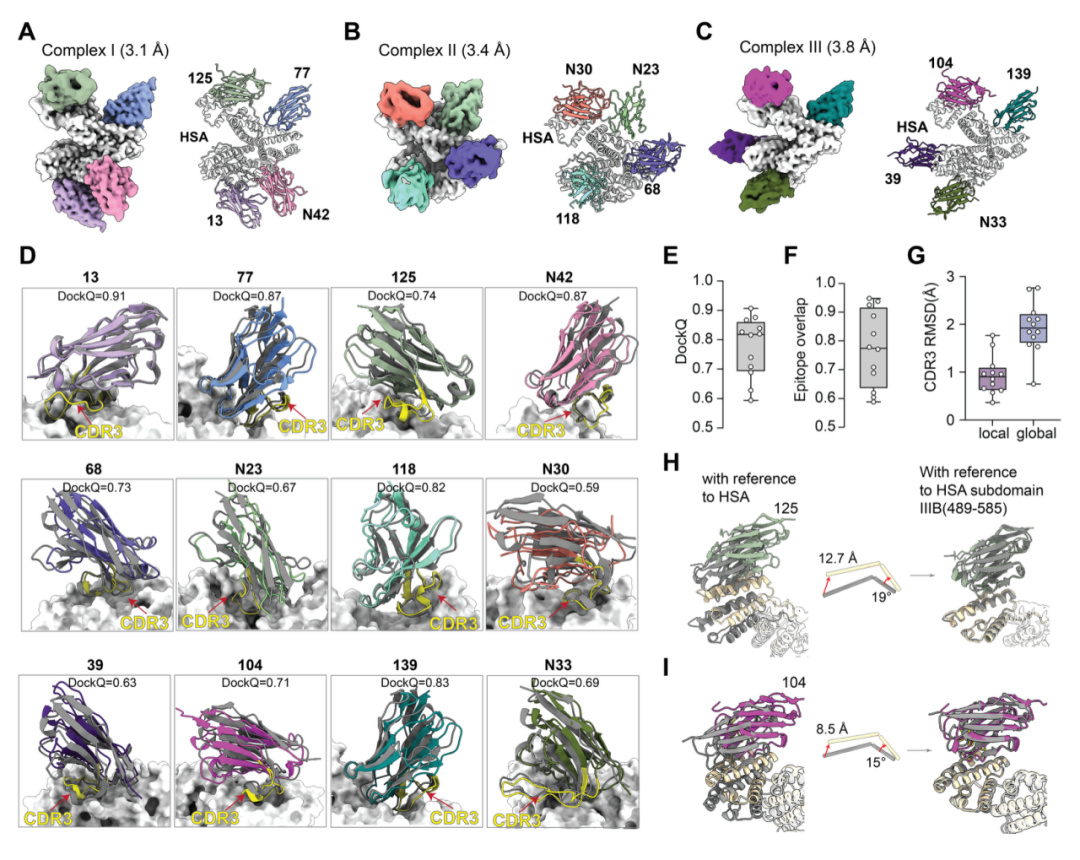
图2: 12个纳米抗体冷冻电镜结构与预测结构叠加图。
首张库规模表位图谱,揭示大量新表位
在确认平台可靠性后,团队将 AF3-TurboAb 应用于 275,371 个免疫来源纳米抗体,构建出大规模抗体识别图谱,最终获得 28,013 个高置信度复合物结构。这一图谱显著拓展了现有数据库中的已知表位空间,揭示出大量此前未被解析过的新表位。
研究还发现,尽管抗体序列高度多样,不同纳米抗体往往会收敛到相似的结合方式;同时,大多数抗体-抗原界面都包含少数“热点”残基,它们构成了稳定结合的核心支点。这些规律为今后的理性设计提供了新的结构依据。
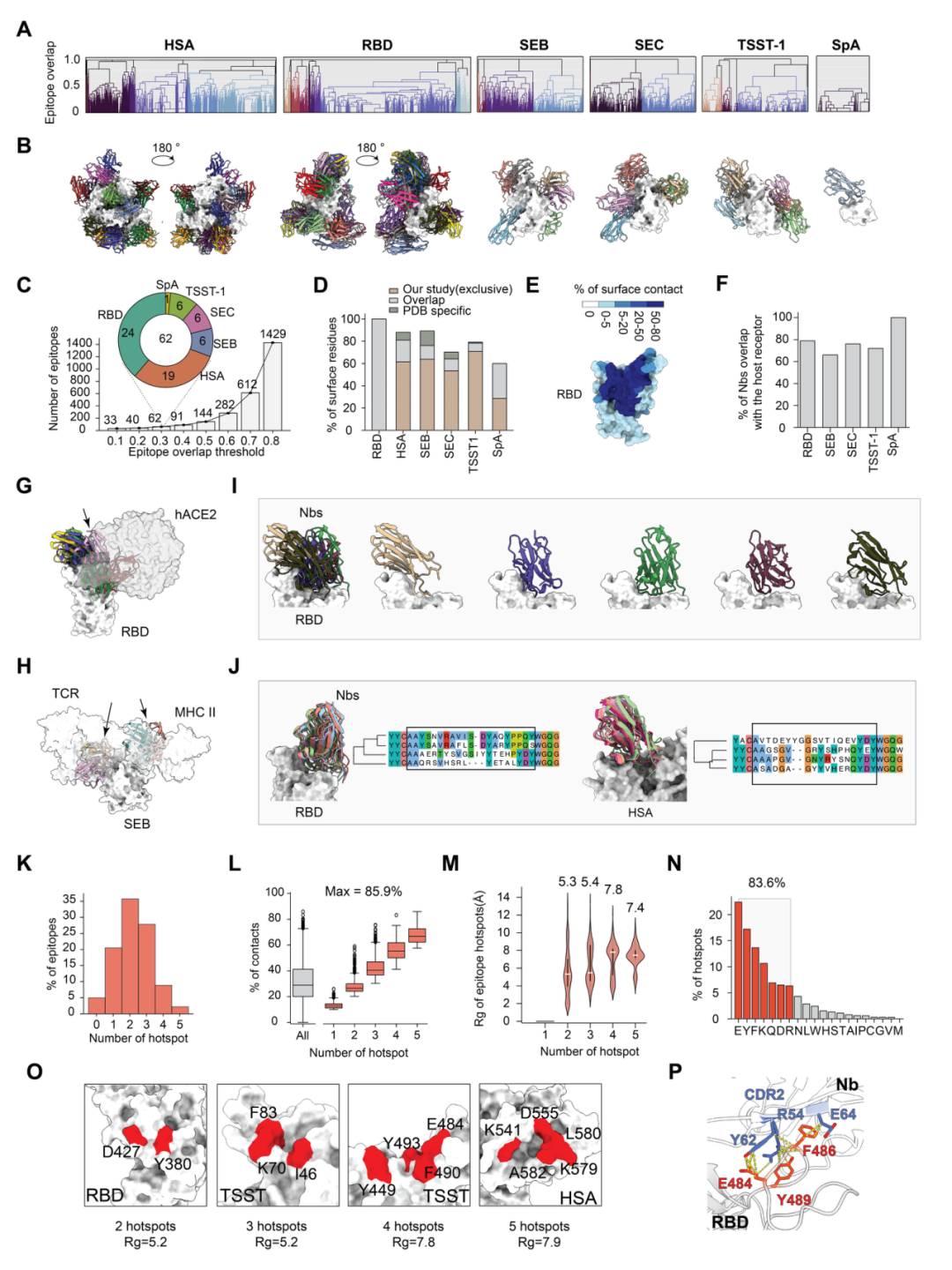
图3:六种抗原的表位多样性分析与热点架构图。
从结构图谱到真实治疗设计:三个应用场景
设计更不易被病毒逃逸的多表位中和剂
团队利用表位图谱理性组合多个互补表位,设计了三表位 SARS-CoV-2 中和构建体。构建后的 Trimer-Fc 在 Wuhan、BA.1、JN.1 等主要变异株中均保持强效中和,其中对 JN.1 的中和 EC50 相比单价对照最高改善超过 2,716 倍。这表明,库规模结构图谱可以直接指导更不易发生病毒逃逸的多表位抗体设计。
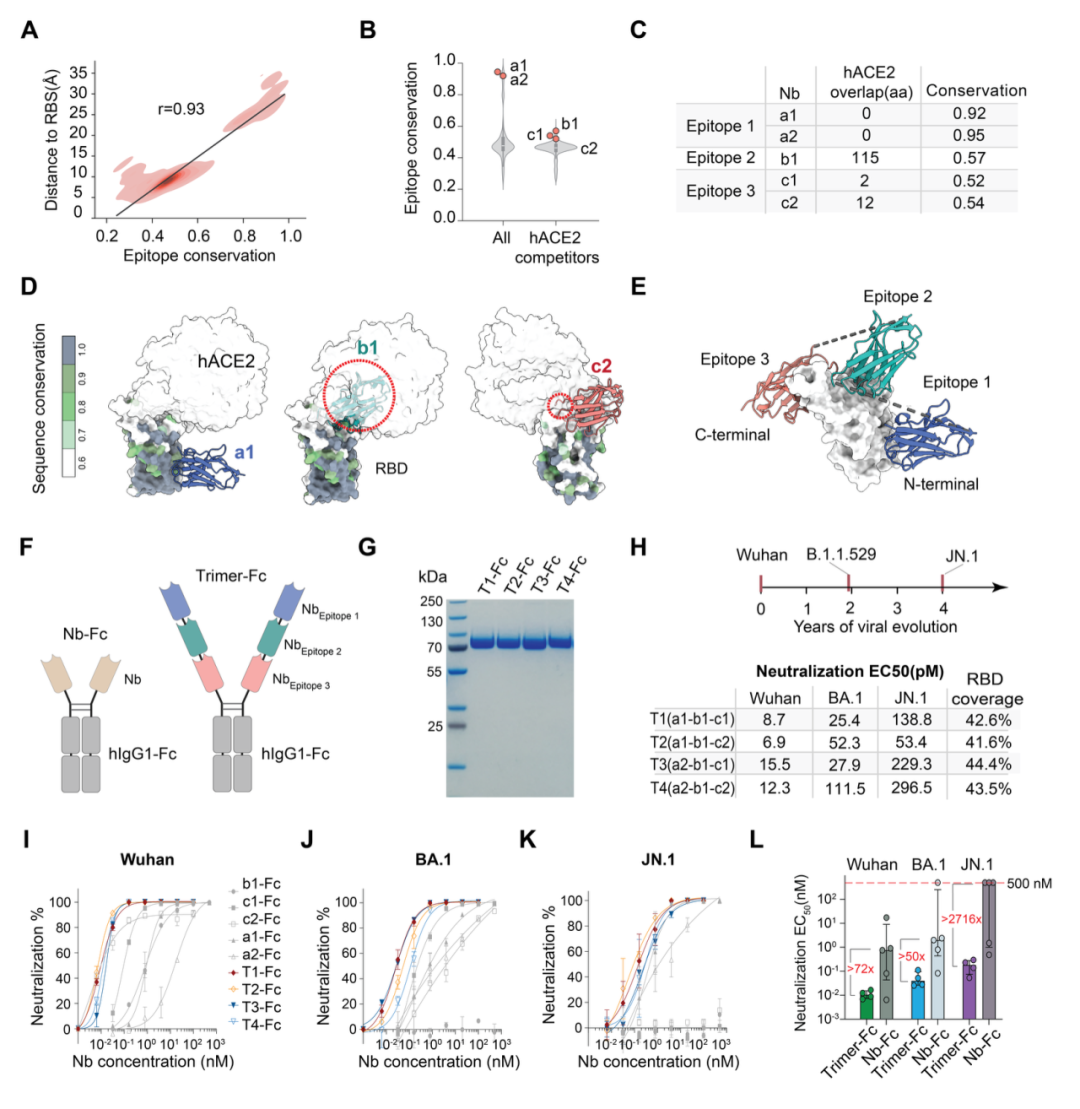
图4:三表位 SARS-CoV-2 中和剂设计与中和数据图。
发现肿瘤相关的糖基化特异性 PD-L1 结合剂
团队在 PD-L1 上识别出多个新表位,并发现纳米抗体 P10 可同时结合人和鼠 PD-L1,且对特定糖基化状态具有明显依赖性。去糖基化后,其结合能力下降超过 5 倍。这一结果提示,结构预测有望帮助发现更具肿瘤相关选择性的免疫检查点抗体。
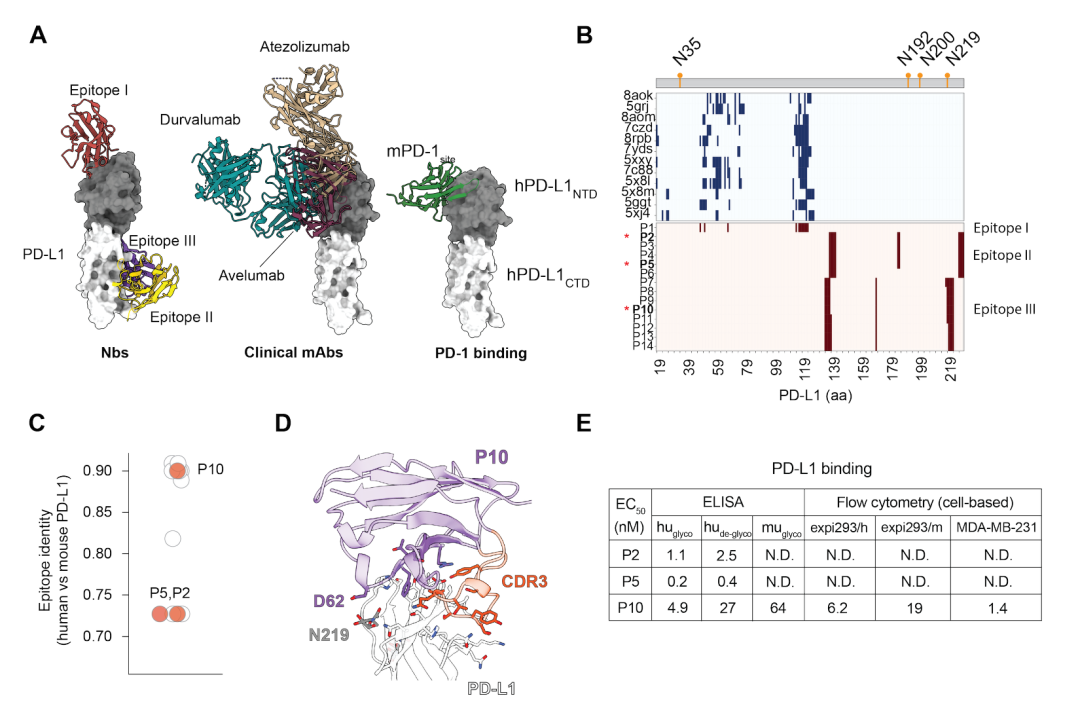
图5:PD-L1 多表位纳米抗体发现与 P10 结合特征图。
实现近实时 in silico 抗体筛选
在 MERS-CoV RBD 概念验证中,团队对 20,000 条候选纳米抗体序列完成端到端虚拟筛选,整个流程仅用时 9.5 小时。最终合成的候选中,5/19 展现出特异性 ELISA 结合活性,显示出 AF3-TurboAb 在公共卫生应急场景中的应用潜力。
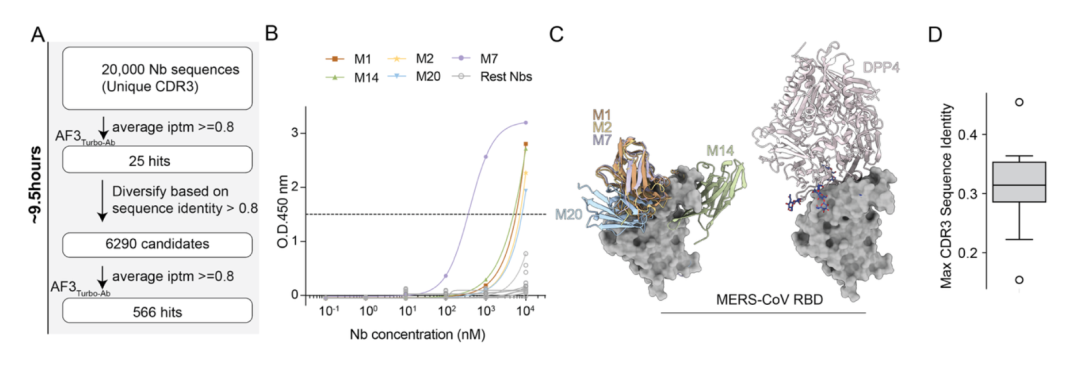
图6:MERS-CoV RBD 虚拟筛选流程图或结果图。
这项工作意味着什么?
AF3-TurboAb 将抗体结构预测从“少数案例、低通量”的模式,推进到“可大规模部署、并能直接支持设计决策”的新阶段。它不仅提升了速度,更通过系统 benchmark、实验验证和真实应用证明,高通量结构预测已经可以真正服务于复杂治疗分子的发现与优化。
未来,AF3-TurboAb 有望进一步拓展到全长 IgG 和 B 细胞受体 repertoire,并与更多机器学习和生物物理评价指标结合,用于纵向免疫监测、亲和力成熟分析以及更高质量的 in silico 抗体优化。随着相关数据和资源的开放,这一平台也有望成为下一代 AI 抗体设计的重要基础设施。
参考资料
Zhe Sang et al. ,Repertoire-scale antibody structural prediction informs therapeutic design.Sci. Adv.12,eaef7163(2026).
DOI:10.1126/sciadv.aef7163
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-04-25,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

