Sci. Adv.|强化学习引导的半柔性分子扩散模型用于基于结构的分子设计
Sci. Adv.|强化学习引导的半柔性分子扩散模型用于基于结构的分子设计

DrugOne
发布于 2026-04-23 18:46:39
发布于 2026-04-23 18:46:39
基于结构药物设计(Structure-Based Drug Design, SBDD)正在快速进入生成式人工智能时代。近年来,扩散模型、等变图神经网络等方法的发展,使研究者能够直接在蛋白口袋中设计三维候选分子,而不再局限于传统虚拟筛选对既有化学库的枚举搜索。然而,现有多数生成方法在训练过程中主要是基于静态蛋白-配体复合物数据学习分子结构与口袋环境之间的对应关系,将分子视作静态结构来建模。这样的方法虽然能够学习口袋约束下的空间分布,却难以进一步学习配体在真实结合过程中发生的局部构象调整与动态适配。如何让模型在生成过程中具备一定的优化能力,从而得到更合理、更高亲和力的分子,成为该方向的重要问题。
该研究提出了一种强化学习引导的半柔性分子扩散模型 SeFMol(Semi-Flexible Molecular Diffusion Model)。通过将扩散模型的去噪过程重新表述为马尔可夫决策过程,并利用强化学习在生成过程中隐式地动态调整分子构象,使配体能够以半柔性的方式更好地适应蛋白口袋。与此同时,SeFMol 还引入多种分子性质作为条件信号,并结合大规模无靶点分子预训练、蛋白-配体复合物微调以及快速采样策略,在提升结合能力的同时兼顾药物样性、化学合理性与采样效率。实验结果表明,SeFMol 在结合亲和力、成功率、性质控制、构象可靠性以及真实靶点泛化等方面优于现有方法,展示出较强的基于结构药物设计的潜力。该研究的相关数据和源代码均已经完全开源。
研究背景
当前基于蛋白质口袋的分子生成方法大多依赖静态复合物数据进行训练,重点学习的是在给定口袋环境下恢复或生成合理分子结构,而不是模拟配体在结合过程中的适配。同时,现有方法往往将优化重点放在对接分数上,却缺乏对药物性质的同步控制。模型可能生成对接分数较好的分子,但这些分子未必同时满足可合成性、药物样性以及若干关键理化性质要求。因此,目前基于结构分子分子生成面临两个紧密相关的问题:一是如何在生成过程中引入更接近真实结合过程的分子构象优化能力,二是如何在提高亲和力的同时将分子限制在更合理的药物化学空间内。
方法简介
受半柔性对接过程中配体会在结合位点内发生构象调整的启发,该研究提出了 SeFMol。整个框架可以概括为三个关键部分:两阶段刚性训练、强化学习驱动的半柔性优化,以及性质引导的快速采样。首先,在刚性训练阶段,先利用100 万个分子进行预训练,并引入8 种理化性质作为条件输入,使扩散模型学习在给定性质约束下恢复合理分子结构的能力。随后,该研究在10 万个蛋白-配体复合物上进一步微调,使模型学习蛋白口袋几何环境与分子结构之间的对应关系,从而获得靶点感知的三维分子生成能力。在此基础上,该研究进一步将扩散模型的逐步去噪过程建模为一个马尔可夫决策过程,将当前分子中间态对应状态,单步去噪对应动作,而最终生成分子依据其与蛋白口袋的结合表现获得奖励。通过这种方式,SeFMol 不再只是基于静态数据分布恢复分子,而是能够在生成过程中动态探索更合理的构象与相互作用模式,从而在一定程度上模拟配体在口袋中逐步适配的半柔性过程。此外,考虑到强化学习中的结合奖励只能在最终完整分子上计算,中间状态缺乏反馈,该研究引入了多性质条件作为持续引导信号,从而减少无效探索,缓解稀疏奖励问题。与此同时,该研究还提出了一种快速采样策略,将传统扩散模型的 1000 步采样压缩到 50 步,在保持分子质量的同时大幅提升训练和推理效率。
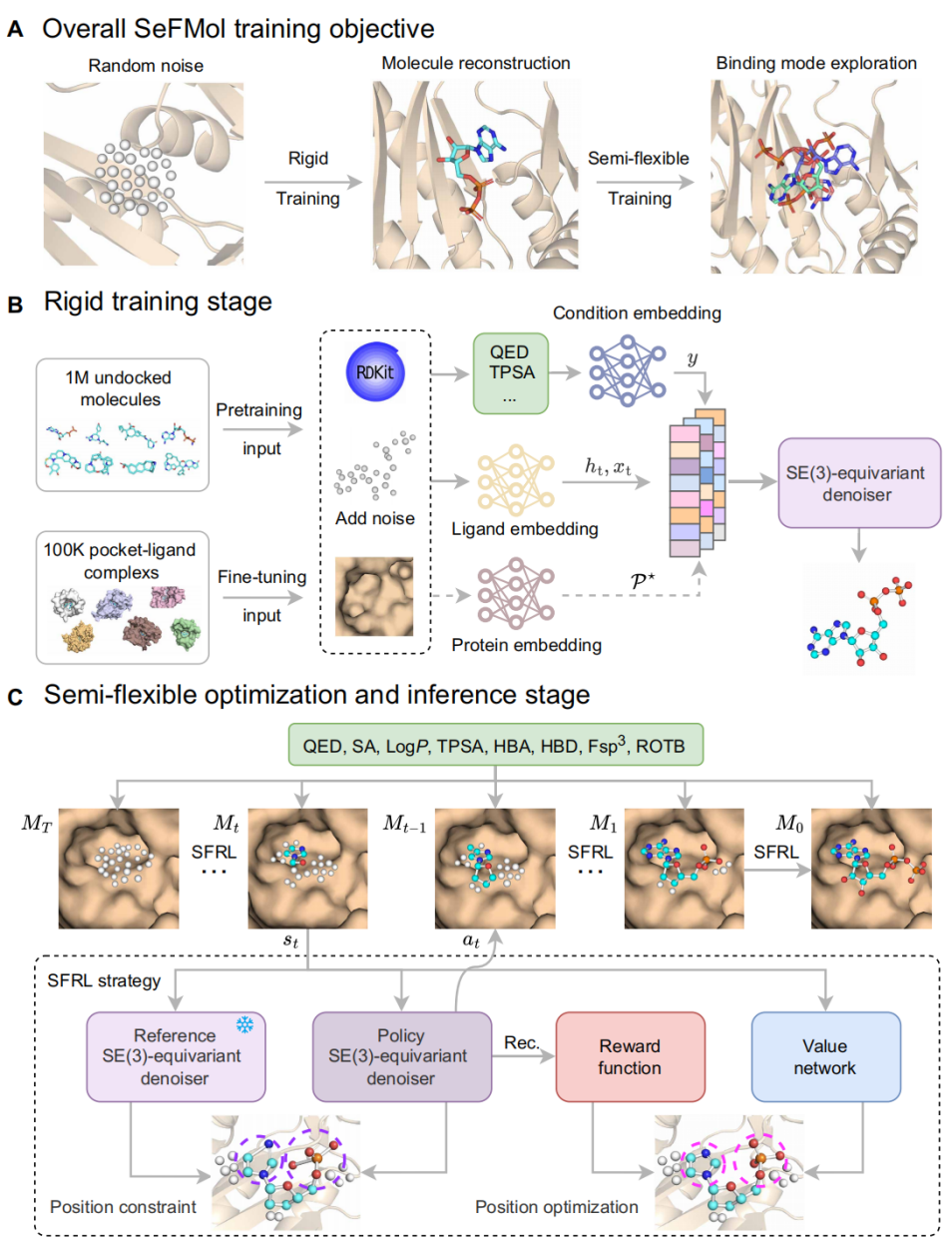
图1. SeFMol 的整体框架。
结果分析
SeFMol 在通用性质与结合性能评估中表现最优
该研究对 SeFMol 进行了系统评估,并与代表性方法进行比较。结果显示,SeFMol生成分子 的平均 Vina Score 达到 -7.23 kcal/mol,优于参考分子的 -6.36。这表明 SeFMol 不仅能够生成形式上合理的分子,还能够更稳定地产生与蛋白口袋具有更高预测结合能力的候选结构。除亲和力指标之外,SeFMol 在常规药物性质上也表现出较强优势。这说明 SeFMol 并不是单纯围绕对接打分进行优化,而是在结合能力、药物样性和分子合理性之间取得了更好的平衡。进一步分析还表明,SeFMol 生成分子的 Vina Score 与 Vina Dock 高度相关,提示其直接生成的构象已经较接近后续重对接后的合理结合状态。
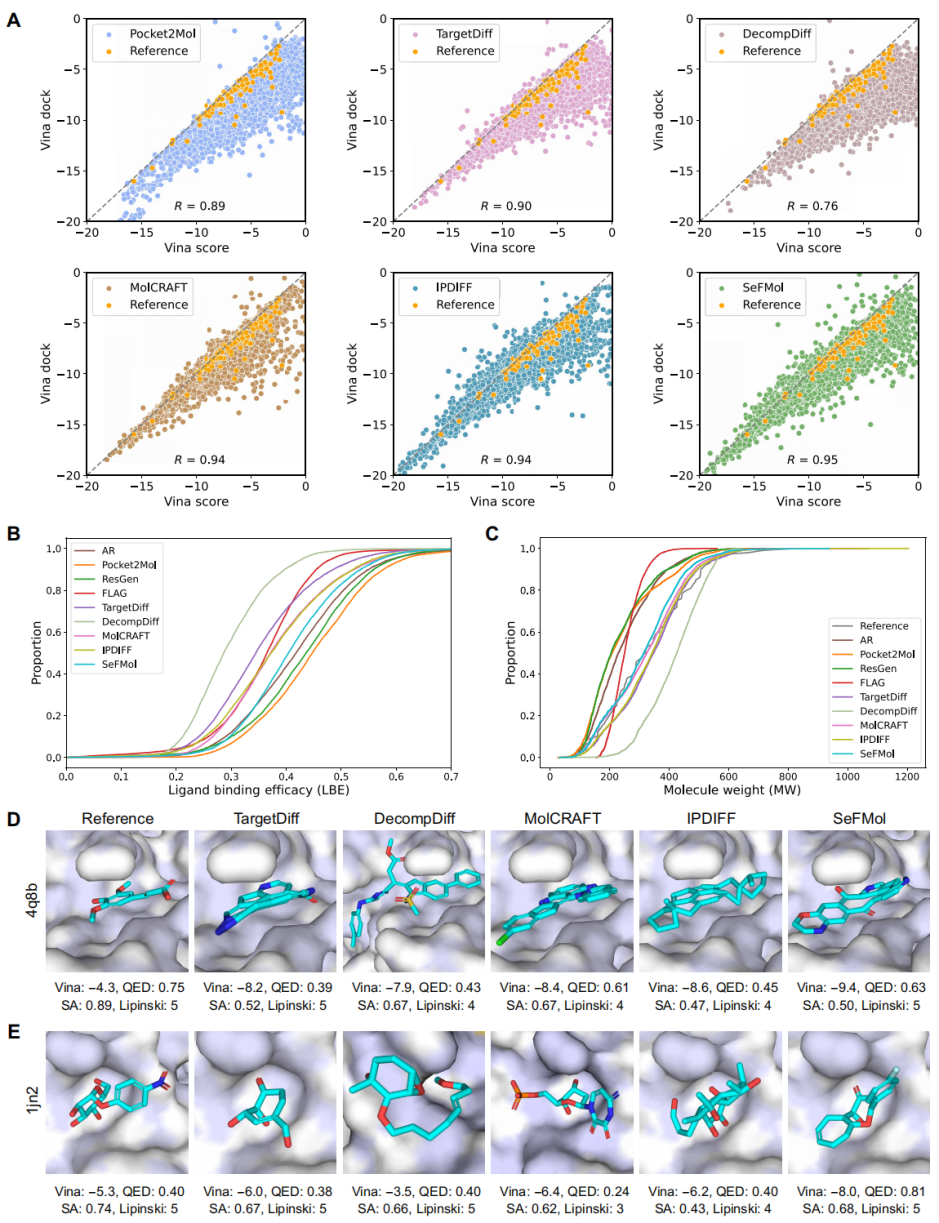
图2. SeFMol 与其他方法在结合性能与通用药物性质指标上的比较。
SeFMol 在采样效率与化学合理性上取得更好平衡
该研究进一步分析了 SeFMol 的采样效率以及生成分子的化学合理性。结果显示,SeFMol 的平均生成时间仅为 0.81 秒/分子,生成成功率达到 98.3%,明显优于多数扩散式基线方法。这一结果说明,该研究提出的快速采样策略有效缓解了传统扩散模型在 3D 分子生成中推理步数过多、速度偏慢的问题,使 SeFMol 在保持较高生成质量的同时,具备更强的实际应用可行性。为了更严格衡量分子的整体质量,该研究进一步引入了成功率指标,要求生成分子同时满足结合分数和多项理化性质约束。结果显示,SeFMol生成分子 的成功率达到 11.53%,高于对照方法,说明其更容易生成既能结合、又具备合理药物化学属性的高质量候选分子。该研究还进一步分析了性质分布,发现 SeFMol 生成分子的性质更集中地围绕目标值波动,而缺乏性质引导的基线方法则往往分布更为发散。
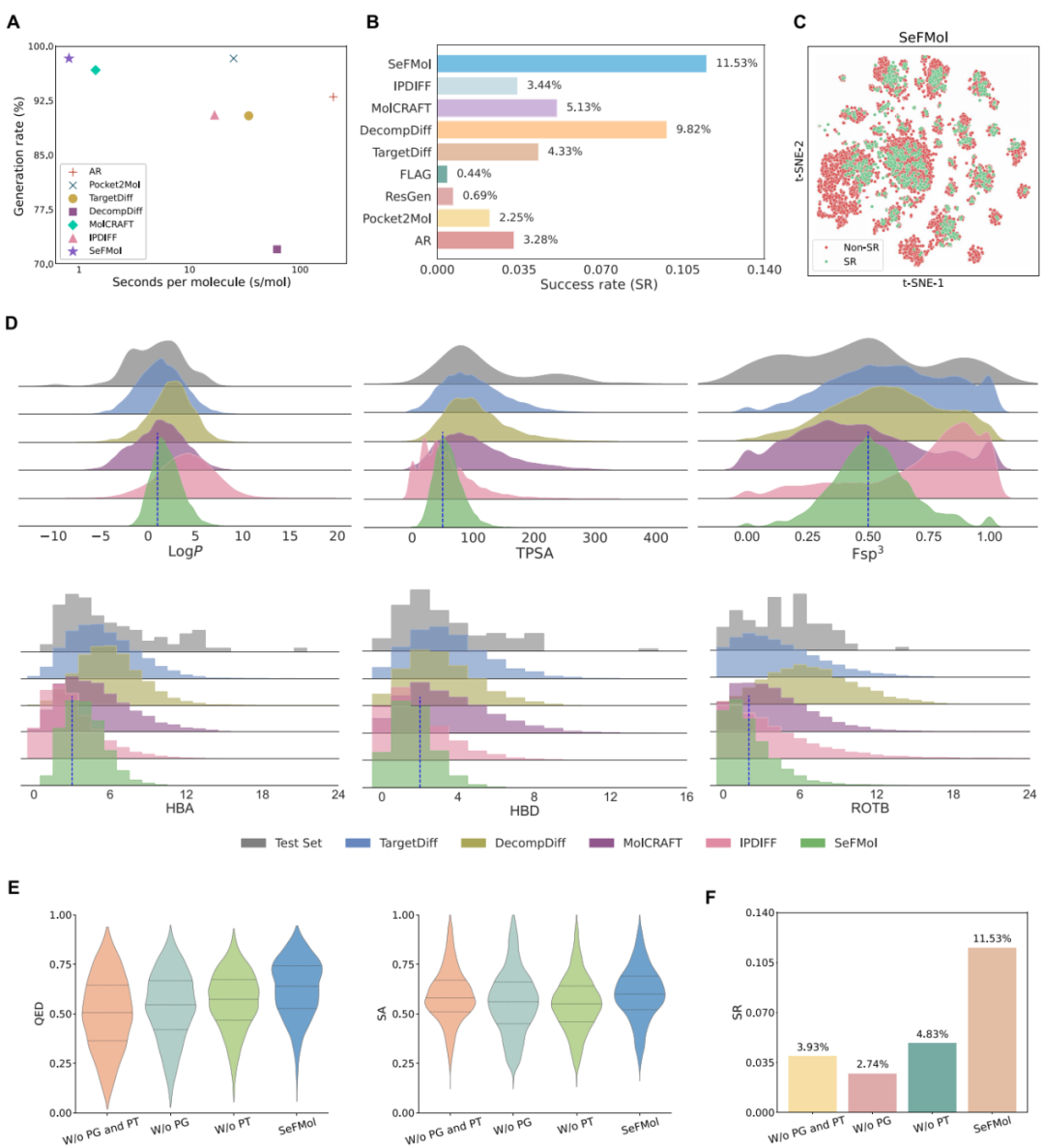
图3. SeFMol 在采样效率、成功率以及理化性质控制方面的表现。
SeFMol 生成的分子具有更高可靠性与更合理构象
除了结合分数和理化性质,该研究还系统评估了 SeFMol 生成分子的三维可靠性。通过比较生成分子与重对接构象之间的 RMSD,以及分析原子碰撞数、环结构分布、分子尺寸分布和相互作用模式,该研究发现 SeFMol 生成的分子在多个维度上都更接近参考分子。进一步的相互作用模式分析表明,SeFMol 在优化结合亲和力的同时,仍然能够较好保留与参考分子相似的微观作用类型分布,这意味着模型并非通过不合理的结构偏移来换取更低的打分,而是在更符合空间约束和相互作用规律的基础上提升结合表现。此外,在新颖性分析中,SeFMol 生成分子的结构分布与训练集也表现出明显差异,说明其并非简单复现已有化学空间,而具备一定的新颖结构探索能力。
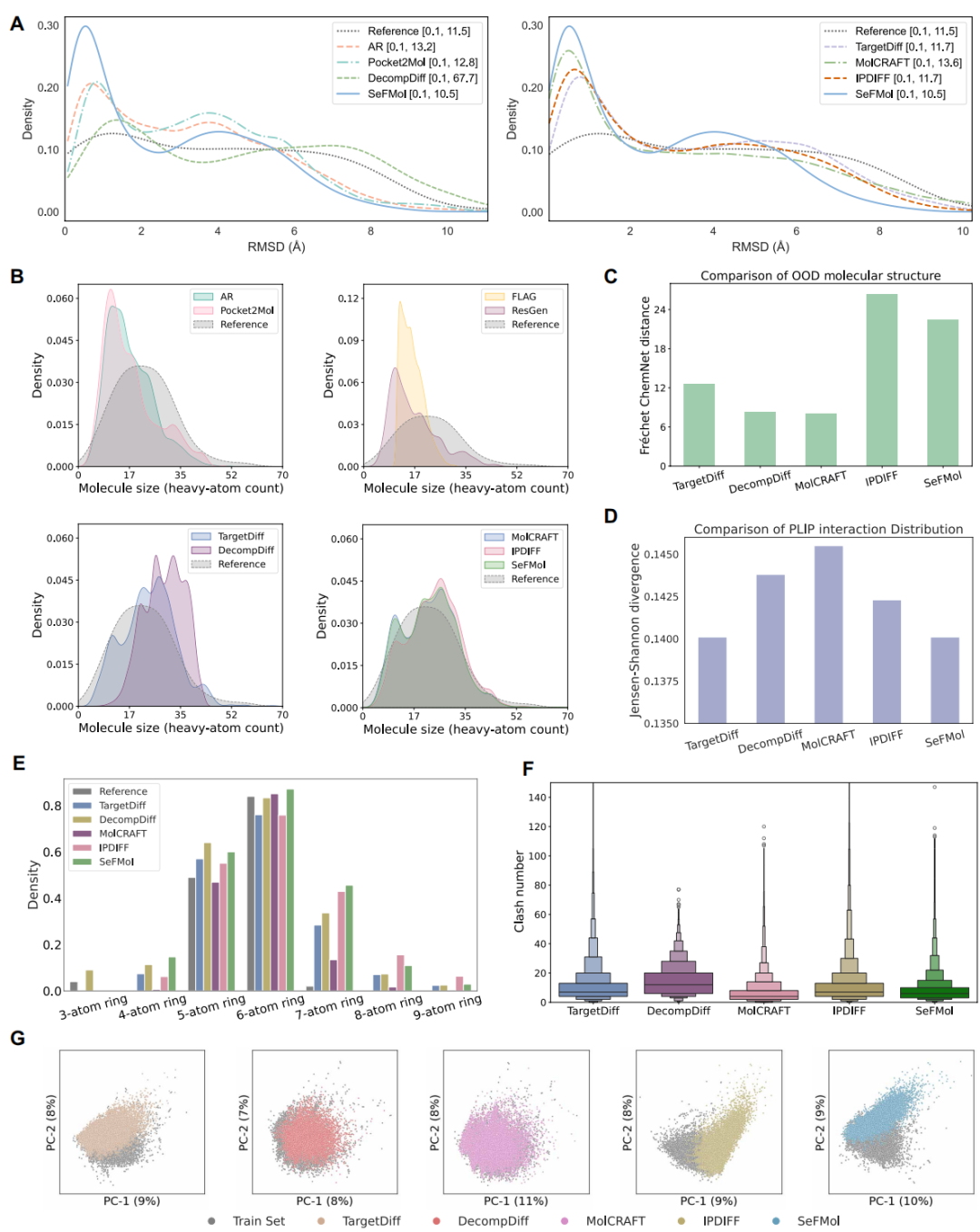
图4. SeFMol 在构象可靠性、相互作用模式合理与结构新颖性方面的表现。
SeFMol 可面向真实治疗靶点进行定制化分子生成
该研究进一步将 SeFMol 应用于两个真实治疗相关靶点:CDK2 和 ROCK1。结果显示,SeFMol 为这两个靶点生成的候选分子整体具有更优的表现,并且既能够复现已知活性分子的经典结合模式,也能够探索出新的合理相互作用。这表明 SeFMol 不仅适用于标准 benchmark 场景,也具备一定的真实靶点定制化设计能力。该研究还进一步测试了 SeFMol 的性质可控性,即在保持其他条件不变的情况下,指定不同的 TPSA 或 Fsp³ 目标值进行生成。结果表明,模型生成分子的性质分布依然能够围绕给定目标值变化,说明其在真实靶点条件下同样具备较好的响应能力。进一步地,该研究还将 SeFMol 应用于 AlphaFold 预测蛋白结构,发现模型同样能够生成具有较优结合表现的候选分子。这提示 SeFMol 并不局限于高质量晶体结构,也有望适用于更广泛的现实药物发现任务。
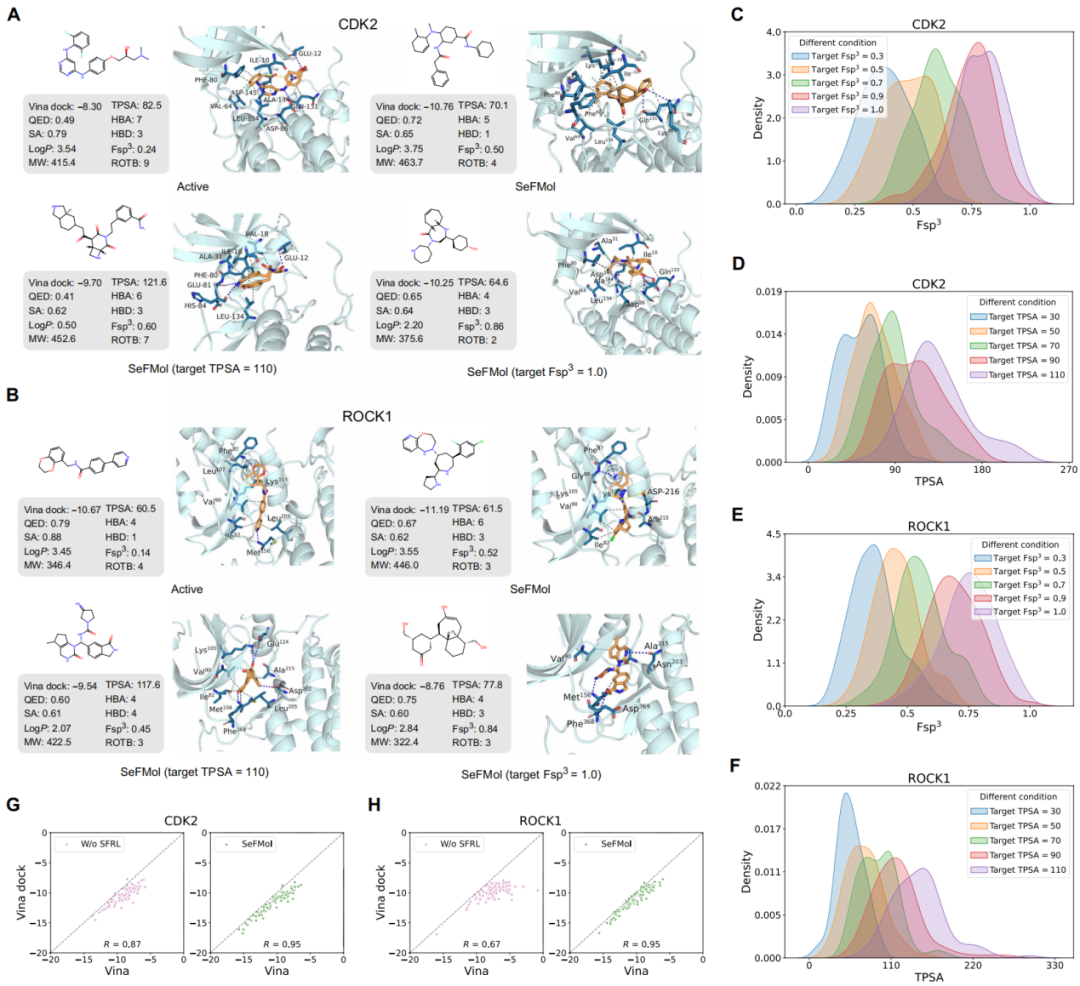
图5. SeFMol 在真实蛋白结构上的应用表现。
研究意义
这项工作值得关注的地方,并不仅仅是它在若干基准指标上超过了现有方法,而是它提出了一种新的基于结构的分子生成思路,即通过在静态数据基础上,将半柔性动态优化机制引入训练过程中。过去的大多数方法更像是在学习如何根据口袋生成一个合理分子,而 SeFMol 则进一步尝试学习如何调整分子,使其更好地适配口袋并满足性质要求。对于先导化合物发现、靶点定制化分子设计以及与实验反馈进一步结合,这种范式都具有较强的启发意义。
参考资料
Xudong Zhang et al. ,Steering semi-flexible molecular diffusion model for structure-based drug design with reinforcement learning.Sci. Adv.12,eady9955(2026).
DOI:10.1126/sciadv.ady9955
源代码链接
https://github.com/ispc-lab/SeFMol
在线服务器
https://www.sefmol.tjai4s.com/
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-04-21,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

