【辰辉创聚生物】重组蛋白完整技术指南
原创【辰辉创聚生物】重组蛋白完整技术指南
原创
辰辉创聚生物
发布于 2026-03-12 23:38:14
发布于 2026-03-12 23:38:14
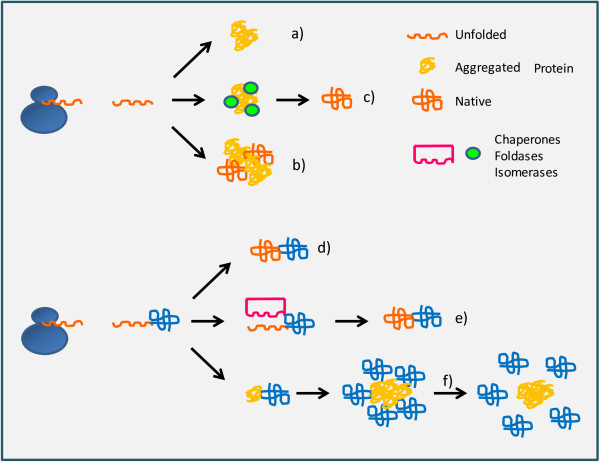
recombinant protein
一、重组蛋白的定义与技术本质
重组蛋白(Recombinant Protein)是指采用基因重组技术,将编码特定蛋白质的外源基因导入合适的宿主细胞,通过细胞的转录和翻译系统表达而产生的蛋白质。这一技术的诞生标志着生命科学研究从天然蛋白提取阶段迈入了人工设计合成的新纪元。
从技术本质上讲,重组蛋白的生产过程涉及以下几个核心环节:目的基因的获取与密码子优化、表达载体的构建、宿主细胞的转染或转化、诱导表达以及蛋白纯化。与天然蛋白相比,重组蛋白具有显著优势:可实现高产量的规模化生产、可引入特定的标签或修饰、可表达难以从天然来源提取的蛋白、批次间一致性更好。
在科研试剂领域,重组蛋白的应用极为广泛,涵盖细胞培养添加剂、检测标准品、免疫检测试剂原料、蛋白质结构功能研究工具、抗体筛选靶点等众多场景。
二、重组蛋白的核心技术参数
(一)纯度
纯度是衡量重组蛋白质量的基础指标。科研级重组蛋白通常采用SDS-PAGE或HPLC进行纯度检测,常规要求纯度大于90%,高灵敏度实验则要求纯度达到95%以上。纯度的检测需考虑目标蛋白是否存在降解片段、聚合体以及宿主蛋白残留等问题。
(二)生物活性
生物活性是重组蛋白功能完整性的关键指标。活性检测方法取决于蛋白类型:
细胞因子:采用细胞增殖实验(如依赖细胞株的增殖)、趋化实验或细胞毒性实验,以ED50(半数最大效应浓度)表示活性
酶类蛋白:通过酶动力学参数(如Kcat、Km)评价催化活性
受体蛋白:采用SPR或BLI技术检测与配体的结合亲和力
(三)内毒素水平
内毒素是革兰氏阴性菌细胞壁的脂多糖成分,可干扰细胞实验。根据实验需求,内毒素级别分为普通级(<1.0 EU/μg)、低内毒素级(<0.1 EU/μg)和极低内毒素级(<0.01 EU/μg)。细胞功能实验和原代细胞培养通常要求低内毒素级别。
(四)翻译后修饰
翻译后修饰(PTM)直接影响蛋白的功能和稳定性:
糖基化:影响蛋白折叠、稳定性和受体识别
磷酸化:调控信号转导通路活性
乙酰化/泛素化:参与表观调控和蛋白降解
三、重组蛋白的主要表达系统
不同表达系统在蛋白产量、修饰能力和应用场景上存在显著差异。
(一)原核表达系统:大肠杆菌
大肠杆菌(E. coli)是应用最广泛的原核表达系统。其优势在于遗传背景清晰、培养周期短、成本低廉、产量高(可达克级)。然而,该系统缺乏真核翻译后修饰机制,难以表达复杂结构蛋白,且还原性胞内环境不利于二硫键的正确形成,易形成包涵体。
适用于表达分子量较小、无需糖基化的胞质蛋白或结构域,如生长因子、部分细胞因子等。
(二)酵母表达系统:毕赤酵母
毕赤酵母(P. pastoris)兼具原核生物易于培养的优点和真核生物的翻译后修饰能力。该系统可进行蛋白糖基化、二硫键形成等修饰,蛋白折叠更接近天然构象,且发酵工艺成熟,可实现高密度培养和高产量表达。
适用于需要糖基化修饰的分泌型蛋白或酶类。
(三)昆虫细胞表达系统:杆状病毒
昆虫杆状病毒表达系统(BEVS)利用Sf9或High Five等昆虫细胞作为宿主。该系统可容纳大片段外源基因插入,具有更接近哺乳动物的蛋白加工能力,能完成复杂的翻译后修饰,且表达水平通常高于哺乳动物系统。
适用于表达复杂结构蛋白、多亚基复合物和需要特定糖基化的蛋白。
(四)哺乳动物细胞表达系统
哺乳动物细胞(如HEK293、CHO)表达系统可产生与天然蛋白完全一致的翻译后修饰,包括复杂的N-糖基化和O-糖基化、磷酸化、乙酰化等。该系统能实现蛋白的正确折叠和组装,生物活性最高。
适用于表达需要完全天然构象的蛋白,如膜蛋白、受体蛋白、抗体片段等。
(五)无细胞蛋白合成系统
无细胞系统是一种新兴的表达技术,采用细胞裂解液或纯化的转录翻译因子,在体外直接合成蛋白。该系统可合成对细胞有毒性的蛋白,合成速度快(数小时完成),且可添加非天然氨基酸或引入特异性标记。
适用于合成毒性蛋白、膜蛋白以及需要快速筛选的突变体文库。
四、重组蛋白的分类与应用场景
(一)细胞因子与生长因子
细胞因子是免疫系统和细胞间通讯的核心调节分子,包括白介素家族(IL-2、IL-6等)、干扰素(IFN-α、IFN-γ)、肿瘤坏死因子(TNF-α)等。生长因子则调节细胞增殖和分化,如表皮生长因子(EGF)、成纤维细胞生长因子(FGF)、转化生长因子-β(TGF-β)等。
在科研中,细胞因子和生长因子主要用于免疫细胞培养、干细胞定向分化、细胞功能研究等场景。
(二)免疫检查点蛋白
免疫检查点分子如PD-1/PD-L1、CTLA-4、TIM-3、LAG-3等在调控免疫应答中发挥关键作用。重组免疫检查点蛋白主要用于抗体药物筛选、免疫调节机制研究以及CAR-T细胞治疗的靶点验证。
(三)酶与调节蛋白
重组酶类包括激酶(如CDK家族)、蛋白酶(如MMP家族)、泛素化相关酶等。这类蛋白主要用于酶动力学研究、抑制剂筛选和信号通路机制解析。
(四)CD抗原与受体蛋白
CD抗原是免疫细胞分型鉴定的核心标志物,如CD3、CD4、CD8、CD19、CD20等。受体蛋白包括G蛋白偶联受体(GPCR)、酪氨酸激酶受体(如EGFR、HER2)、核受体等。重组受体蛋白用于配体-受体结合研究、抗体筛选和结构生物学研究。
(五)病毒蛋白
重组病毒蛋白包括冠状病毒刺突蛋白(Spike)、流感病毒血凝素(HA)、人类免疫缺陷病毒包膜蛋白(HIV Env)等。这类蛋白是病毒与宿主相互作用机制研究、抗病毒药物筛选和疫苗研发的关键试剂。
五、重组蛋白的质量控制
(一)理化性质鉴定
采用质谱技术对蛋白的分子量、氨基酸序列和翻译后修饰进行确证。采用动态光散射(DLS)或尺寸排阻色谱(SEC)分析蛋白的聚集状态和均一性。
(二)纯度分析
采用SDS-PAGE在还原和非还原条件下分析蛋白纯度和二硫键形成情况。采用HPLC-SEC定量分析蛋白聚合体和降解片段的含量。
(三)活性验证
根据不同蛋白类型选择细胞增殖实验、酶活测定或结合实验(SPR/BLI/ELISA)进行活性验证,提供ED50或结合常数(KD)等关键参数。
(四)内毒素检测
采用鲎试剂法(LAL)定量检测内毒素含量,确保符合不同实验的需求。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
评论
登录后参与评论
推荐阅读
目录

