第18篇HD文章--基因背景漂变识别缓解癌症治疗耐药的药物靶点
原创第18篇HD文章--基因背景漂变识别缓解癌症治疗耐药的药物靶点
原创
追风少年i
发布于 2026-03-07 10:25:13
发布于 2026-03-07 10:25:13
作者,Evil Genius
事业编考试临近了,希望大家都可以考出好成绩,成功上岸。
宇宙的尽头是编制,这句话在科研领域,是铁律,没有编制托底,认真搞科研无从谈起。
今天我们继续分享文献

知识积累
癌症由正常细胞和恶性细胞的异质性群体构成,这些细胞对治疗的反应不同,从而产生复杂且动态的疗效与耐药模式,而这是难以预测的。
癌症对治疗靶点的依赖性也各不相同。相同的突变在不同肿瘤中可能起到促进或抑制作用,并且表达相似水平药物靶点的癌症,对小分子抑制剂的反应也可能存在差异。
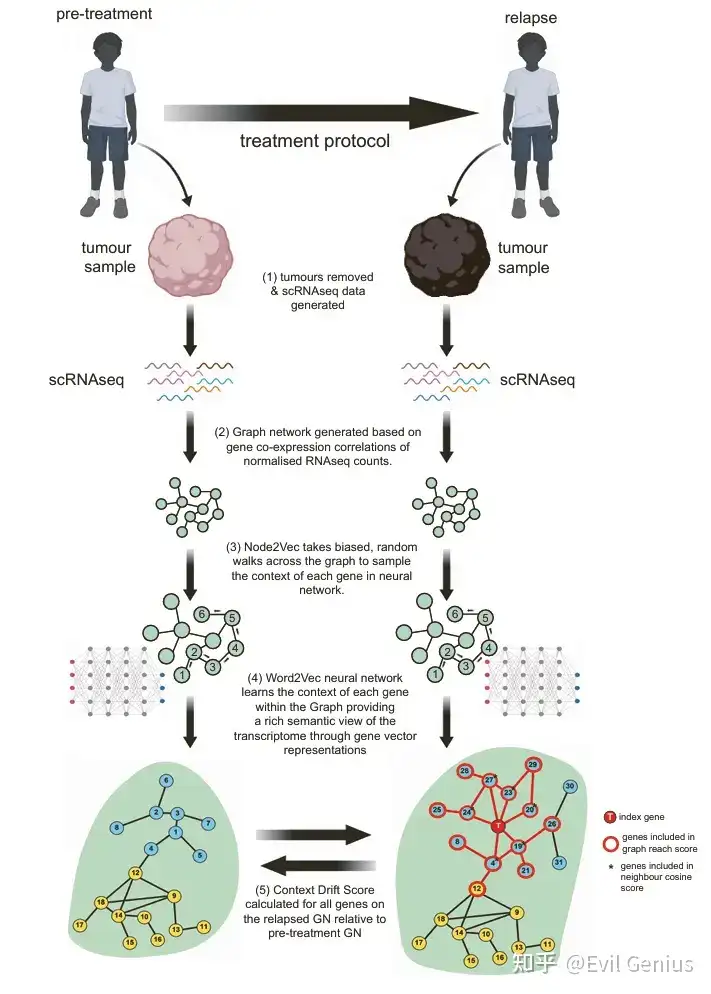
NLP最初是为了“阅读”大量文本而开发的,通过嵌入向量生成强大的词语表征,从而学习词语通常出现的上下文。我们设想,这种词嵌入技术可以被改造用于基因共表达数据,从而能够描绘癌症发展和治疗耐药过程中基因共表达关系的变化。
结果1、RECODR-原发肿瘤易感性预测
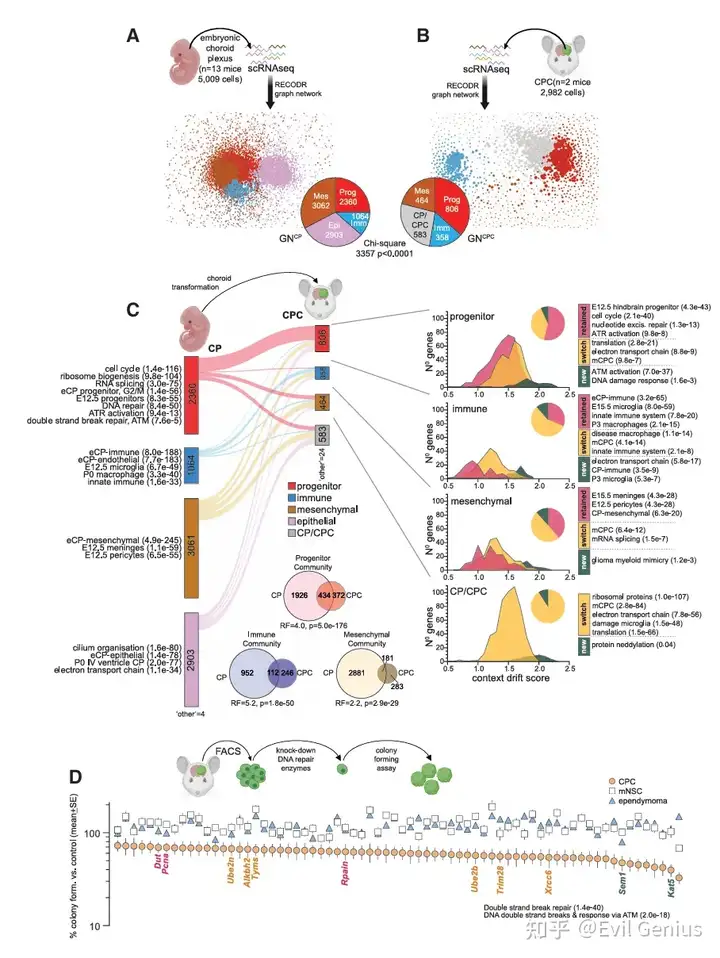
脉络丛癌是一种罕见的儿童脑肿瘤,目前缺乏有效的分子靶向治疗,尤其是TP53突变型CPC预后极差。研究团队利用之前构建的基因工程小鼠CPC模型,结合单细胞RNA测序技术,探究正常脉络丛向CPC转化过程中的基因背景变化。
RECODR分析揭示肿瘤发生机制
通过对2982个CPC细胞与正常CP细胞的scRNA-seq图谱进行RECODR分析,团队构建了共表达图网络。结果显示:
基因保留:约三分之一的基因在正常组织和肿瘤中保留了相同的共表达背景("retained"基因),表明CPC保留了胚胎祖组织的特征。
基因切换:约三分之二的基因在肿瘤发生过程中改变了其所在的共表达群落("switched"基因),表明其功能背景发生了变化。
基因新募:9%的基因被新招募到肿瘤网络中("new"基因)。
量化基因背景漂移
RECODR采用图嵌入方法(Node2Vec + Word2Vec)为每个基因计算"背景漂移分数",该分数综合了四个指标:邻居数量变化、图覆盖范围、邻居余弦相似度、索引基因余弦相似度。结果显示,DNA修复调控因子(特别是ATM通路相关基因,如Kat5)在肿瘤发生过程中表现出最高的背景漂移,提示其在CPC发生中起关键作用。
实验验证:ATM是CPC的潜在治疗靶点
功能筛选:通过shRNA沉默227个DNA修复基因,发现70个基因对CPC克隆形成至关重要,其中ATM通路(尤其是Kat5)需求最高。
药物验证:使用ATM抑制剂AZD1390治疗荷瘤小鼠,两种给药方案显著抑制肿瘤生长,并延长了小鼠生存期。这是首次报道ATM抑制剂单药在癌症中显示出疗效。
方法比较与优势
与现有方法(差异表达分析、WGCNA、diffcoexp、scDRUG)相比,这些方法均未将ATM识别为CPC的高优先级靶点,突显了RECODR在发现隐藏耐药机制和治疗靶点方面的独特优势。
结论:RECODR通过捕捉基因在疾病发展过程中的"背景漂移",成功识别出ATM作为CPC的治疗脆弱点,为开发新的联合治疗方案提供了理论依据。
结果2、RECODR-预测单药治疗耐药性
研究背景:单药治疗终将耐药
尽管AZD1390或放疗单药治疗初期有效,但所有小鼠的肿瘤最终都复发,模拟了临床中单药治疗导致耐药的现象。
RECODR分析揭示耐药机制
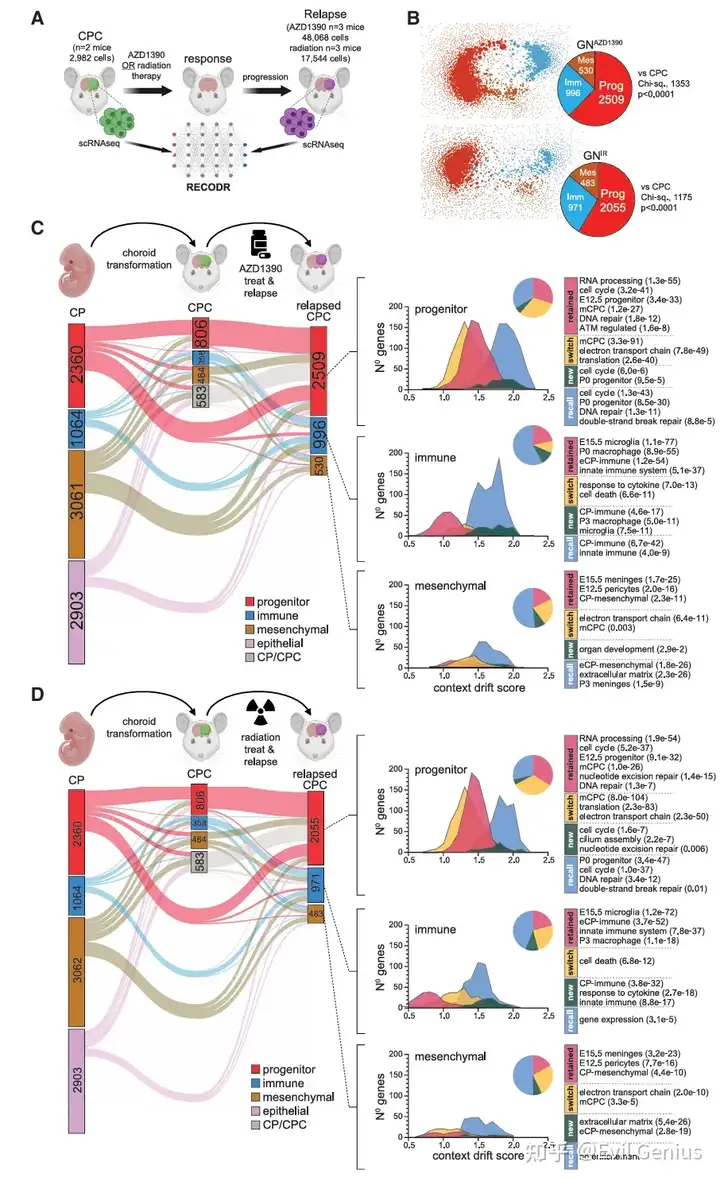
通过对比未经治疗的CPC与AZD1390耐药、放疗耐药肿瘤的单细胞转录组图谱,RECODR发现:
相似的重编程:两种不同作用机制的疗法产生耐药后,其基因共表达网络高度相似,表明肿瘤通过共同的机制抵抗治疗。
祖细胞群落扩张:耐药肿瘤中,"祖细胞"相关基因群落扩大了2-3倍,且该群落中的基因表现出最高的背景漂移分数,提示其在耐药中起核心作用。
胚胎基因的"召回":约三分之一耐药肿瘤祖细胞群落中的基因,在未经治疗的CPC中不存在,但存在于胚胎正常脉络丛中。这表明肿瘤在耐药过程中"召回"了胚胎发育时期的功能程序。
"召回"基因的功能:这些基因富集于细胞周期调控(如Cdk6、Ccna2)和DNA双链断裂修复(如Parp1、Rad51)通路,且表现出最高的背景漂移。
靶点筛选与联合用药策略
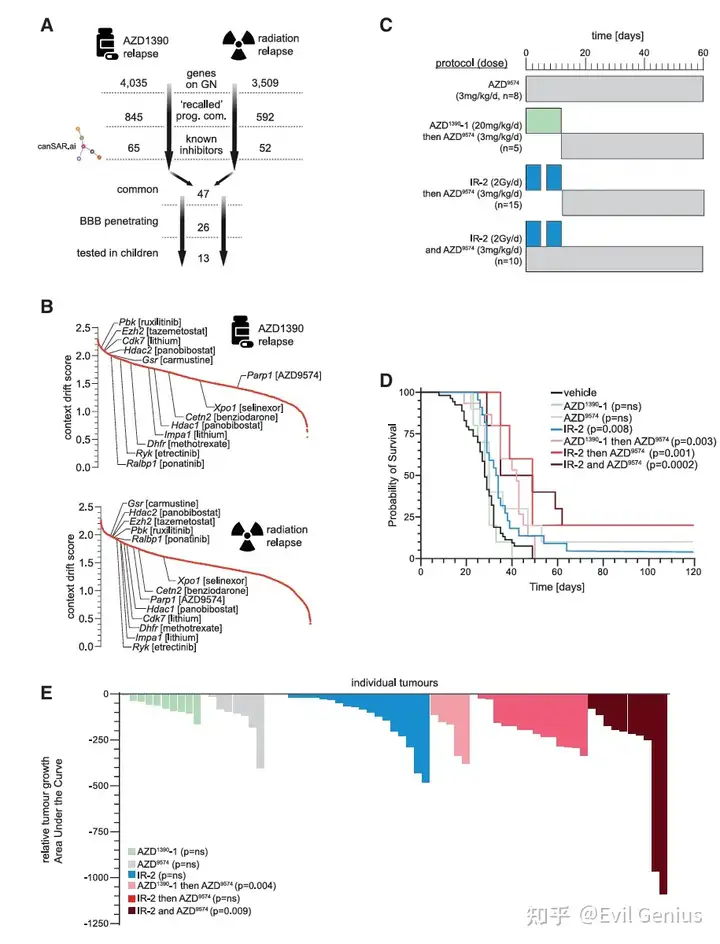
基于背景漂移分数,研究团队筛选了13个潜在靶点,筛选标准包括:同时出现在两种耐药网络的"召回"基因中、有临床可用且能穿透血脑屏障的抑制剂、已在儿童中测试过。
关键靶点:PARP1:Parp1在未经治疗的CPC中几乎不表达,但在耐药肿瘤中被显著"召回"并高表达。
实验验证:使用新型脑穿透性PARP抑制剂AZD9574单药治疗未经治疗的CPC无效(符合RECODR预测),但将AZD9574与AZD1390或放疗联用,显著增强了抗肿瘤效果,延缓或克服了耐药。
方法比较与优势
与差异表达分析、diffcoexp、scDRUG、WGCNA等方法相比,这些传统方法均未将Parp1识别为关键耐药靶点,或未能准确预测其对不同肿瘤状态的选择性疗效,凸显了RECODR在捕捉转录组动态变化和识别耐药特异性靶点方面的独特优势。
结论:RECODR通过捕捉耐药过程中基因背景的漂移,成功识别出PARP1是CPC克服AZD1390/放疗耐药的关键靶点,并验证了PARP抑制剂联合疗法的有效性。这为理解肿瘤耐药的可塑性机制和开发合理的联合治疗方案提供了新范式。
结果3、RECODR方法如何进一步用于分析联合治疗(AZD1390+放疗)后的耐药机制
研究背景:联合治疗仍无法完全克服耐药
尽管在AZD1390或放疗基础上加用PARP抑制剂AZD9574显著提升了疗效,但大多数小鼠仍然复发(仅AZD9574+放疗组有20%实现长期生存)。研究团队转向临床正在测试的AZD1390+放疗联合方案,试图通过RECODR解析其耐药机制。
联合治疗方案筛选
实验设计:将65只荷瘤小鼠随机分为7组(方案A-G),接受不同强度和时序的AZD1390+放疗联合治疗。
疗效结果:5个方案(B、C、E、F、G)的肿瘤抑制效果和生存期显著优于单药治疗,但所有方案最终均出现治疗失败(肿瘤复发)。
RECODR分析揭示联合治疗耐药机制
样本来源:对方案E(与临床使用方案相似)复发后的肿瘤进行单细胞RNA测序,获得8,032个细胞的转录组图谱。
比较分析:将这些数据与正常CP、未经治疗CPC以及单药耐药肿瘤的基因网络进行RECODR对比分析,旨在识别驱动联合治疗耐药的基因背景变化。
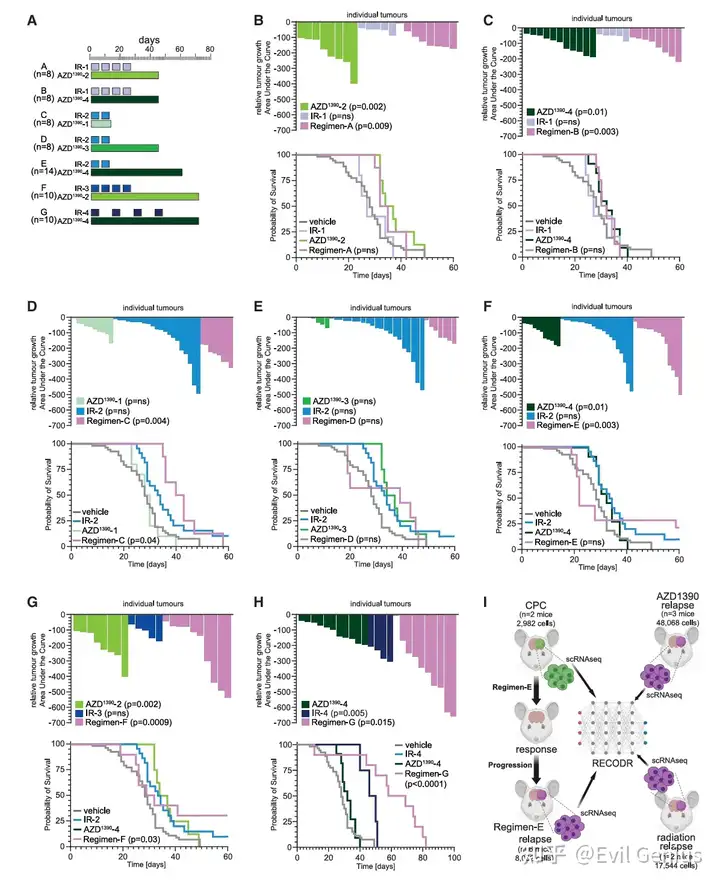
联合治疗耐药后的独特基因网络变化
免疫群落显著扩张:与未经治疗的CPC或单药耐药肿瘤相比,联合治疗(方案E)耐药后的基因网络中,免疫相关基因群落显著扩大。该群落中的基因获得了最高的背景漂移分数。
基因来源:该免疫群落包含82%的"新"基因(在未经治疗和单药耐药网络中均不存在)和53%的"召回"基因(来源于胚胎正常脉络丛),富集于先天免疫、小胶质细胞、巨噬细胞等功能。
祖细胞群落持续存在:与单药耐药类似,联合耐药肿瘤中也保留了扩张的祖细胞群落,富集细胞周期和DNA修复相关基因,且功能验证显示DHFR蛋白表达升高、γH2AX表达降低(分别提示增殖增强和DNA修复能力增强)。
免疫群落来源的探究:肿瘤细胞发生了"髓系拟态"
问题提出:由于所有测序细胞均为FACS分选的YFP+/RFP+肿瘤细胞,免疫群落的出现提示肿瘤细胞本身可能获得了免疫样特征(髓系拟态),而非单纯由污染的非肿瘤免疫细胞引起。
多模态验证:
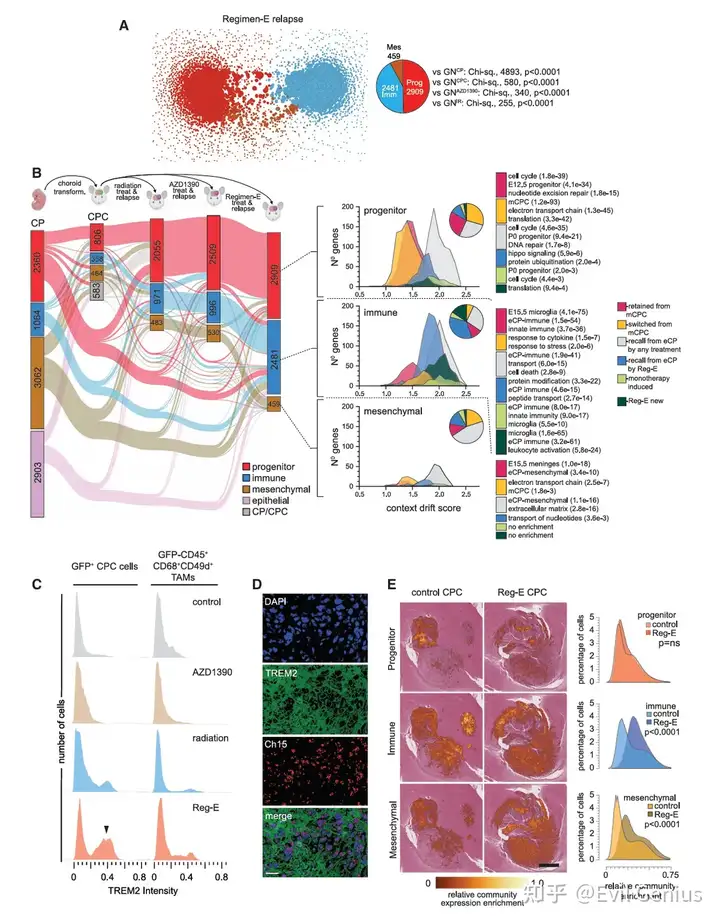
流式细胞+FISH:在联合耐药肿瘤中鉴定出一群高表达TREM2、GFP阳性、且获得15号染色体拷贝数扩增的恶性细胞。这些细胞在表面标志物上明显区别于肿瘤相关巨噬细胞(TREM2+/CD45+/CD68+等)和小胶质细胞。
空间转录组学(Visium HD):在具有非整倍体(如15号染色体扩增)的肿瘤细胞中,免疫群落、祖细胞群落和间质群落的共表达显著富集,且联合耐药肿瘤中免疫群落的表达高于对照组。更重要的是,这些群落特征在同一空间bin内共表达,提示同一个肿瘤细胞同时激活了多种程序。
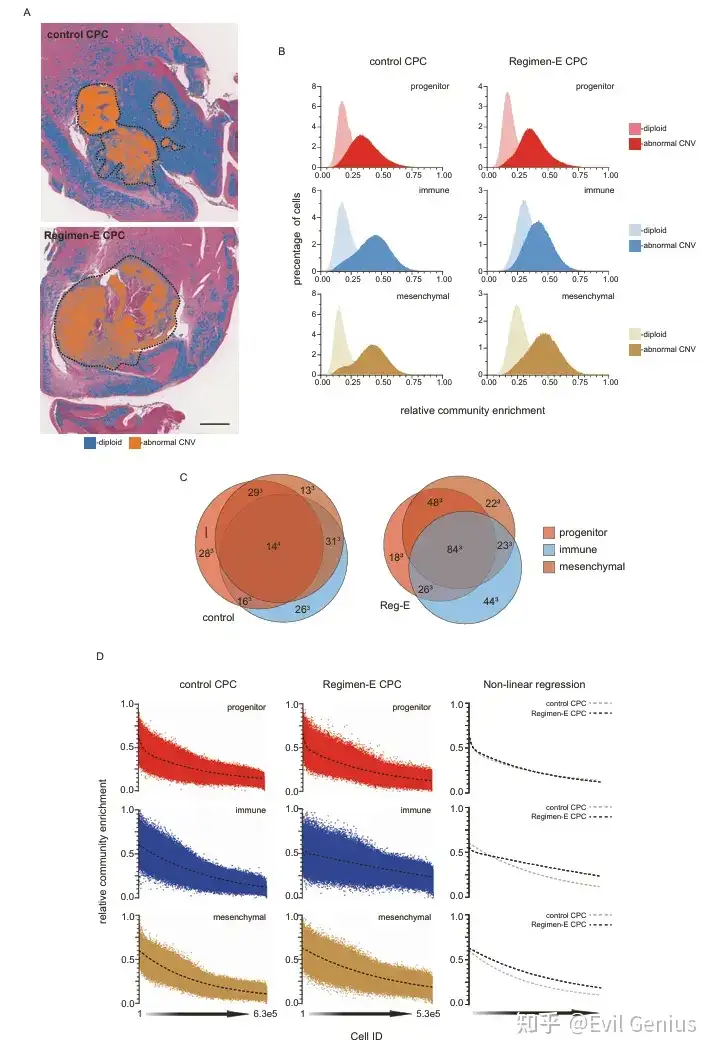
主要结论
RECODR揭示了对联合治疗耐药的复杂机制:
单药驱动机制:保留了祖细胞群落的扩张(细胞周期、DNA修复激活)。
联合特有机制:触发了免疫群落的扩张,表现为肿瘤细胞获得"髓系拟态"特征(如表达TREM2),这可能是联合治疗压力下肿瘤细胞采取的全新适应策略。
这表明,联合治疗虽然初期效果更好,但最终诱导了更为复杂的耐药表型,肿瘤细胞通过"召回"胚胎免疫相关程序来逃避治疗压力。
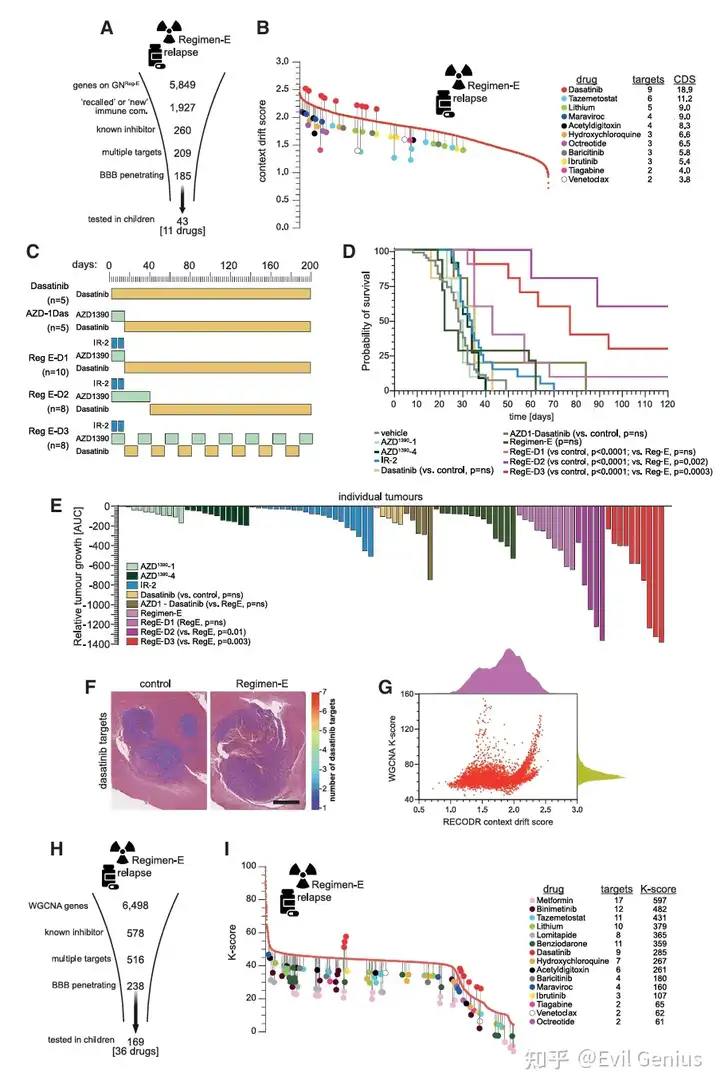
靶点筛选策略
为了找到能缓解AZD1390+放疗联合耐药的靶点,研究团队对联合耐药肿瘤基因网络(GNReg-E)中的5,849个基因进行了筛选,标准包括:
位于免疫群落且为"召回"或"新"基因;
有临床可用且能穿透血脑屏障的抑制剂;
抑制剂已在儿童中测试过;
优先选择能同时靶向多个免疫群落基因的药物(因为可能更有效破坏耐药网络)。
达沙替尼脱颖而出
多靶点覆盖:达沙替尼靶向的基因中,有9个(如Lyn, Syk, Btk, Hck等)位于联合耐药肿瘤的免疫群落中。
背景漂移分数高:这些靶基因的累积背景漂移分数最高。
对比鲜明:在未经治疗的CPC或单药耐药网络中,几乎找不到达沙替尼的靶点,或靶点背景漂移分数很低。
实验验证RECODR的预测
根据RECODR的预测,研究团队设计了5个治疗组(共36只小鼠):
预测1:达沙替尼单药或AZD1390序贯达沙替尼无效 → 实验结果证实无效。
预测2:在联合治疗耐药过程中适时加入达沙替尼(尤其是方案E-D2和E-D3)应有效 → 实验结果:
E-D2和E-D3方案显著抑制肿瘤生长,大幅延长小鼠生存期;
60%的小鼠实现长期无瘤生存(而联合治疗本身最终全部复发)。
方法比较
与RECODR相比,其他计算方法表现不佳:
差异表达分析:未检测到达沙替尼任何靶点在耐药后差异表达。
diffcoexp:仅检测到一个靶点(Grb2)的低水平差异共表达。
WGCNA:K-score无法有效区分潜在靶点,未能优先识别达沙替尼的价值。
核心结论
RECODR成功预测了:
达沙替尼的疗效具有严格的背景依赖性(仅在联合耐药后的免疫群落激活时才有效);
基于此预测,设计了高效的治疗方案,使60%的小鼠实现长期生存。
这验证了通过靶向耐药后新出现的"免疫拟态"细胞程序来克服联合治疗耐药的可行性。
结果4、将RECODR方法应用于临床患者数据(髓母细胞瘤和三阴性乳腺癌)
髓母细胞瘤:识别耐药亚型特异性背景漂移
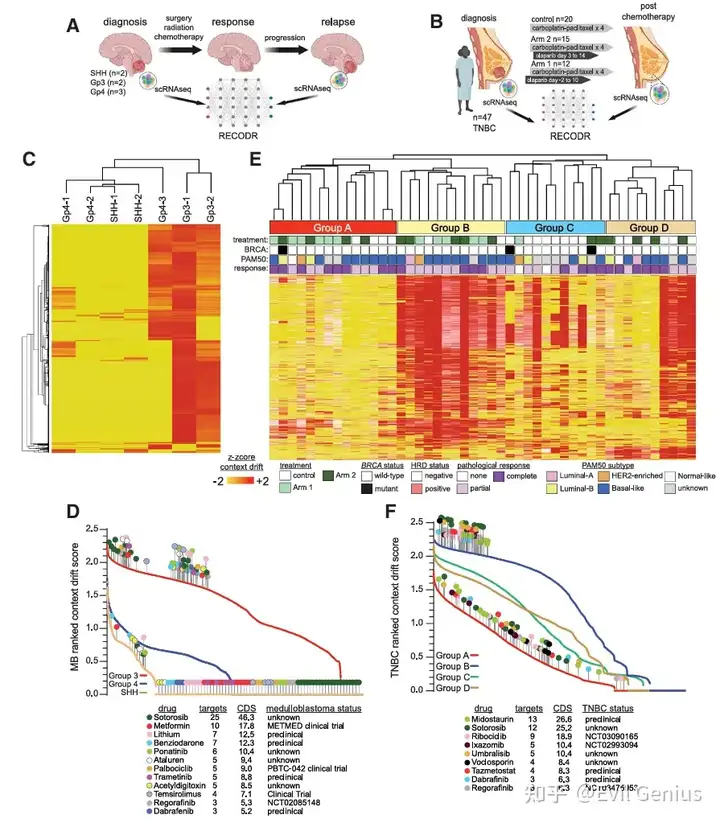
数据来源:对7例髓母细胞瘤患者(SHH亚型2例、Group 3亚型2例、Group 4亚型3例,含1例转移性)在诊断时和复发后的配对肿瘤scRNA-seq数据进行分析。
关键发现:在治疗前后,Group 3亚型和转移性Group 4肿瘤中,有4,500个基因表现出最高的背景漂移分数,而SHH亚型和非转移性Group 4肿瘤中这些基因几乎无变化。这提示RECODR捕捉到了与耐药性相关的动态变化,而非静态的亚型分类特征。
信息独特性:这4,500个基因中,只有1%与基于表达水平区分亚型的差异表达基因重叠,说明背景漂移分数提供了与传统表达分析不同的信息维度。
潜在新疗法预测:基于这些高背景漂移基因,筛选出12种已用于儿童且能穿透血脑屏障的药物。其中8种(如二甲双胍、帕博西尼、替西罗莫司、瑞戈非尼、曲美替尼等)已在髓母细胞瘤的临床或临床前研究中,但RECODR的结果提示它们最有可能在Group 3亚型中克服耐药,若在其他亚型中测试可能被误判为无效。
三阴性乳腺癌:识别具有高转录组可塑性的新亚组
数据来源:分析PARTNER临床试验中47名TNBC患者在新辅助化疗前后配对的snRNA-seq数据。
新亚组发现:利用背景漂移分数变化最大的4,500个基因进行无监督聚类,将TNBC分为4个亚组(A-D)。其中B组(12例)显示出特别高的基因背景漂移分数,提示这些肿瘤具有内在的高转录组进化能力,可能代表了既往未知的TNBC亚型。
与表达谱聚类的区别:基于背景漂移分数的聚类结果不同于基于基因表达水平的聚类,进一步证明其信息的独特性。
潜在新疗法预测:针对B组的背景漂移基因,预测了9种可能添加到新辅助治疗中的药物。其中6种(如瑞博西尼、伊沙佐米、瑞戈非尼、米哚妥林、他泽美司他等)已在TNBC的临床或临床前研究中。
核心结论
RECODR能够从临床患者的纵向测序数据中,捕捉到传统表达分析无法揭示的、与治疗耐药相关的动态基因背景变化。
在髓母细胞瘤中,成功识别出Group 3亚型特有的耐药相关基因变化,并预测了亚型特异性的潜在治疗药物。
在TNBC中,基于背景漂移分数发现了一个具有高转录组可塑性的新亚组(B组),并为其预测了潜在的联合治疗策略。
这为将RECODR应用于临床、指导个体化治疗和克服耐药提供了初步证据。
最后来看看方法
visium HD

visium HD分析CNV

生活很好,有你更好。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
评论
登录后参与评论
推荐阅读
目录

