顶刊分享(第11篇HD文章)--感觉神经元通过刺激乳腺癌微环境中的致密细胞外基质驱动免疫排斥
原创顶刊分享(第11篇HD文章)--感觉神经元通过刺激乳腺癌微环境中的致密细胞外基质驱动免疫排斥
原创
追风少年i
发布于 2026-02-12 10:11:02
发布于 2026-02-12 10:11:02
作者,Evil Genius
visium HD技术经历了将近2年的沉淀和积累,感觉要迎来一波小的“爆发”了,敢第一批吃“螃蟹”的人要收获一定的成果了,今天我们分享搜集的第11篇HD的文章,cell正刊。
当然,多说一句,现在单细胞空间的分析研究不能简单的说一下是癌种样本就可以了,而是要根据病理和基因组信息进行详细分子分型,文章就针对的是三阴性乳腺癌。
知识积累
三阴性乳腺癌以缺乏雌激素受体、孕激素受体表达及人表皮生长因子受体2(HER2)无扩增或过表达为特征,至今仍是乳腺癌中侵袭性最强、最难治的亚型。
然而仅部分三阴性乳腺癌患者能从免疫检查点阻断疗法中获益。导致免疫治疗耐药的关键因素在于肿瘤微环境的紊乱。
结果1、三阴性乳腺癌中神经浸润与失调的肿瘤微环境相关,并以感觉神经元为主导
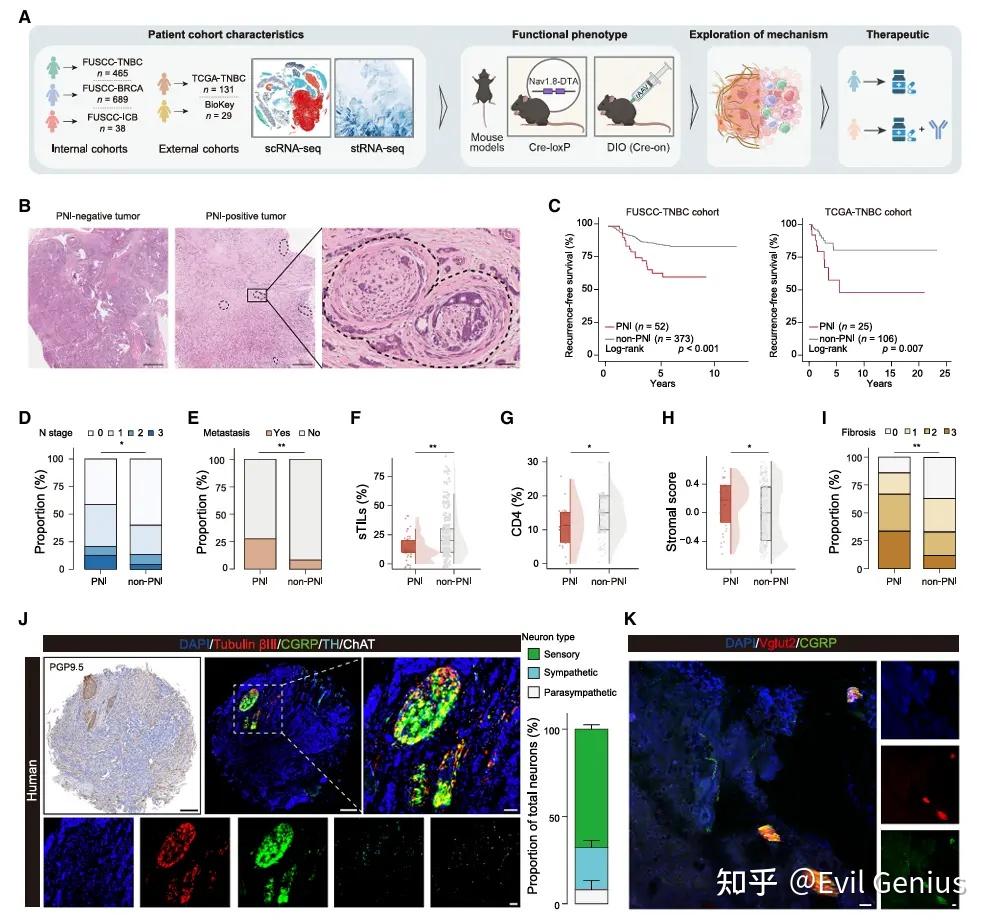
整合复旦大学附属肿瘤医院三阴性乳腺癌队列(n=465)数据,通过评估H&E染色图像判定神经浸润状态。
存在神经浸润的患者无复发生存期更短,在癌症基因组图谱三阴性乳腺癌队列(n=131)中的验证分析得出相似预后结论。神经浸润密度越高预后越差。神经浸润阳性还与更晚期的淋巴结分期及更高转移率(尤其是骨转移)相关。多因素Cox分析显示神经浸润是独立预后因素,凸显其临床重要性。
存在神经浸润的肿瘤组织中肿瘤浸润淋巴细胞、CD4+ T细胞及三级淋巴结构/淋巴细胞聚集显著减少,表明抗肿瘤免疫应答减弱。同时神经浸润伴随明显的间质活化,包括更高的间质评分、更严重的纤维化及纤维化相关基因表达上调。
乳腺组织中分布着感觉神经元、交感神经元与副交感神经元。通过多重免疫荧光技术检测肿瘤组织中神经元类型密度发现,虽然交感与副交感神经元同时存在,但感觉神经元约占三阴性乳腺癌组织神经突总面积的70%。
神经浸润是三阴性乳腺癌的不良预后因素,与促纤维增生及免疫抑制的肿瘤微环境相关,其中源自胸11至腰4节段背根神经节的感觉神经元是主要神经类型。
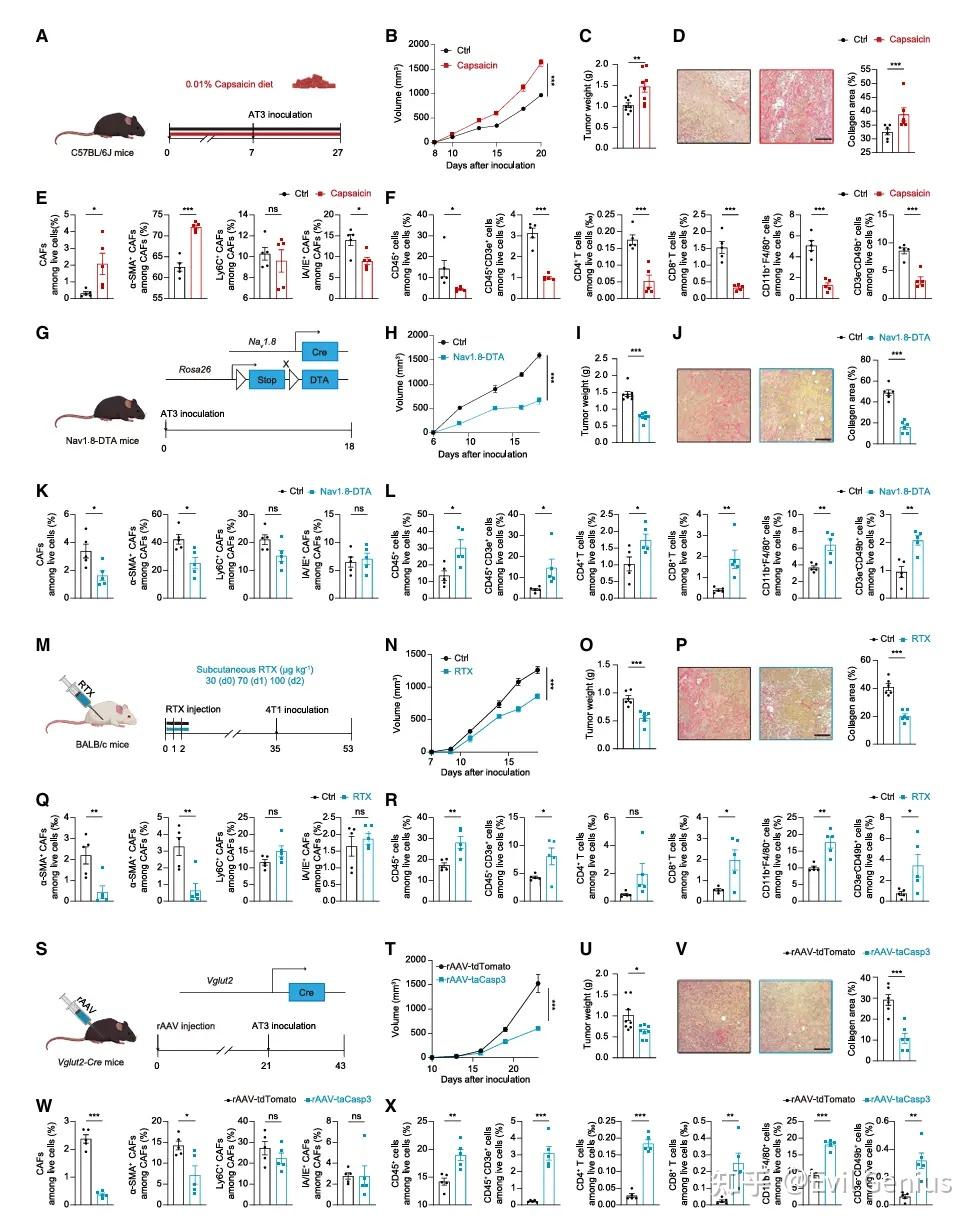
结果2、感觉神经元通过刺激胶原沉积并减少免疫浸润加速肿瘤进展
感觉神经元激活驱动促纤维增生与免疫抑制:
模型验证: 低剂量辣椒素饮食成功激活全身感觉神经元(通过行为学及CGRP水平升高证实)。
表型结果: 神经元激活显著加速肿瘤生长,并促进肿瘤纤维化。
机制探究:
感觉神经元激活后,肿瘤内癌症相关成纤维细胞(CAFs)总数增加,其中主要富集肌成纤维细胞型(myCAFs)亚群。
myCAFs分泌的I型胶原表达上调,这是形成致密、免疫排斥性TME的关键细胞外基质成分。
免疫影响: 感觉神经元激活导致多种抗肿瘤免疫细胞(包括T细胞、巨噬细胞、NK细胞等)的浸润显著减少,但未改变这些免疫细胞亚群的分化比例。
特异性验证: 该模型未影响交感/副交感神经活性(NE/ACh水平不变),也无明显肝肾毒性,表明效应由感觉神经元特异性介导。
消融感觉神经元可逆转TME紊乱并抑制肿瘤:
通过三种独立的消融模型(基因敲除、化学消融、局部病毒介导消融)一致证明:
抑制肿瘤: 消融感觉神经元(无论全身或局部)均能显著减缓肿瘤生长。
重塑TME:
减少促纤维化: 肿瘤内CAFs(特别是myCAFs)比例下降,I型胶原沉积减少。
增强免疫浸润: 肿瘤中免疫细胞(包括CD4+和CD8+ T细胞)的浸润增加,免疫功能得到“恢复”。
特异性与局部效应: 局部瘤内消融感觉神经元即足以产生上述抗肿瘤效果,排除了全身性影响的干扰,凸显了局部感觉神经浸润在TNBC TME紊乱中的核心作用。
总结核心机制:
感觉神经元在TNBC中通过促进CAFs向myCAFs表型分化,刺激胶原(尤其是I型胶原)沉积,从而构建致密的纤维化间质。这种物理和生化屏障阻碍了抗肿瘤免疫细胞的浸润,最终导致免疫排斥性TME的形成和肿瘤进展。逆转这一神经-CAF轴(消融感觉神经元)能够解除免疫抑制,为TNBC治疗提供了新的潜在靶点。
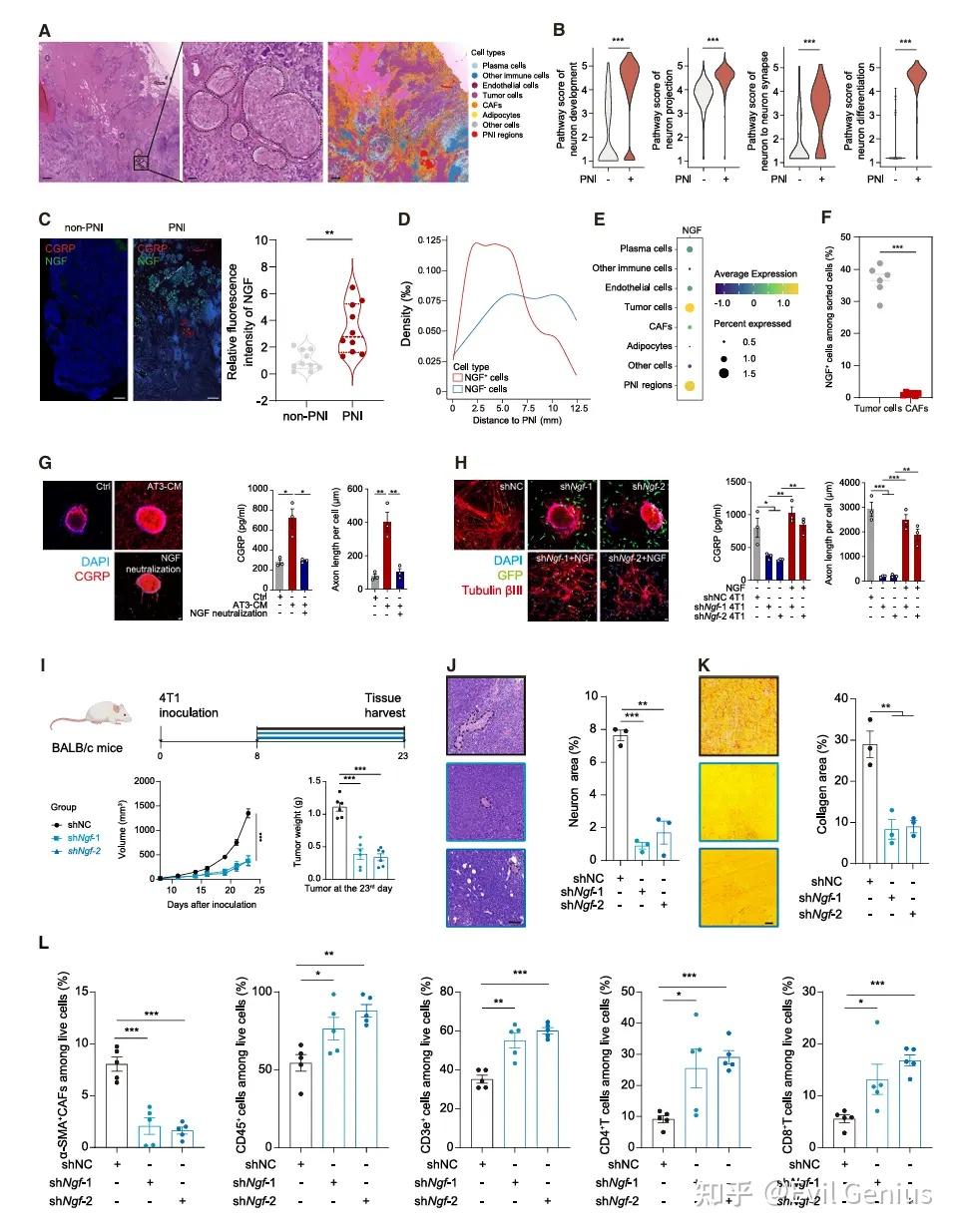
结果3、肿瘤来源的NGF促进感觉神经元神经突生长与CGRP分泌
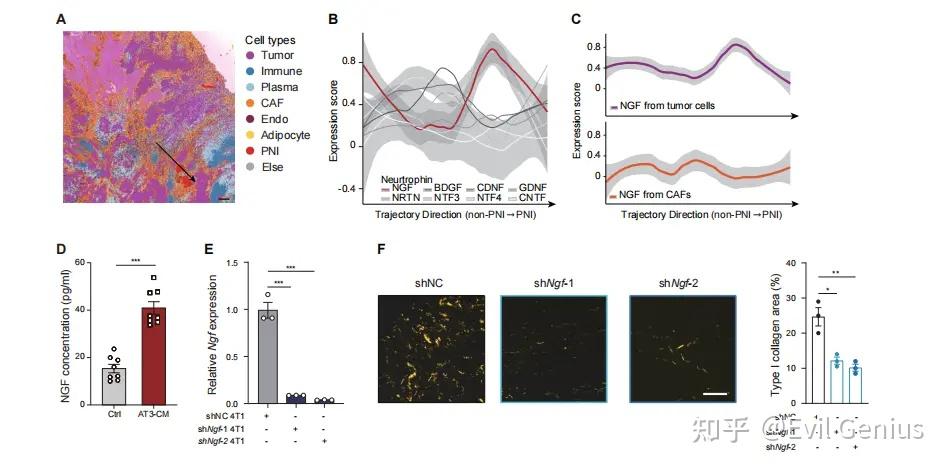
神经元发育与分化等相关通路在神经浸润区域显著富集。空间轨迹分析揭示了从非神经浸润区到神经浸润区的发育轨迹,其中神经生长因子在神经浸润区附近特异性富集。
多重免疫荧光染色进一步证实,神经浸润阳性样本中的NGF水平显著更高。对神经浸润阳性样本的空间距离分析显示,NGF阳性细胞在神经浸润区域邻近位置显著富集,提示NGF可能具有促进神经浸润的作用。
在三阴性乳腺癌中,与神经浸润区域空间共定位的NGF主要来源于肿瘤细胞而非癌症相关成纤维细胞。
肿瘤分泌的NGF不仅能够吸引神经元,还参与破坏肿瘤微环境并促进肿瘤生长。
结果4、感觉神经元邻近CAFs并促进胶原沉积
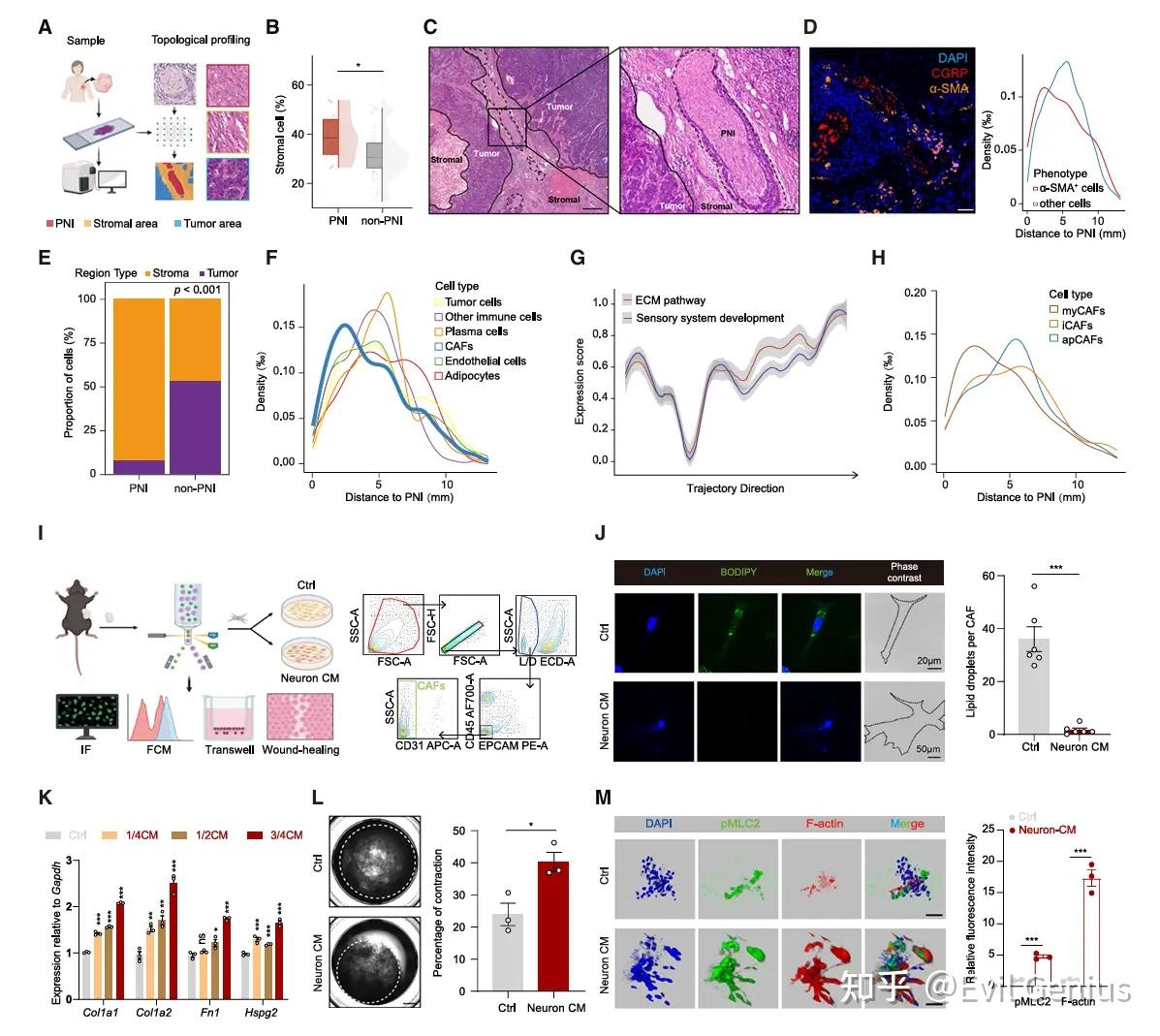
感觉神经元条件培养基处理并未改变AT3肿瘤细胞的增殖与迁移能力。因此将研究重心转向神经浸润的肿瘤微环境特征。
在Visium HD样本分析中,将区域划分为500 μm网格,根据基质细胞是否多于肿瘤细胞将其分类为基质区或肿瘤区。绝大多数神经浸润位于基质区域。此外,癌症相关成纤维细胞在神经浸润邻近区域高度富集,而免疫细胞则显著远离神经浸润区域。
这些发现与轨迹分析结果一致:细胞外基质通路与感觉系统发育通路呈现高度共表达。结合感觉神经元消融模型中癌症相关成纤维细胞的急剧减少现象,提示癌症相关成纤维细胞可能是感觉神经元的作用靶点。
为明确感觉神经元对癌症相关成纤维细胞的影响,我们对空间转录组数据中的癌症相关成纤维细胞进行亚群分析,鉴定出肌成纤维细胞型、炎症型和抗原呈递型三个亚群(图S4D)。其中肌成纤维细胞型与神经浸润的空间距离最近。
感觉神经元驱动的肌成纤维细胞型激活可能促进免疫抑制性肿瘤微环境的形成。
结果5、感觉神经元来源的CGRP结合CAFs上的RAMP1促进胶原分泌
感觉神经元通过分泌CGRP激活CAFs,驱动胶原沉积。
关键信号分子与受体:
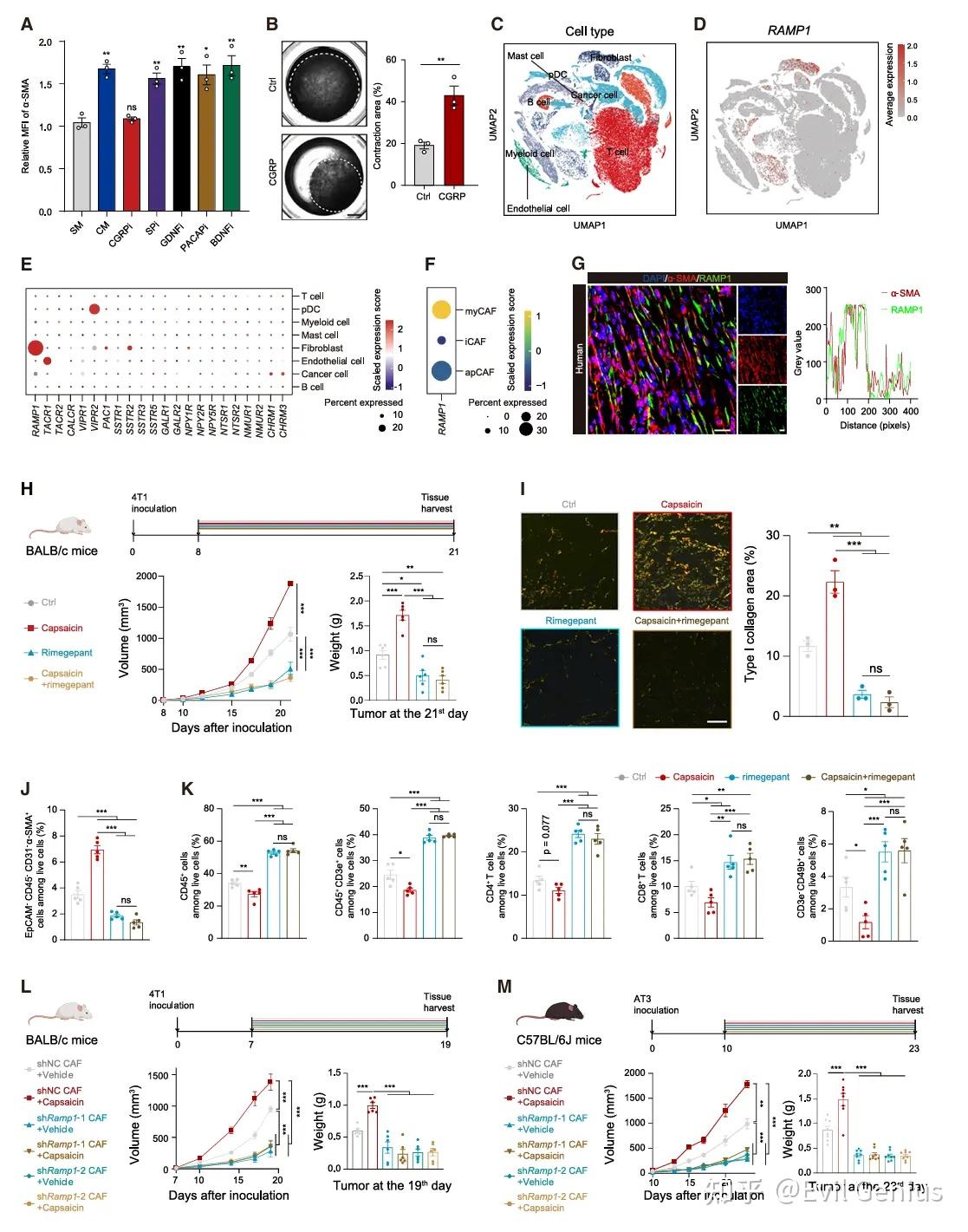
上游信号: 感觉神经元释放的主要神经肽——降钙素基因相关肽(CGRP),是激活肌成纤维细胞型癌症相关成纤维细胞(myCAF)的关键介质。
下游受体: CGRP受体复合物的关键组分 RAMP1 在癌症相关成纤维细胞(CAFs),尤其是myCAF亚群上特异性高表达,与myCAF标志物呈强正相关。
机制验证:
体外实验:
CGRP能诱导静息态CAFs活化,并增强其迁移和胶原收缩功能,但不影响其增殖。
CGRP抑制剂瑞美吉泮(rimegepant) 可特异性阻断神经元条件培养基诱导的myCAF表型。
体内验证:
药理学阻断(瑞美吉泮)或基因敲低CAFs上的RAMP1,均能有效抑制感觉神经元激活(辣椒素饮食)所驱动的肿瘤生长。
阻断CGRP-RAMP1轴后,肿瘤微环境发生重塑:myCAF比例和I型胶原沉积减少,同时 CD8+ T细胞等免疫细胞浸润增加。
该效应依赖于完整的免疫系统(在免疫缺陷小鼠中未观察到),表明其作用是通过调节肿瘤免疫微环境实现的。
从感觉神经元到肿瘤基质的明确信号通路:感觉神经元 → 分泌CGRP → 结合CAFs上的RAMP1受体 → 激活myCAF表型 → 促进胶原沉积、形成免疫排斥性微环境。阻断CGRP-RAMP1轴(例如使用rimegepant)能够逆转这一过程,抑制肿瘤生长并改善免疫浸润,这为三阴性乳腺癌的联合免疫治疗提供了新的潜在策略和靶点。
结果6、CGRP-RAMP1轴通过cAMP/PKA/CREB1通路增强CAFs的胶原生物合成
信号通路的确定:
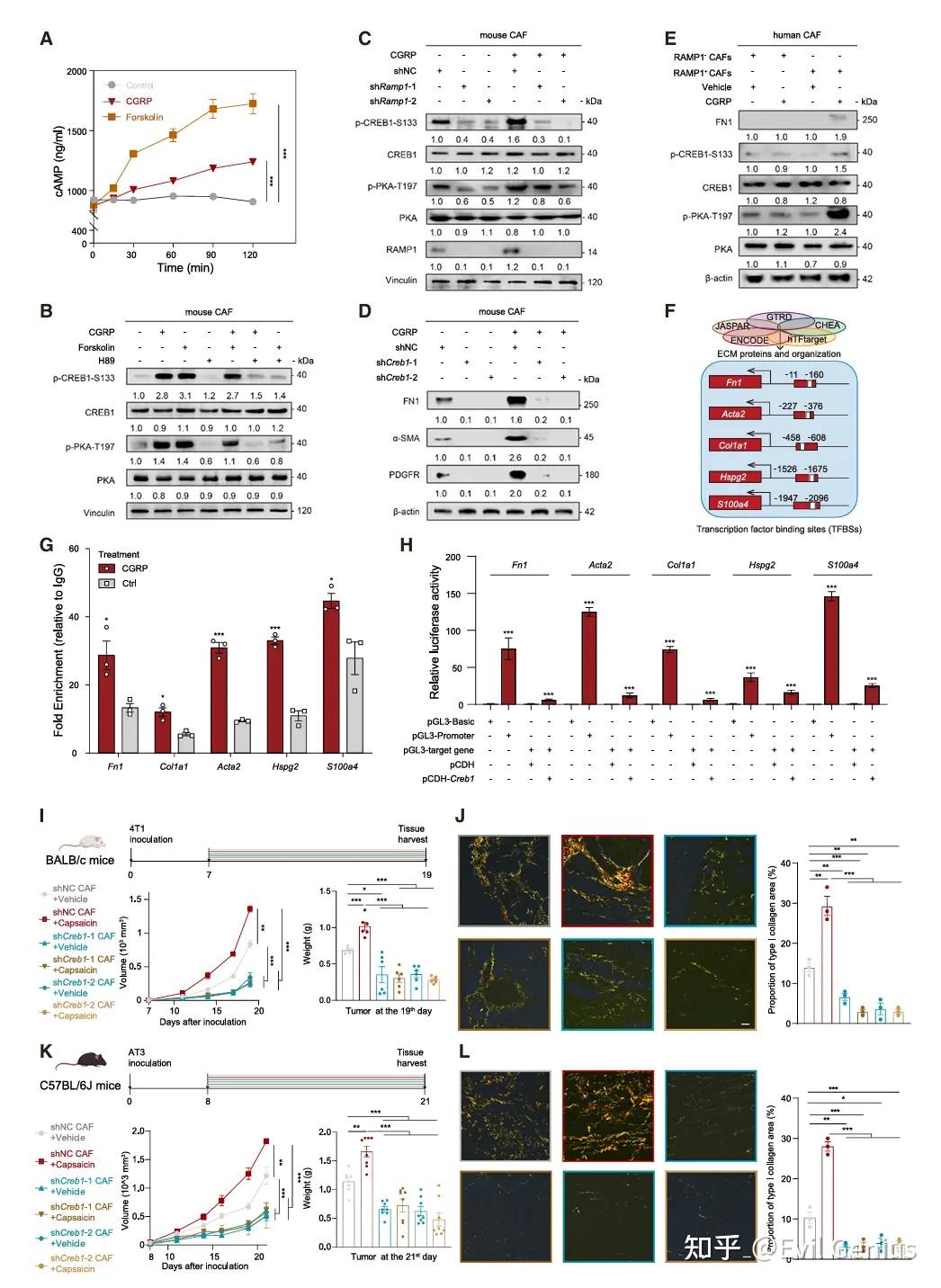
通路激活: CGRP与CAFs上的RAMP1受体结合后,激活了经典的 cAMP/PKA/CREB1信号通路。
证据:CGRP处理增加了CAFs内cAMP水平,并诱导了PKA及其下游转录因子CREB1的磷酸化。
特异性:PKA抑制剂(H89)可阻断此效应,敲低RAMP1则使CAFs对此通路激活无反应。
下游转录调控机制:
关键转录因子: 磷酸化的CREB1是驱动胶原合成的核心转录因子。
功能缺失:敲低CREB1会直接阻碍胶原合成,并降低肌成纤维细胞型标志物(FN1, α-SMA, PDGFR)的表达,即使存在CGRP刺激也无法挽救。
直接转录调控: CREB1通过直接结合到多个细胞外基质相关基因(如 Col1a1, Fn1, Acta2 等)的启动子区域,上调其转录。
证据:染色质免疫共沉淀和荧光素酶报告基因实验均证实了CREB1对这些基因启动子的直接结合和激活作用。
体内功能验证:
在体内肿瘤模型中,敲低CAFs中的CREB1,能够有效逆转感觉神经元激活(或CGRP信号)所导致的:
肿瘤生长加速。
肿瘤促纤维化(胶原沉积)。
免疫排斥性微环境的形成。
结论:
研究完整揭示了 “CGRP-RAMP1 → cAMP/PKA → CREB1磷酸化 → ECM基因转录激活 → 胶原合成与沉积” 的信号传导轴。CREB1作为该通路的枢纽转录因子,直接连接了神经信号与肿瘤基质的重构。靶向此通路(如抑制CGRP、RAMP1或CREB1)可破坏致密胶原基质的形成,为逆转免疫排斥性肿瘤微环境提供了具体的分子靶点。
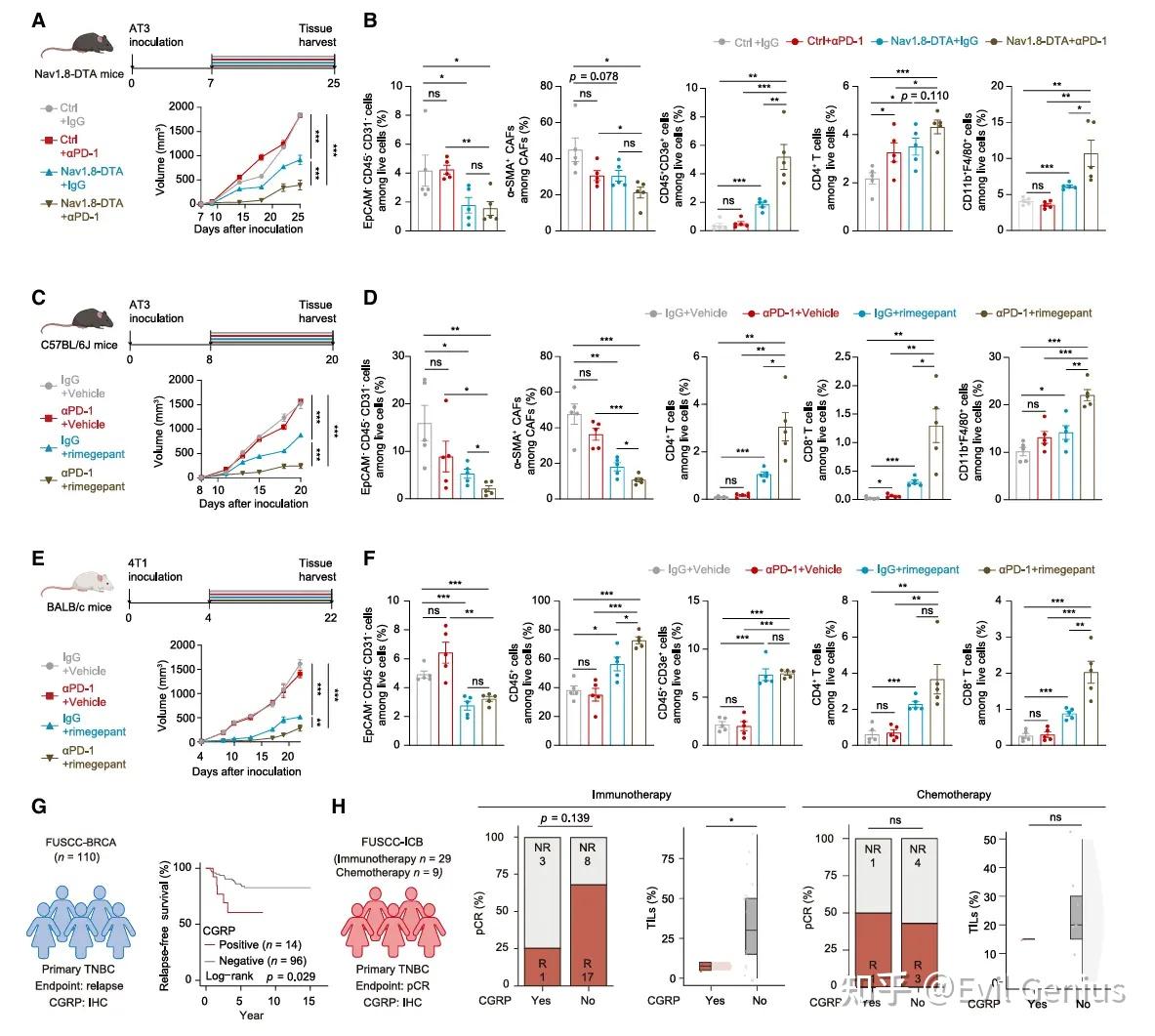
结果7、靶向感觉神经元与免疫检查点阻断在三阴性乳腺癌中产生协同作用
CGRP抑制剂与抗PD-1治疗的联合可能是一种优化的免疫治疗策略。CGRP是三阴性乳腺癌患者预后和免疫治疗疗效预测的一个有前景的生物标志物。
最后来看看方法

生活很好,有你更好。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
评论
登录后参与评论
推荐阅读
目录

