昌平实验室打造PPIFlow:AI 流匹配算法驱动的高亲和力蛋白结合剂设计
昌平实验室打造PPIFlow:AI 流匹配算法驱动的高亲和力蛋白结合剂设计

DrugIntel
发布于 2026-01-29 13:05:23
发布于 2026-01-29 13:05:23

在蛋白质工程与治疗性生物药研发领域,高亲和力蛋白结合剂的从头设计一直是制约技术转化的核心瓶颈。传统方法依赖实验筛选与体外maturation,不仅成本高昂、周期漫长,还难以精准控制结合表位与分子构象。昌平实验室团队开发的PPIFlow框架,通过流匹配生成模型与新型体外maturation策略的深度融合,实现了无需实验优化即可直接生成皮摩尔(pM)至纳摩尔(nM)级亲和力结合剂的突破,为蛋白结合剂设计提供了新的纯计算解决方案。相关研究成果以《High-Affinity Protein Binder Design via Flow Matching and In Silico Maturation》为题于bioRxiv预印本发布,其技术创新性与应用潜力值得深入剖析。
一、领域痛点与技术背景
蛋白质-蛋白质相互作用(PPIs)是细胞生理功能的核心基础,也是肿瘤、自身免疫病等疾病的关键治疗靶点。理想的蛋白结合剂需同时满足高亲和力(pM/nM级)、精准靶向(特定表位)与结构稳定三大核心要求,但长期以来面临双重技术瓶颈:
- 计算设计与实际亲和力并非强相关:现有深度学习模型(如RFdiffusion、BindCraft)虽能生成结构合理的蛋白骨架,但因难以捕捉精准的几何互补性与侧链堆积效应,生成的结合剂亲和力为中等水平,需依赖大规模实验筛选优化;
- 体外maturation效率低下:传统定向进化、文库筛选等方法资源消耗大,且难以实现对结合界面的精细调控,限制了候选分子的成药潜力;
- 抗体设计难度更高:单域抗体(VHHs)等治疗性抗体需兼顾抗原结合特异性与框架稳定性,从头设计的成功率与亲和力达标率一直处于较低水平。
流匹配(Flow Matching)技术的出现为解决上述问题提供了新的可能。流匹配通过学习简单分布与复杂结构间的连续映射,具备训练稳定性强、采样效率高的优势,能够更精准地建模蛋白质骨架的刚体变换过程。PPIFlow框架正是基于这一技术,结合体外maturation策略与高效筛选工具,构建了从骨架生成到亲和力优化的全流程计算设计体系。
二、PPIFlow框架的核心技术创新
PPIFlow的突破性在于将流匹配生成模型、靶向体外maturation与高效结构评分三大模块深度协同,形成了闭环设计流程,其核心技术创新可概括为以下三点:
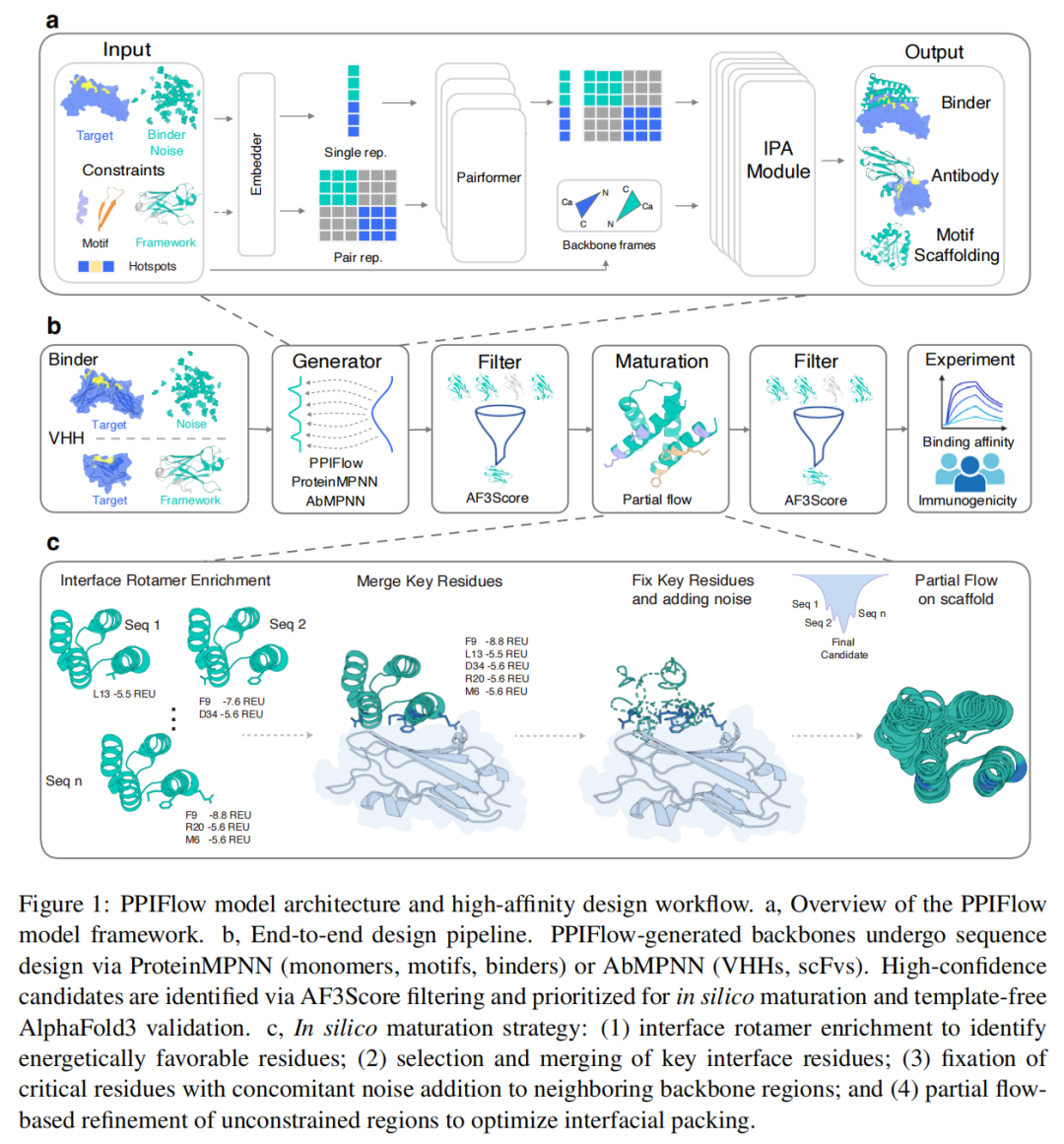
1. 流匹配驱动的精准骨架生成
PPIFlow采用SE(3)空间刚体流建模,将蛋白质骨架表示为刚性残基框架集合,通过学习平移与旋转场,直接实现从随机分布到真实结构的连续转化。
- Pairformer模块:通过interleaved attention与transition层,联合更新残基级与成对嵌入特征,明确捕捉结合界面的几何关系与化学相互作用,缓解了传统模型难以建模长程残基相互作用的问题;
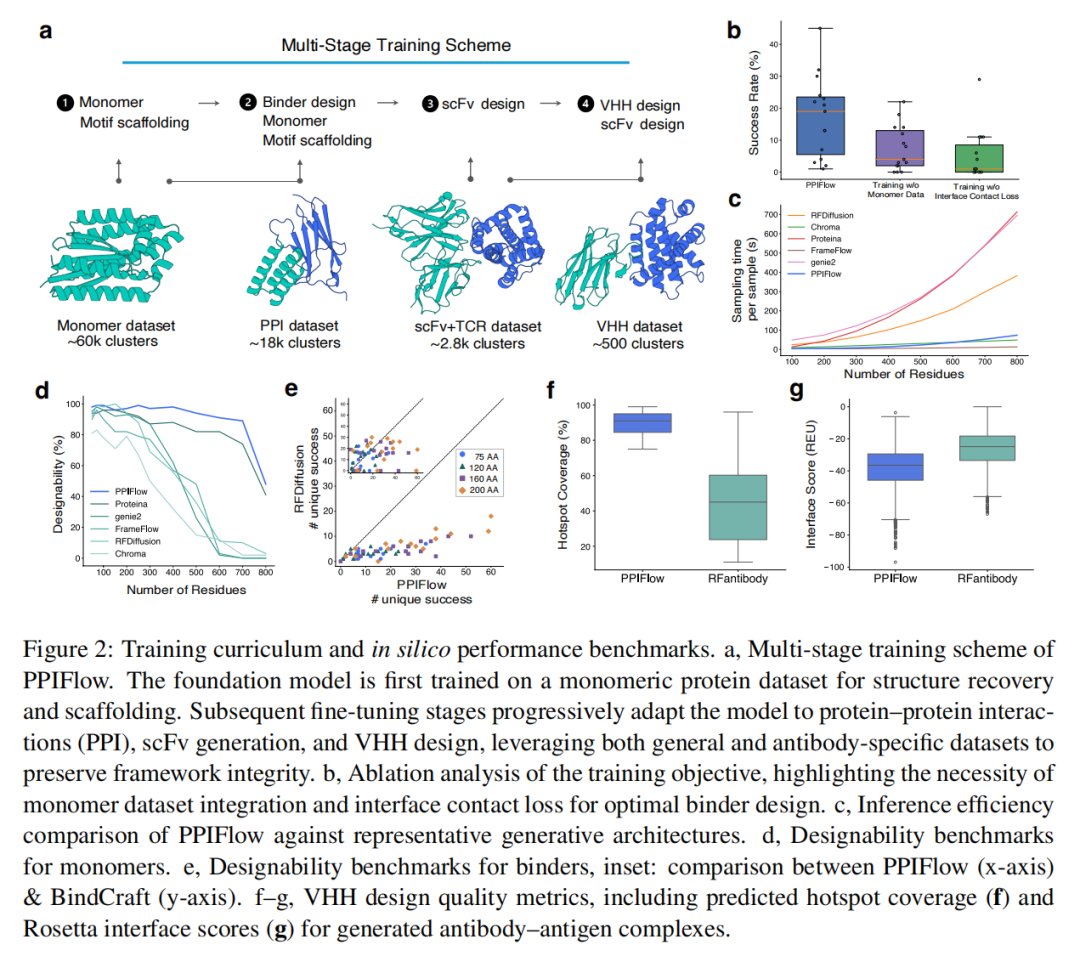
- 多阶段训练策略:模型先在单体蛋白数据集上学习通用结构先验,再逐步微调至蛋白质-蛋白质相互作用(PPI)、单链可变片段(scFv)与VHH设计任务,有效避免灾难性遗忘,提升了复杂场景下的泛化能力;
- 几何约束增强:引入界面接触损失、骨架原子损失与结合剂成对距离损失,确保生成的骨架结构具备物理合理性与靶向结合潜力。
2. 新型体外maturation策略:从 结构合理 到 高亲和力 的跨越
为弥补计算设计与实际亲和力的差距,PPIFlow开发了包含四大步骤的体外maturation流程,实现结合界面的精准优化:
- 界面旋转异构体富集:通过Rosetta能量计算,筛选出相互作用能量<-5 Rosetta能量单位(REU)的“锚定残基”,识别能量最优的侧链构象;
- 关键残基融合:合并多序列设计中贡献显著的关键界面残基,构建富集型界面;
- 骨架扰动与再生:固定关键残基,将剩余骨架扰动至中间流状态(t=0.6),通过流匹配模型再生扰动区域,解决空间冲突并重塑结合界面;
- 序列重设计:采用ProteinMPNN(通用结合剂)或AbMPNN(VHHs)在低温度(T=0.1)下重设计非约束区域,提升序列-结构兼容性与折叠稳定性。
3. AF3Score:高效精准的候选分子筛选工具
为解决传统筛选方法计算成本高、效率低的问题,PPIFlow集成了AlphaFold3的简化评分工具AF3Score,无需构建多序列比对(MSA)与迭代循环,即可快速评估候选分子的结构置信度与结合潜力。
- 计算效率提升约两个数量级,大幅缩短候选分子优先级排序时间;
- 采用复合评分标准(AF3 ipTM×100 - Rosetta界面评分),结合AlphaFold3结构验证与Rosetta界面分析,确保筛选出的候选分子兼具结构稳定性与结合特异性。
三、实验验证:全面超越现有技术的性能表现
研究团队在15个治疗相关靶标上对PPIFlow进行了严格验证,涵盖7个微型结合剂靶标(IL7RA、IFNAR2、IL17A等)与8个VHH靶标(CCL2、HNMT、PDGFR等),实验结果展现出三大核心优势:
1. 超高亲和力与成功率
- mini-结合剂:210个候选分子全部成功表达,36.2%(76个)的结合剂亲和力优于1μM,其中6个靶标获得pM级结合剂,最优亲和力达1pM(TRKA_05、IL7RA_02);
- VHHs:240个候选分子表达成功率100%,33.8%(81个)实现特异性结合,27.9%(67个)亲和力优于1μM,CCL2靶向VHH(CCL2_21)亲和力达250pM,PDGFR、1433E等靶标获得单-digit nM级结合剂;
- 表位精准性:VHH设计的热点覆盖度中位数>0.9,框架一致性误差(RMSD)仅0.18Å,确保了结合特异性与成药潜力。
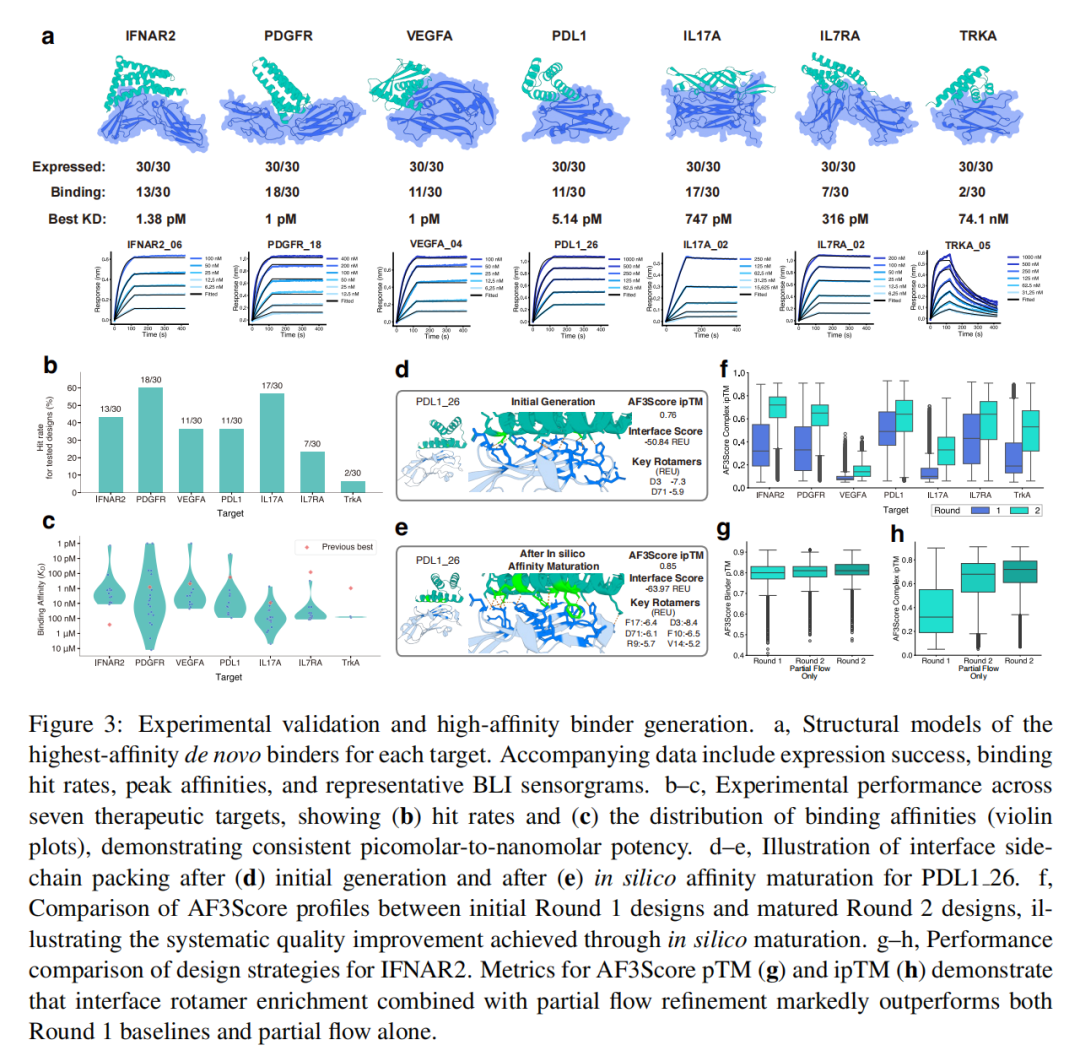
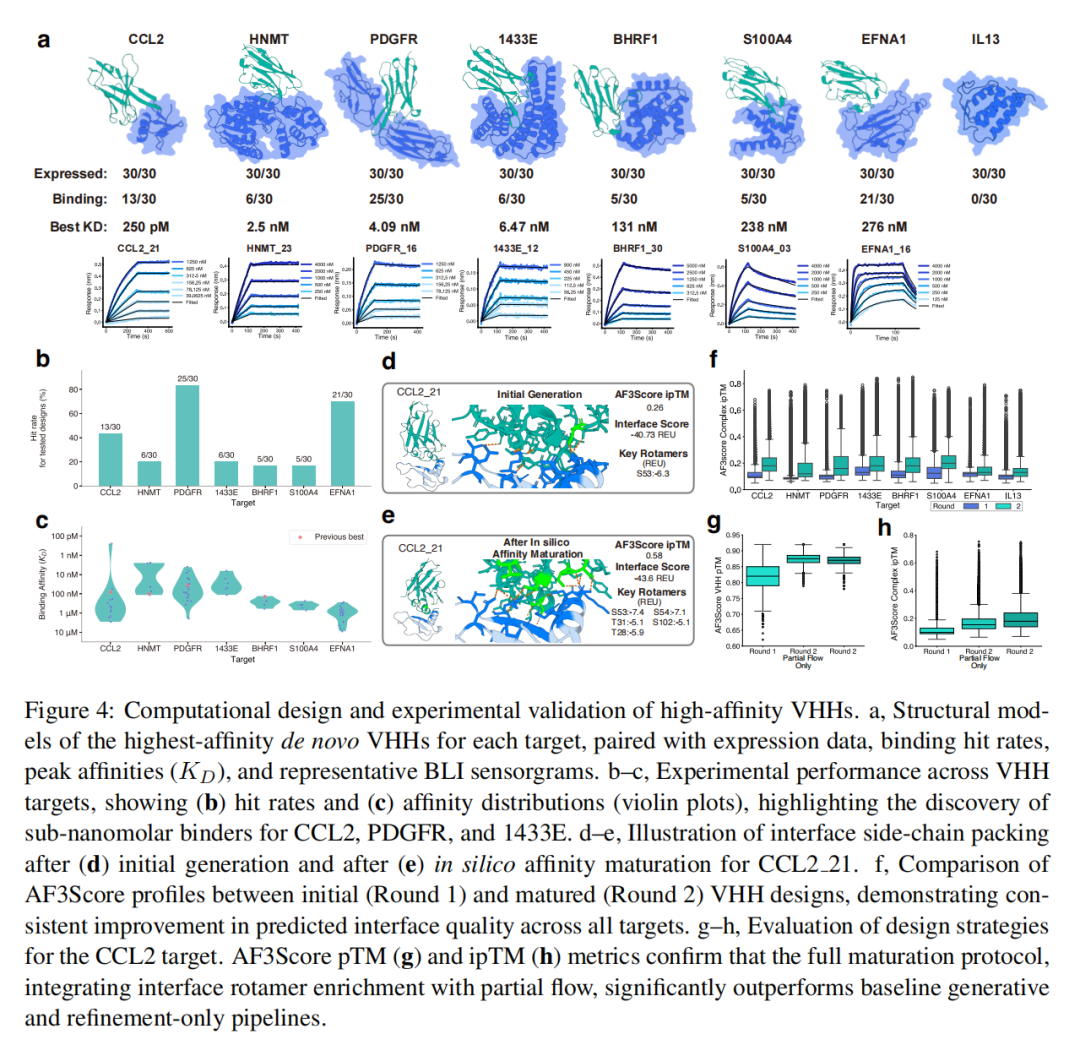
2. 优于现有方法的综合性能
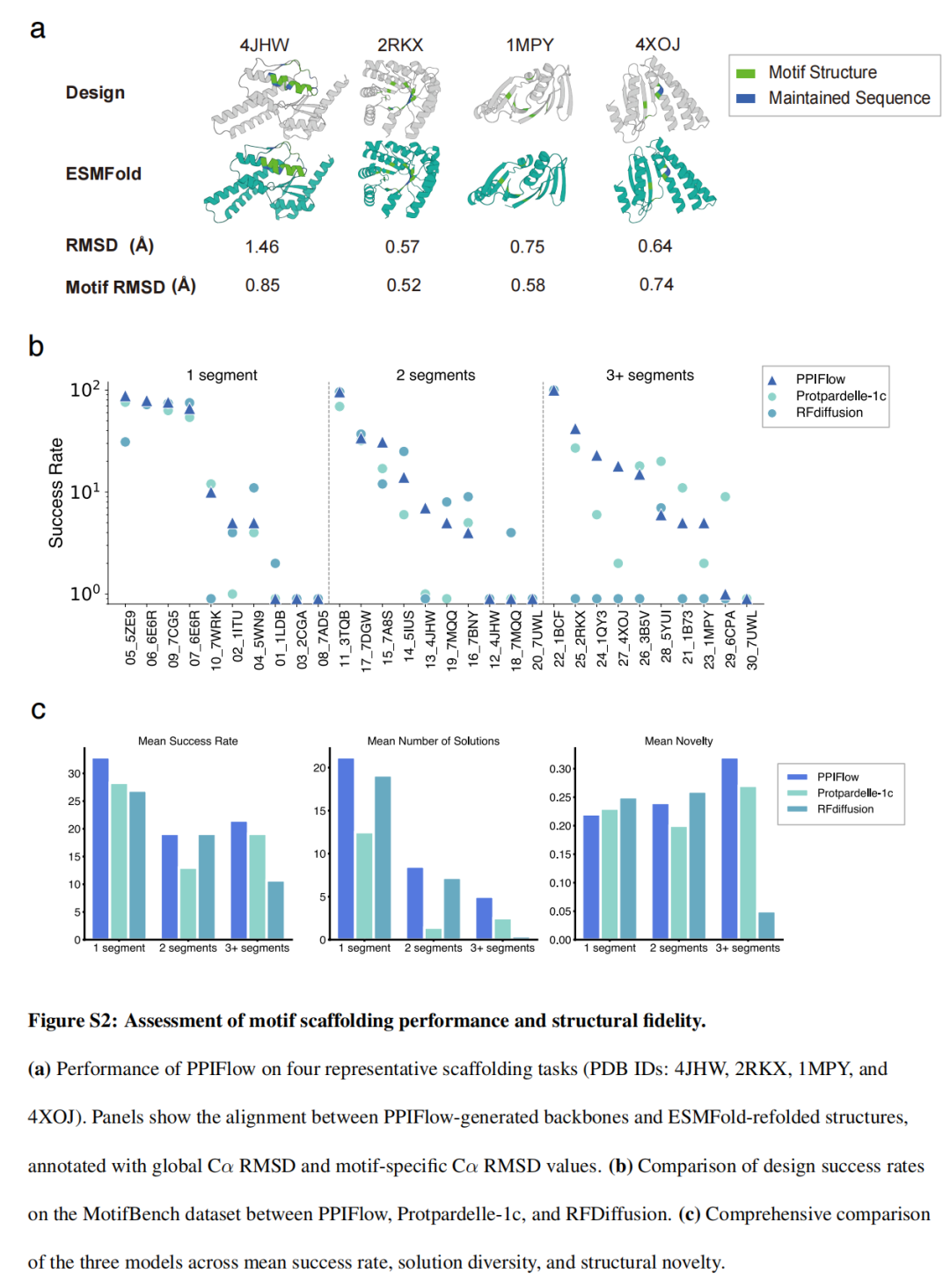
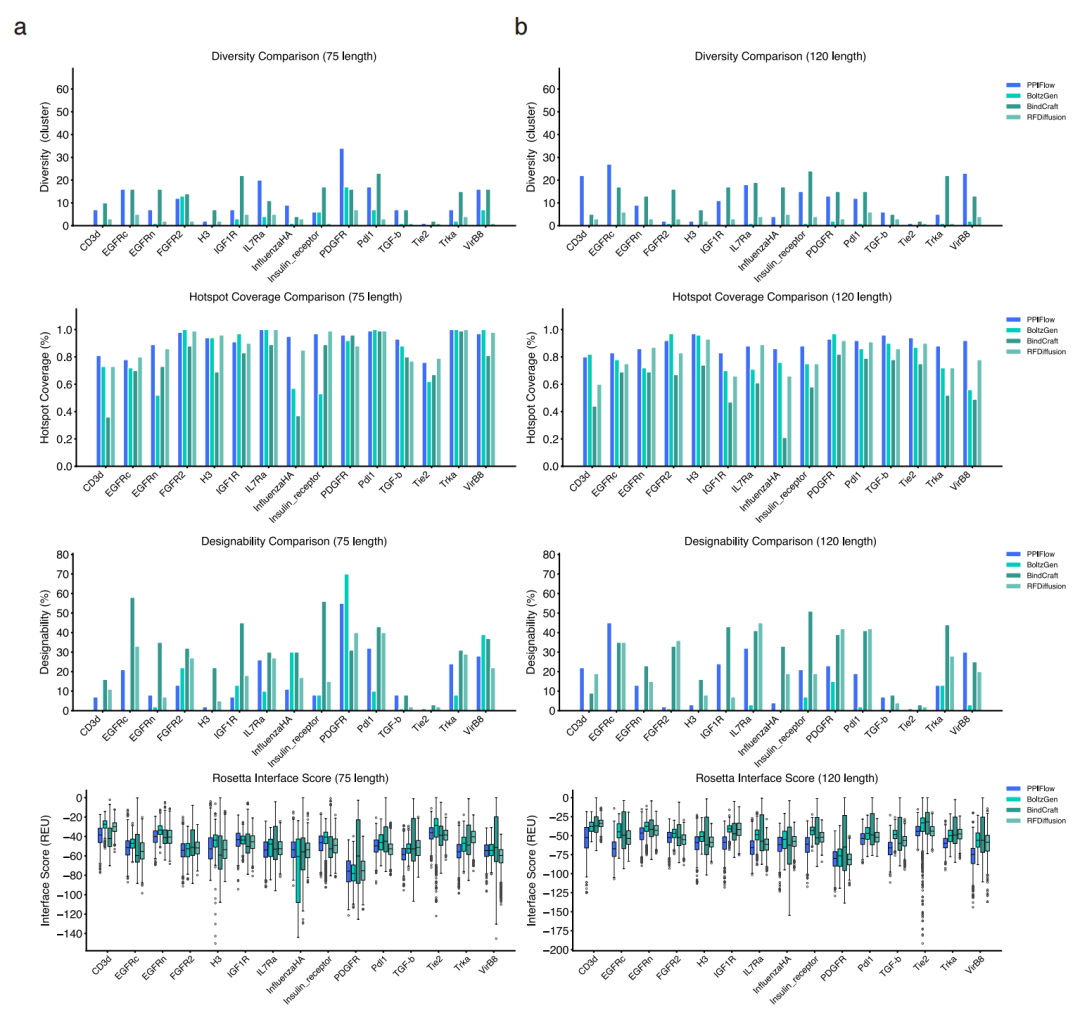
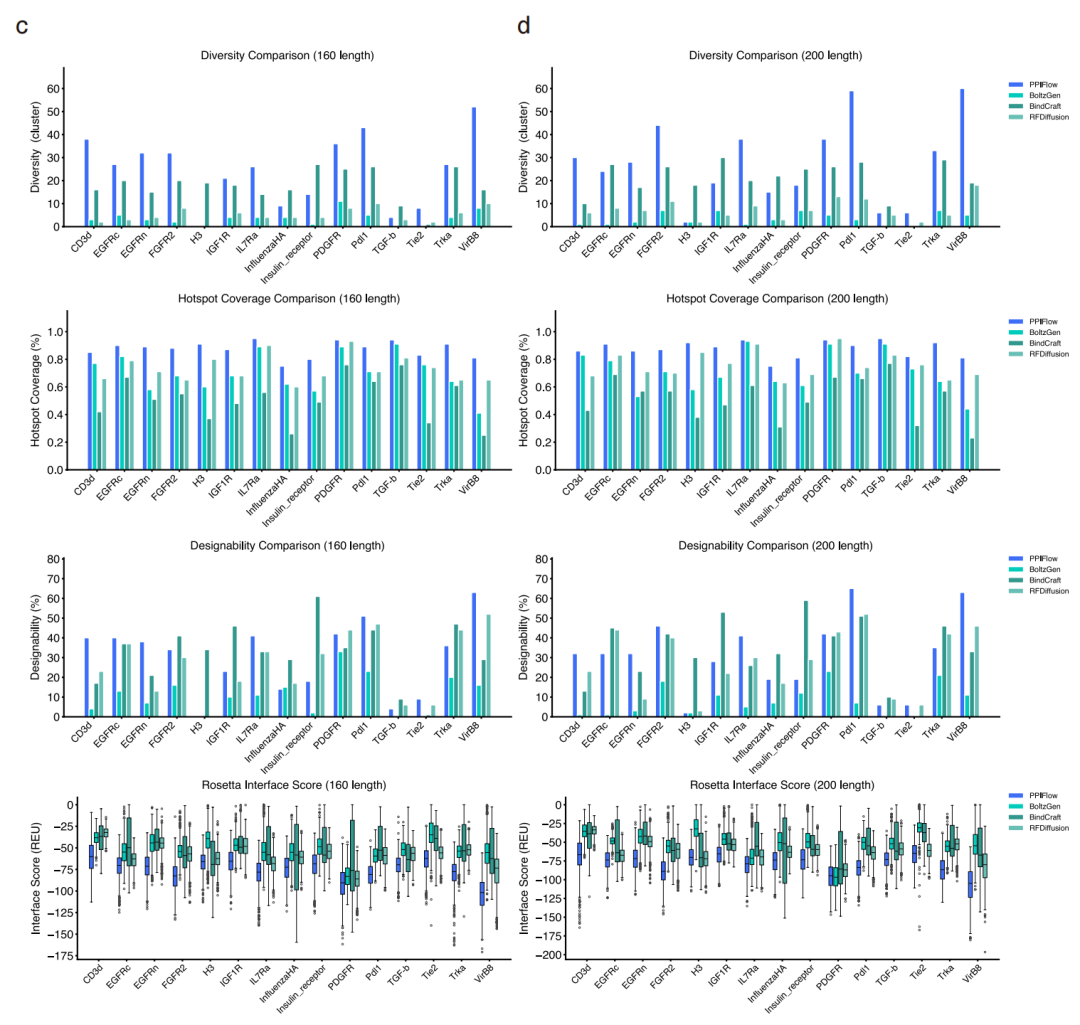
在MotifBench基准测试中,PPIFlow得分为42.38,远超RFdiffusion的28.6,成功缓解了4JHW、4XOJ等多片段 motif 支架搭建难题;在75-200残基长度的结合剂设计中,其结构多样性、设计成功率与界面能量评分均全面超越RFdiffusion、BindCraft与BoltzGen等主流工具,尤其在大尺寸结合剂设计中优势更为突出。

四、局限性与未来展望
尽管PPIFlow展现出卓越性能,但仍存在一些局限性:
- 目前仅支持骨架生成,侧链堆积需后续处理,全原子生成框架可能进一步提升复杂界面的设计效果;
- 针对部分靶标(如IL13)的成功率较低,主要原因是难以识别稳定的 锚定残基,限制了体外maturation的效果;
- 仅适用于蛋白质-蛋白质复合物设计,尚未拓展至核酸、小分子等其他靶点类型。
未来,团队计划通过开发全原子流匹配模型、优化低成功率靶标的锚定残基识别算法、拓展多靶点类型支持等方向,进一步提升框架的通用性与性能。此外,PPIFlow的代码与数据已开源(https://github.com/Mingchenchen/PPIFlow),将为全球科研人员提供免费可用的技术支撑。
六、总结
PPIFlow框架通过流匹配生成模型、新型体外maturation策略与高效筛选工具的深度融合,成功实现了高亲和力蛋白结合剂的纯计算从头设计,其在实验验证中展现的高成功率、超高亲和力与计算效率。
参考文献:Qilin Yu, Liangyue Guo, Xiayan Qin, Xikun Huang, Baihui Tian, Hongzhun Wang, Yu Liu, Yunzhi Lang, Di Wang, Zhouhanyu Shen, Jie Lin, Mingchen Chen, High-Affinity Protein Binder Design via Flow Matching and In Silico Maturation, bioRxiv 2026.01.19.700484
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-01-28,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读
目录

