Briefings Bioinf. | CMOMO:约束条件下多属性分子优化的突破性框架
Briefings Bioinf. | CMOMO:约束条件下多属性分子优化的突破性框架

MindDance
发布于 2026-01-08 12:57:49
发布于 2026-01-08 12:57:49
CMOMO: a deep multi-objective optimization framework for constrained molecular multi-property optimization
期刊: Briefings in Bioinformatics 链接: https://doi.org/10.1093/bib/bbaf335 代码: https://github.com/ahu-bioinf-lab/CMOMO-master 简介: 该论文提出了 CMOMO,一种深度多目标优化框架,旨在解决受约束的分子多属性优化问题,其创新点在于通过动态约束处理策略平衡多属性优化与约束满足,并设计了基于潜在向量碎片化的进化繁殖策略以有效生成有前景的分子。CMOMO 将优化过程分为无约束和有约束两个阶段,在无约束阶段专注于提升分子属性,在有约束阶段采用排名聚合策略平衡属性与约束。实验在两个基准任务和两个实际任务(4LDE 蛋白配体优化、GSK3β 抑制剂优化)上进行,使用了从公共数据库筛选的数据集,结果显示 CMOMO 在优化成功率、超体积等指标上均优于五种现有方法,能生成更多满足类药约束且属性优良的分子。该论文证明了 CMOMO 在分子优化中的优越性,为药物研发提供了高效工具。

在现代药物发现领域,分子优化面临着一个核心挑战:如何在庞大的化学空间中精准识别出既满足多重类药约束,又具备优异多属性的分子。近期发表于《Briefings in Bioinformatics》的研究论文提出了一种创新性的深度多目标优化框架——CMOMO,为这一难题提供了系统性解决方案。
一、研究背景:分子优化的核心矛盾与现有方法局限
分子优化作为药物研发的关键环节,其本质是在复杂化学空间中进行多目标探索。理想情况下,优化后的分子需同时满足:提升多种生物活性与理化性质,且符合严苛的类药约束(如环结构尺寸、毒性亚结构排除等)。然而,现有方法普遍存在难以调和的矛盾:
- • 单属性优化的局限性:早期方法多聚焦单一属性(如QED或PlogP),但药物研发实际需要同步优化多种协同属性,单目标优化往往导致"顾此失彼"。
- • 多属性优化的权重困境:部分方法(如QMO、Molfinder)通过权重聚合将多属性转化为单目标,但权重参数的微小变化会显著影响结果,且无法体现属性间的权衡关系。
- • 约束处理的简单化:现有约束处理策略存在明显缺陷——MSO将约束与属性简单聚合导致参数调优困难,GB-GA-P通过直接丢弃 infeasible molecules牺牲了潜在优质分子的进化潜力,这些方法均无法实现属性优化与约束满足的动态平衡。
特别需要强调的是,类药约束(如环原子数限制为5-6个)并非可优化的目标函数,而是必须满足的硬性条件,这使得分子优化问题本质上属于约束多目标优化问题,其可行域往往呈现狭窄、离散、不规则的特征,传统方法在此类空间中探索效率极低。
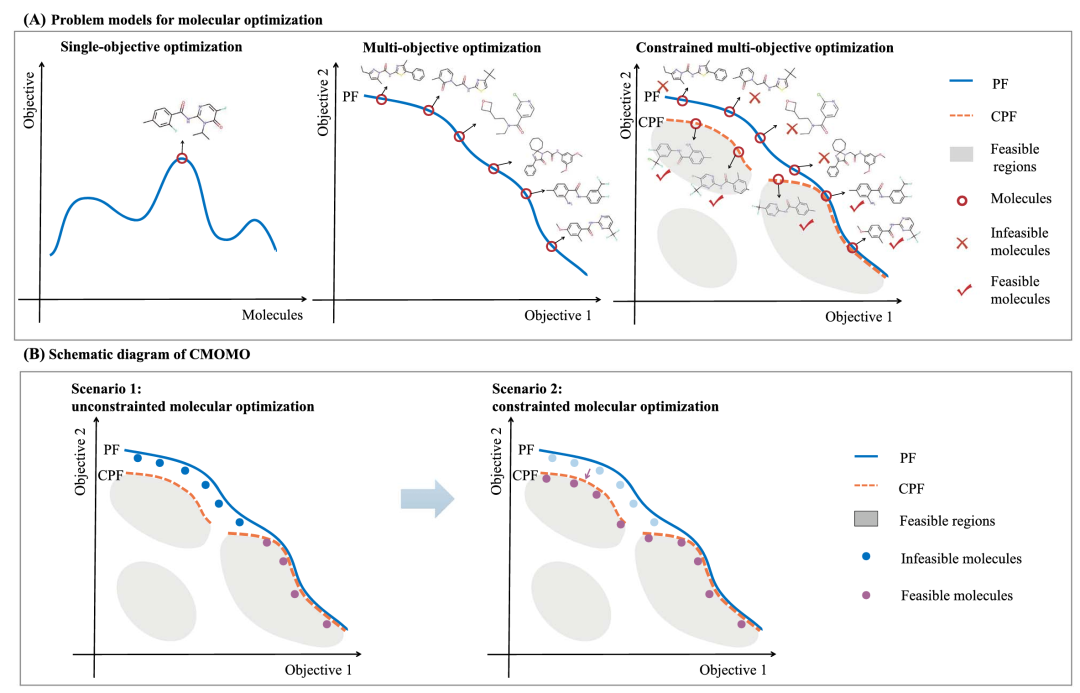
分子优化的三种问题模型及 CMOMO 的示意图。(A)单目标优化旨在找到具有最佳目标值的分子;多目标优化旨在搜索帕累托前沿(PF)上一组在多个属性间权衡的分子;约束多目标优化旨在识别约束帕累托前沿(CPF)上一组在多个属性间权衡且满足类药约束的分子。(B)CMOMO 框架的优化过程,CMOMO 首先专注于属性优化以找到位于 PF 上的分子,然后发现位于 CPF 上的分子以解决约束多目标分子优化问题。
分子优化的三种问题模型及 CMOMO 的示意图。(A)单目标优化旨在找到具有最佳目标值的分子;多目标优化旨在搜索帕累托前沿(PF)上一组在多个属性间权衡的分子;约束多目标优化旨在识别约束帕累托前沿(CPF)上一组在多个属性间权衡且满足类药约束的分子。(B)CMOMO 框架的优化过程,CMOMO 首先专注于属性优化以找到位于 PF 上的分子,然后发现位于 CPF 上的分子以解决约束多目标分子优化问题。
二、CMOMO框架设计:动态协同优化的创新范式
CMOMO(Constrained Multi-Objective Molecular Optimization)框架的核心创新在于将深度生成模型与进化算法相结合,通过两阶段动态优化策略实现属性提升与约束满足的精准平衡。其架构设计体现了对分子优化问题本质的深刻理解:
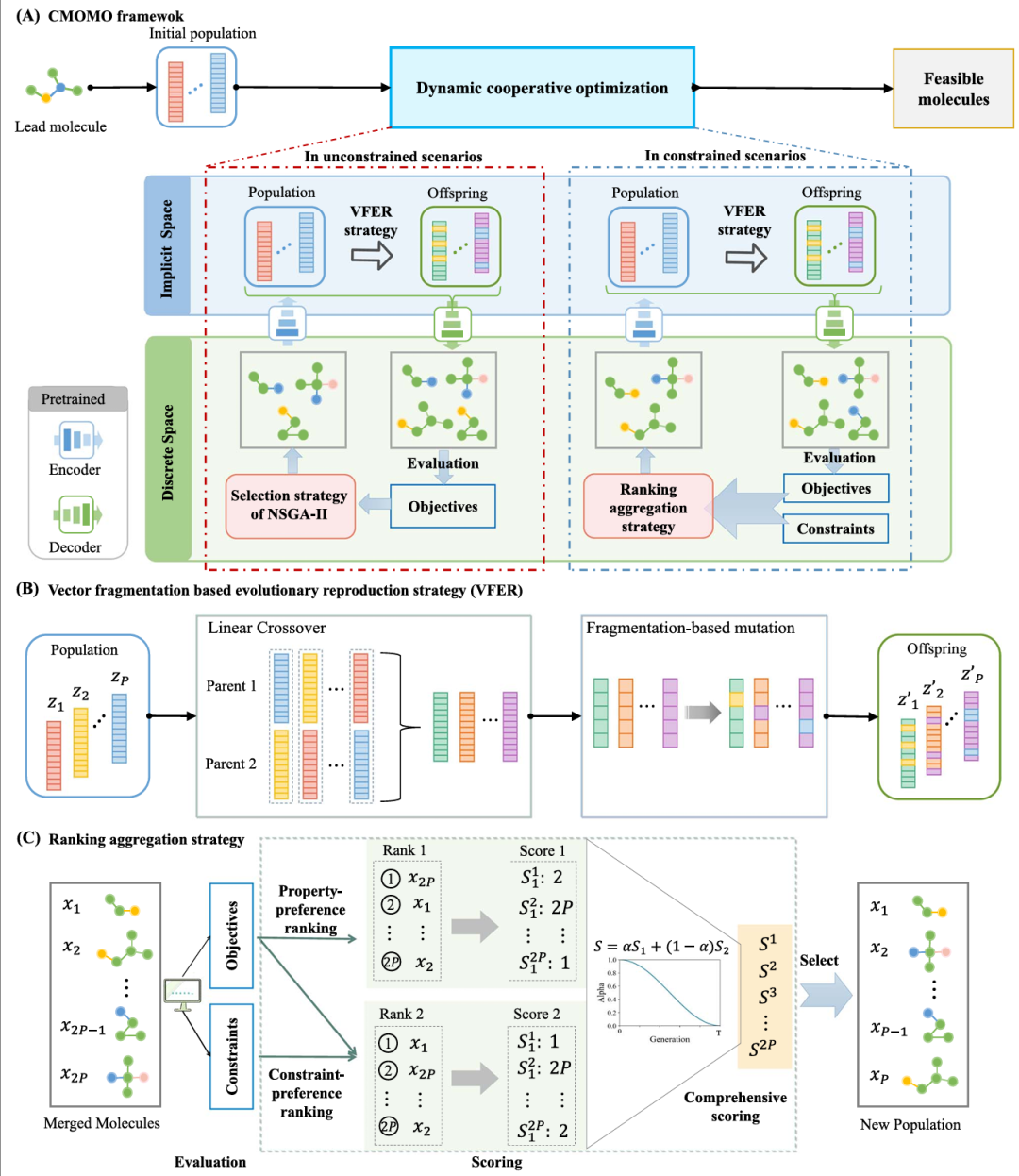
CMOMO 的说明图。(A)CMOMO 首先为先导分子生成包含 P 个分子的初始种群,然后执行动态协同优化,最终得到一组可行分子(具有理想的分子属性且符合类药约束)。(B)VFER 策略,该策略通过线性交叉和基于碎片化的突变操作生成有前景的子代分子。(C)排名聚合策略,该策略动态聚合分别按属性和约束排序的分子排名。
CMOMO 的说明图。(A)CMOMO 首先为先导分子生成包含 P 个分子的初始种群,然后执行动态协同优化,最终得到一组可行分子(具有理想的分子属性且符合类药约束)。(B)VFER 策略,该策略通过线性交叉和基于碎片化的突变操作生成有前景的子代分子。(C)排名聚合策略,该策略动态聚合分别按属性和约束排序的分子排名。
1. 两阶段动态约束处理策略
CMOMO将优化过程划分为递进式的两个场景,通过策略切换实现全局探索与局部精准优化的有机统一:
- • 场景一:无约束多属性优化
首先利用预训练的encoder-decoder将分子映射至连续隐空间,采用NSGA-II的环境选择策略筛选具有优异属性的分子群体。此阶段不考虑约束条件,目的是快速挖掘化学空间中属性潜力较高的区域,为后续优化奠定基础。该阶段通过线性交叉操作融合先导分子与Bank库中高属性分子的 latent vectors,生成高质量初始种群,解决了传统方法初始探索效率低下的问题。
- • 场景二:约束条件下的平衡优化
引入创新的排名聚合策略(Ranking Aggregation Strategy),通过三个关键步骤实现属性与约束的动态平衡:
- • 属性偏好排序:仅基于分子属性进行NSGA-II排序
- • 约束偏好排序:结合属性与约束违反度(CV)进行支配排序(可行分子优先于不可行分子,同状态下属性更优或CV更低者排序更前)
- • 综合评分:通过余弦衰减参数α动态融合两种排序结果(α从1逐渐衰减至0,实现从属性优先到约束优先的平滑过渡)
这种设计巧妙解决了约束多目标优化中"过度关注约束导致属性退化"或"忽视约束导致结果无效"的两难问题,其动态调整机制与分子进化的内在规律高度契合。
2. 潜在向量碎片化进化繁殖策略(VFER)
作为CMOMO的核心组件,VFER(Vector Fragmentation-based Evolutionary Reproduction)策略针对高维隐空间优化的挑战,设计了创新性的进化操作:
- • 线性交叉:基于混合线性交叉算子生成子代 latent vectors,公式如下: 其中d控制搜索空间的插值/外推范围,u1、u2为[0,1]区间随机数,该操作有效融合了父代分子的优质"基因"。
- • 碎片化突变:将 latent vector分割为若干片段,随机选择片段进行整体突变。这种策略显著降低了高维空间中的"维度灾难"影响,避免了传统多项式突变易陷入局部最优的缺陷,实验证明其对CMOMO性能的贡献最为关键。
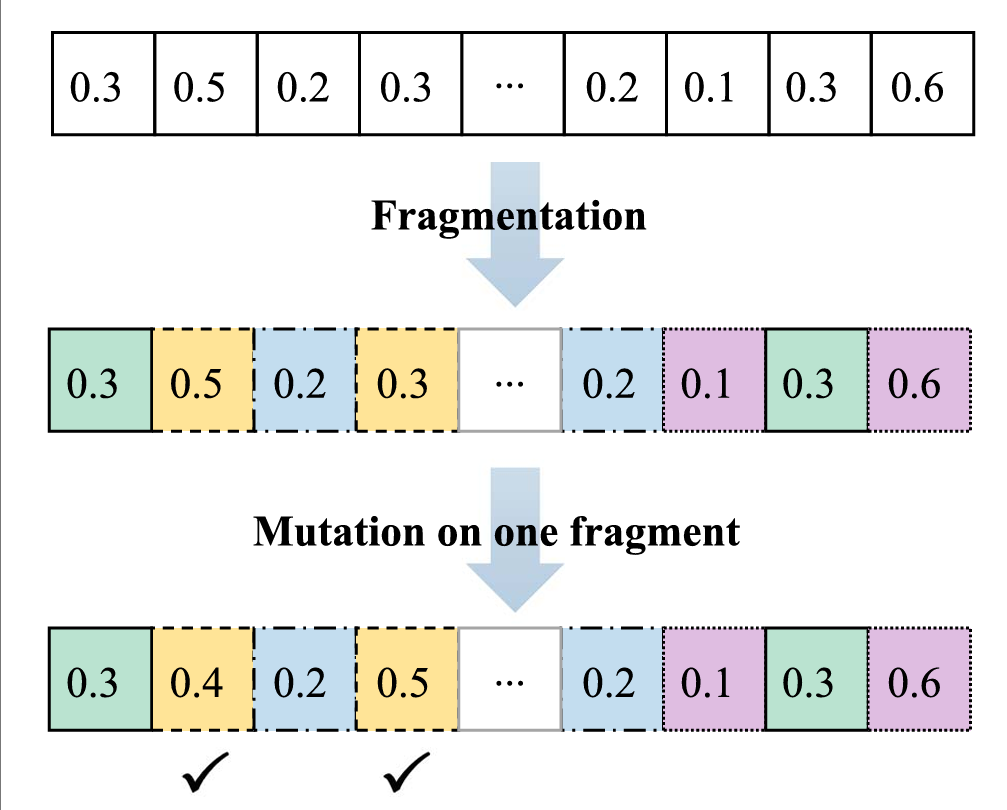
所提出的基于碎片化的突变算子的示例。
所提出的基于碎片化的突变算子的示例。
3. 约束违反度量化方法
CMOMO采用标准化的约束违反度(CV)评估分子可行性:
其中σ₁衡量环结构约束违反度(小环或大环的原子数偏差总和),σ₂量化毒性亚结构的出现次数。这种标准化处理解决了不同约束间量纲差异的问题,使CV值具有跨约束的可比性。
三、实验验证:全面超越现有方法的性能表现
CMOMO在两类基准任务与两类实际药物研发任务中均展现出显著优势,其性能提升并非偶然,而是源于架构设计的科学性:
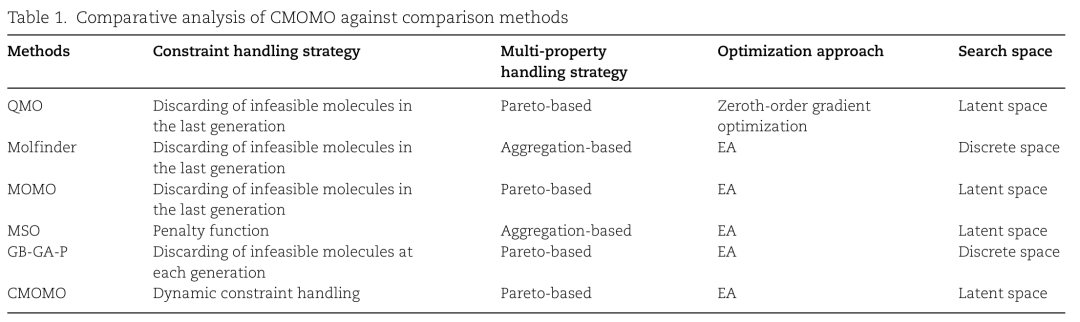
CMOMO 与对比方法的比较分析,从约束处理策略、多属性处理策略、优化方法、搜索空间四个维度进行对比。
CMOMO 与对比方法的比较分析,从约束处理策略、多属性处理策略、优化方法、搜索空间四个维度进行对比。
1. 基准任务:多维度指标全面领先
在优化QED(药物相似性)、PlogP_imp(脂水分配系数改进量)和Similarity(与先导分子相似性)的Task 1中:
- • CMOMO的优化成功率(SR)达到94.8%,远超QMO(68.4%)、MOMO(52.0%)等对比方法;
- • 成功优化分子的HV值(衡量收敛性与多样性的综合指标)为0.226,是Molfinder(0.057)的4倍以上;
- • 每个先导分子对应的成功优化分子数量显著多于对比方法,证明其探索化学空间的广度优势。
在基于Perindopril结构优化的Task 2中,CMOMO同样在SR(70.9%)、HV(0.243)等指标上保持领先,验证了其在不同分子体系中的稳定性。
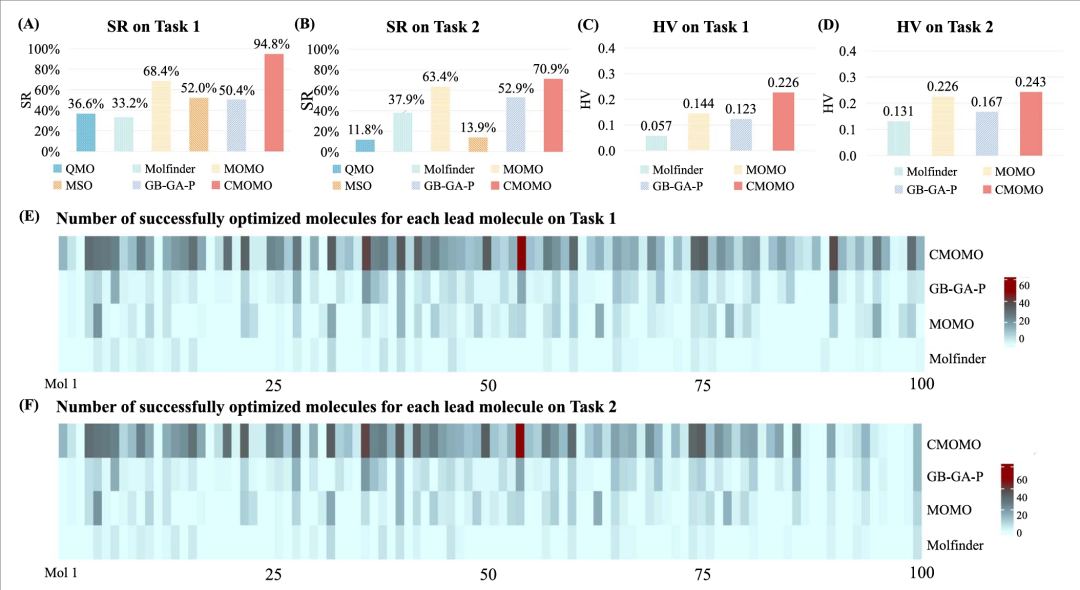
CMOMO 和对比方法在两个基准约束多目标优化任务上的性能。(A)CMOMO 和对比方法在任务 1 上的成功率(SR);(B)CMOMO 和对比方法在任务 2 上的成功率;(C)CMOMO 和三种帕累托优化方法在任务 1 上的超体积(HV);(D)CMOMO 和三种帕累托优化方法在任务 2 上的超体积;(E)四种多目标优化方法在任务 1 上每个先导分子的成功优化分子数量;(F)四种多目标优化方法在任务 2 上每个先导分子的成功优化分子数量。
CMOMO 和对比方法在两个基准约束多目标优化任务上的性能。(A)CMOMO 和对比方法在任务 1 上的成功率(SR);(B)CMOMO 和对比方法在任务 2 上的成功率;(C)CMOMO 和三种帕累托优化方法在任务 1 上的超体积(HV);(D)CMOMO 和三种帕累托优化方法在任务 2 上的超体积;(E)四种多目标优化方法在任务 1 上每个先导分子的成功优化分子数量;(F)四种多目标优化方法在任务 2 上每个先导分子的成功优化分子数量。
2. 实际应用任务:解决药物研发痛点
- • 4LDE蛋白配体优化(β2-肾上腺素受体,与肌肉松弛和支气管扩张相关): CMOMO的SR达75%,显著高于次优方法的59%;优化分子与4LDE的对接能均低于-7 kcal/mol(药物活性阈值),且形成4-2个关键疏水相互作用,验证了其实际生物活性潜力。
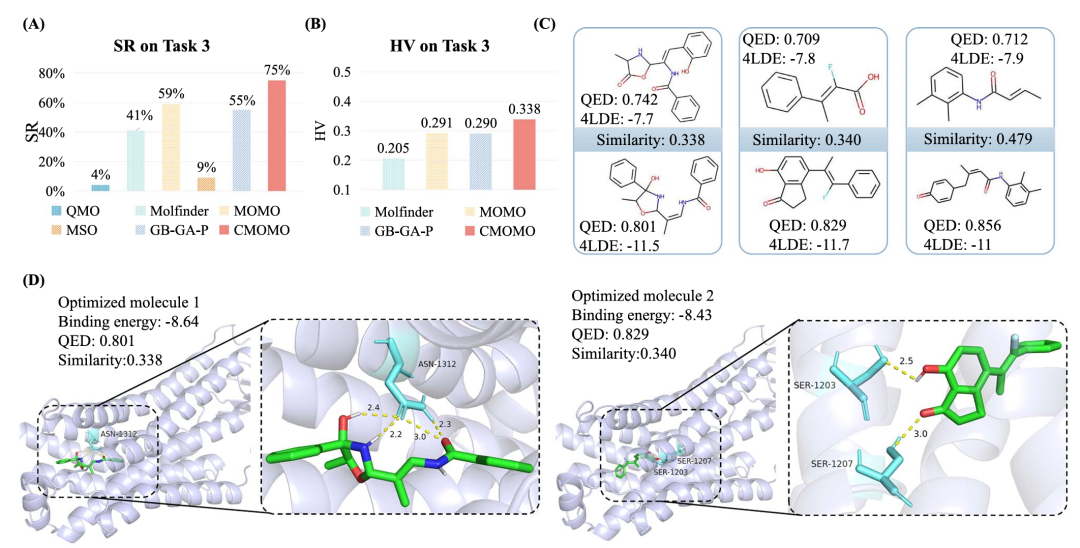
CMOMO 和对比方法在任务 3 上的性能。(A)CMOMO 和对比方法在任务 3 上的成功率;(B)CMOMO 和三种帕累托优化方法在任务 3 上的超体积;(C)CMOMO 在五个测试实例上的优化结果,上下两行分别表示先导分子和优化分子;(D)展示了两个针对 4LDE 蛋白的优化分子的对接构象、QED、结合能和相似性,两个分子均表现出理想的 QED、结合能和相似性,右侧两个子图展示了优化分子与蛋白质结合口袋中氨基酸残基的相互作用。
CMOMO 和对比方法在任务 3 上的性能。(A)CMOMO 和对比方法在任务 3 上的成功率;(B)CMOMO 和三种帕累托优化方法在任务 3 上的超体积;(C)CMOMO 在五个测试实例上的优化结果,上下两行分别表示先导分子和优化分子;(D)展示了两个针对 4LDE 蛋白的优化分子的对接构象、QED、结合能和相似性,两个分子均表现出理想的 QED、结合能和相似性,右侧两个子图展示了优化分子与蛋白质结合口袋中氨基酸残基的相互作用。
- • GSK3β抑制剂优化(与阿尔茨海默病相关的靶点): 成功率达52.7%,是对比方法(最高24.6%)的两倍以上;优化分子同时具备高QED(药物相似性)、高GSK3β抑制活性和高SA(合成可及性),解决了传统方法难以兼顾多属性的难题。特别值得注意的是,其优化分子的结合能低至-7.86 kcal/mol,具备成为候选药物的潜力。
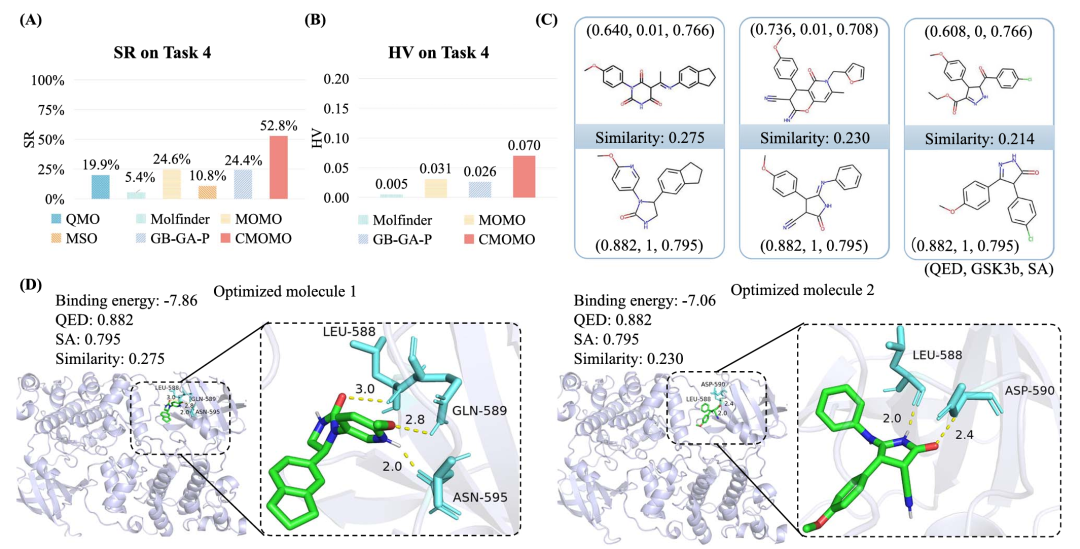
CMOMO 和对比方法在任务 4 上的性能。(A)任务 4 上的成功率;(B)任务 4 上的超体积;(C)优化结果示例,包含相似性等信息;(D)两个优化分子的结合能等信息,以及与蛋白质结合口袋中氨基酸残基的相互作用。
CMOMO 和对比方法在任务 4 上的性能。(A)任务 4 上的成功率;(B)任务 4 上的超体积;(C)优化结果示例,包含相似性等信息;(D)两个优化分子的结合能等信息,以及与蛋白质结合口袋中氨基酸残基的相互作用。
3. 组件有效性验证:VFER策略的核心作用
消融实验(Ablation Study)表明:
- • 移除VFER策略的CMOMO_novfer在SR、HV和关键属性值上均显著下降,证明碎片化进化繁殖是提升性能的核心引擎;
- • 移除Bank库的CMOMO_nobank导致初始种群质量下降,间接影响后续优化;
- • 移除排名聚合策略的CMOMO_noagg无法平衡属性与约束,导致可行域探索效率降低。
这一结果揭示了各组件的协同作用机制:Bank库奠定初始质量基础,排名聚合策略实现平衡优化,而VFER策略则是驱动进化过程的核心动力。
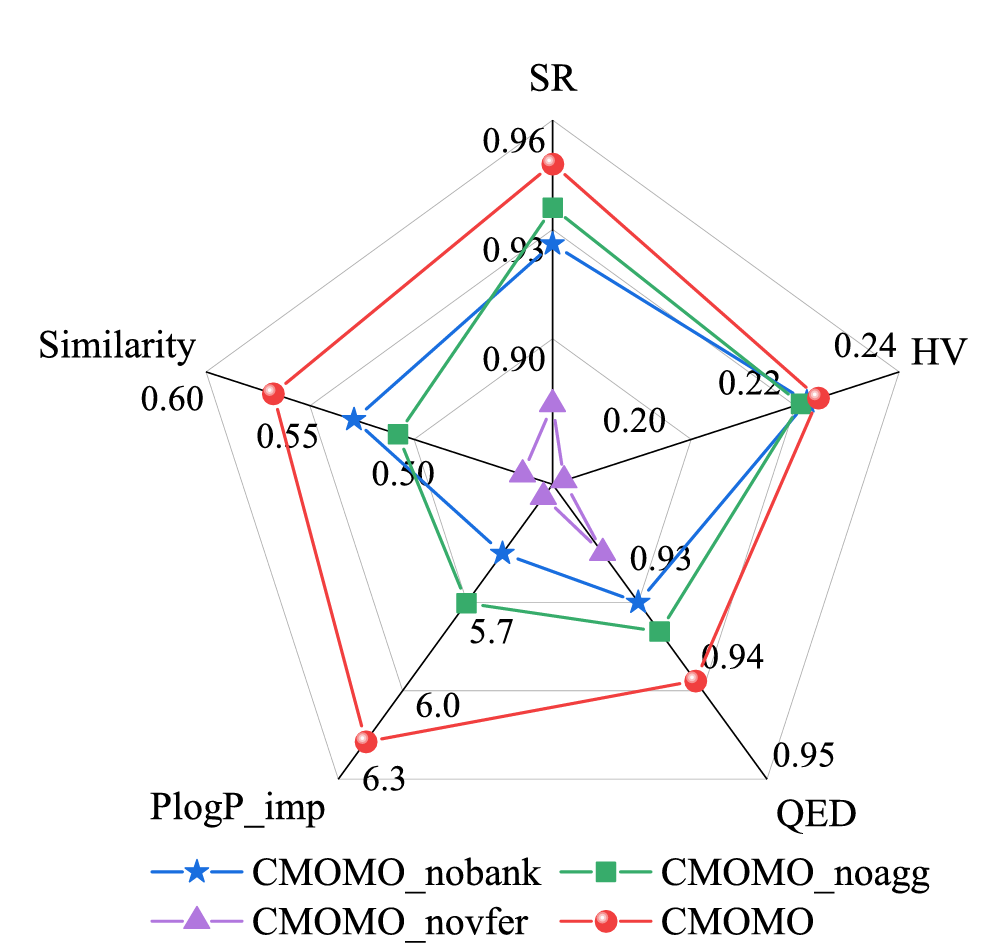
CMOMO 及其三个变体在任务 1 上的性能,展示了成功率、超体积以及 QED、PlogP_imp、相似性这三个属性值的对比。
CMOMO 及其三个变体在任务 1 上的性能,展示了成功率、超体积以及 QED、PlogP_imp、相似性这三个属性值的对比。
四、进化路径分析:CMOMO如何探索化学空间?
通过追踪分子从先导结构到优化产物的进化轨迹,可深入理解CMOMO的工作机制:
- • 多路径进化:单个先导分子可通过不同修饰路径(如局部环结构调整、侧链优化等)生成多样化的优化分子,这些分子在QED、PlogP等属性上形成互补的权衡关系,体现了其挖掘化学空间多样性的能力。
- • 不可行分子的利用:进化过程中保留部分低CV的不可行分子,使其通过后续突变转化为可行分子,这种策略避免了优质分子的过早淘汰,提升了全局探索能力。
- • 结构修饰的精准性:Tanimoto相似性图谱显示,优化分子在保留先导分子核心结构(蓝色区域)的同时,对非关键区域(红色区域)进行针对性修饰,实现了"保留优势、改进缺陷"的精准优化。
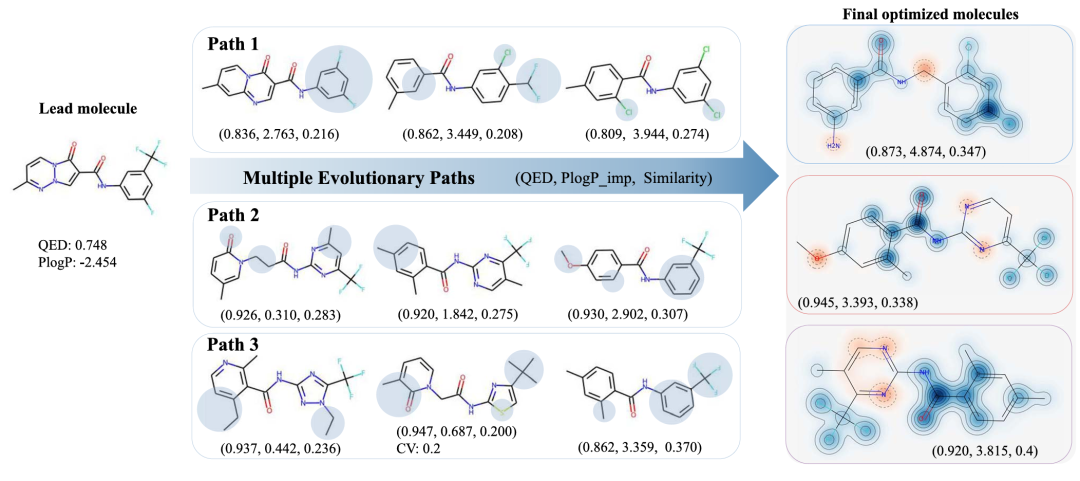
CMOMO 针对一个随机选择的先导分子的优化分子形成的多条进化路径。图中三行展示了从先导分子到最终优化分子的进化路径,每行中的阴影区域突出显示了修饰的亚结构,最后一列的三个塔尼莫相似性图展示了最终优化分子,其中与先导分子相似和不相似的区域分别用蓝色和红色表示。
CMOMO 针对一个随机选择的先导分子的优化分子形成的多条进化路径。图中三行展示了从先导分子到最终优化分子的进化路径,每行中的阴影区域突出显示了修饰的亚结构,最后一列的三个塔尼莫相似性图展示了最终优化分子,其中与先导分子相似和不相似的区域分别用蓝色和红色表示。
五、总结与展望:药物研发的高效工具
CMOMO框架的提出为约束条件下的多属性分子优化提供了全新范式,其核心价值体现在:
- 1. 理论创新:将分子优化问题精准建模为约束多目标优化问题,通过动态约束处理策略突破了传统方法的固有局限;
- 2. 方法创新:VFER策略解决了高维隐空间进化效率低下的问题,排名聚合策略实现了属性与约束的平滑平衡;
- 3. 应用价值:在实际药物靶点(4LDE、GSK3β)优化中展现出成为候选药物的潜力,为加速药物研发提供了实用工具。
未来,CMOMO有望在肽类、蛋白质等其他类型药物优化中拓展应用,并可通过整合更多类型的约束条件(如合成可行性、代谢稳定性)进一步提升其实用价值。对于药物研发从业者而言,这一框架不仅提供了更高效的分子优化工具,更启发了我们从约束多目标优化的视角重新审视药物发现过程中的核心问题。
(●'◡'●) 需要进一步讨论的同学欢迎留言交流!
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2025-07-17,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读
目录

