Nat. Chem. | 通过强化氢键作用实现超稳定蛋白的计算设计
Nat. Chem. | 通过强化氢键作用实现超稳定蛋白的计算设计

DrugAI
发布于 2026-01-06 14:07:18
发布于 2026-01-06 14:07:18
DRUGONE
蛋白质在极端机械拉伸和高温环境下往往容易失稳,而自然界中某些结构蛋白却能在严苛条件下保持稳定,其核心在于高度协同的氢键网络。研究人员提出一种以最大化主链氢键为核心原则的蛋白计算设计策略,通过人工智能辅助结构与序列设计,并结合分子动力学筛选,成功从头设计出一系列“超稳定”蛋白。这些蛋白在机械强度和热稳定性上显著超越天然对照结构,并可进一步构建在宏观尺度上依然稳定的蛋白材料,为极端环境下功能蛋白与生物材料设计提供了新路径。

氢键是稳定蛋白质结构的基本化学作用,尤其在 β 折叠中,多个氢键的协同断裂能够显著提升对外力和高温的抵抗能力。自然界中,肌联蛋白、丝素蛋白和某些细菌黏附复合物均利用这种“剪切式”氢键加载方式,实现异常高的机械稳定性。
然而,传统蛋白工程方法通常只能通过点突变或局部修饰获得有限的稳定性提升,难以系统性地构建大规模氢键网络。随着人工智能驱动的蛋白结构生成和序列设计工具日趋成熟,研究人员开始探索:能否将自然界中已知的稳定性化学原理,转化为可规模化应用的计算设计策略?
方法概述
研究人员以肌联蛋白的免疫球蛋白结构域为模板,构建了一套**“AI 设计 + 分子动力学筛选”**的一体化计算流程。该流程首先固定关键受力 β 链作为核心结构单元,利用生成式模型扩展蛋白骨架,从而系统性增加主链氢键数量;随后通过序列设计模型生成可折叠序列,并使用高精度结构预测和多轮分子动力学模拟,筛选同时具备高机械强度和高热稳定性的候选蛋白。最终设计出的蛋白被实验验证其稳定性表现。
结果
从天然模板到超稳定设计的整体流程
研究人员逐步延长蛋白中承受拉伸的 β 链长度,使主链氢键数量由天然结构中的个位数,增加至数十个。这一结构扩展策略显著改变了受力几何方式,使氢键在外力作用下协同断裂,而非逐个解离。
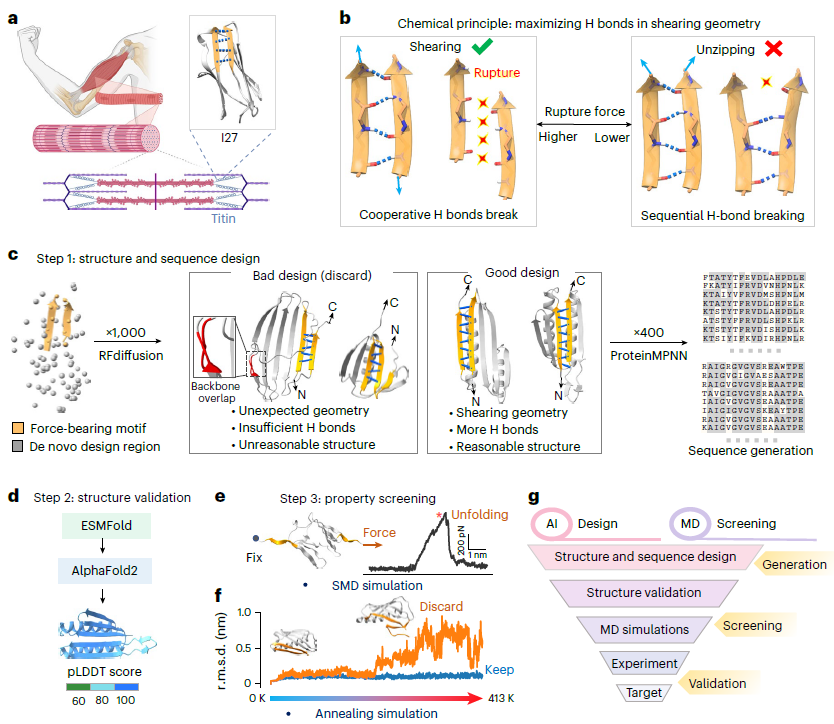
图 1|超稳定蛋白的计算设计流程与总体策略。
氢键数量与机械稳定性的线性增强关系
实验与模拟结果一致表明,蛋白的机械展开力与主链氢键数量呈显著正相关。随着氢键网络不断扩大,设计蛋白的抗拉伸能力提升至纳牛顿量级,远高于天然对照蛋白。
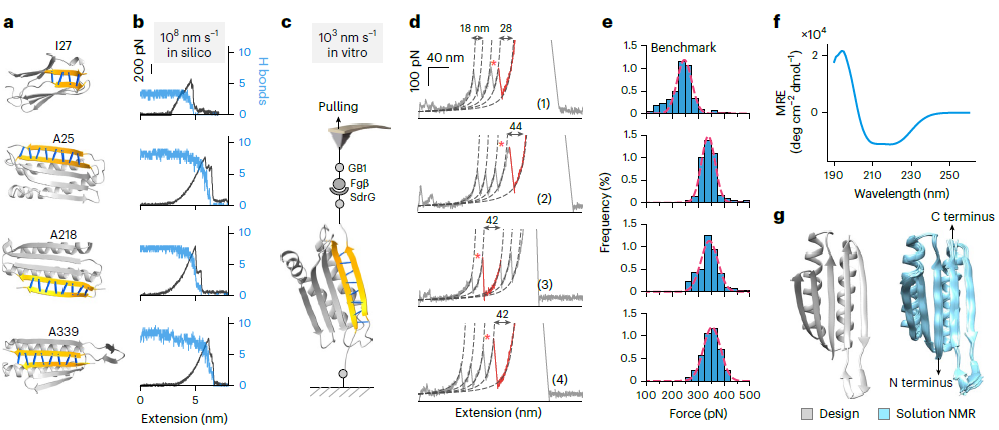
图 2|主链氢键数量与蛋白机械展开强度的关系。
极端热稳定性的获得
除机械稳定性外,这些设计蛋白在高温条件下依然保持结构完整。部分蛋白在远高于常规蛋白耐受温度的条件下仍能维持折叠状态,显示出卓越的热稳定性。
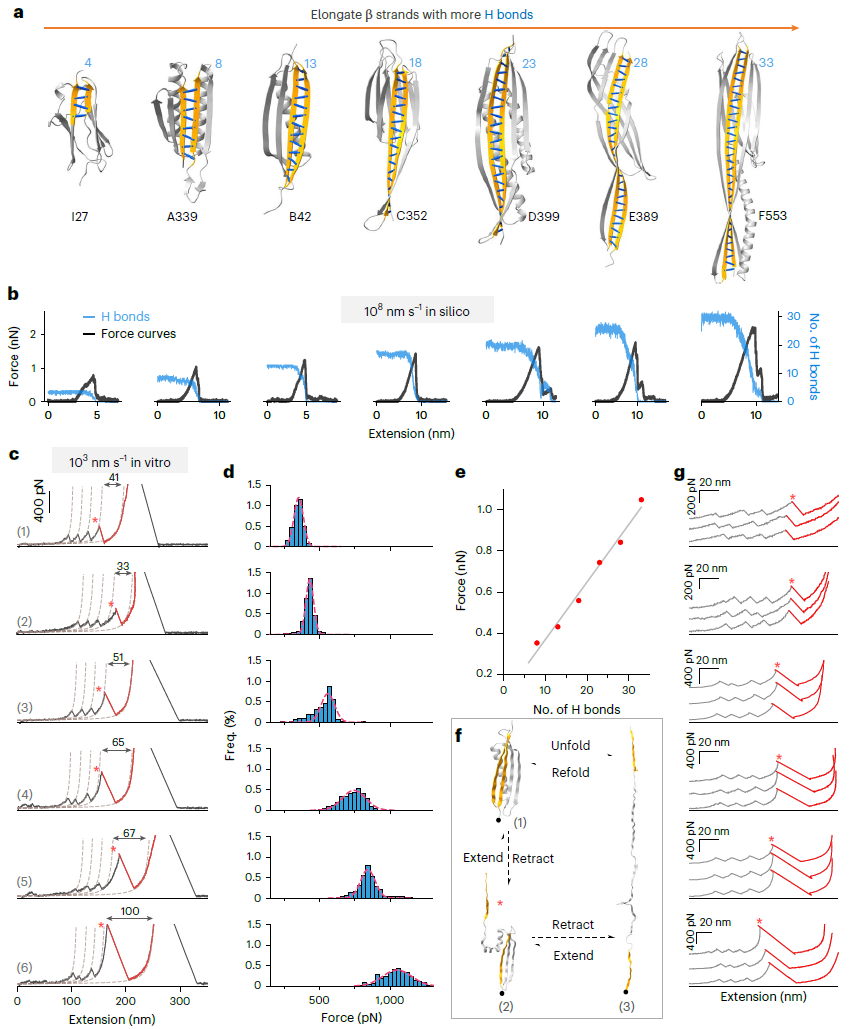
图 3|设计蛋白在高温条件下的结构稳定性评估。
从分子稳定性到宏观材料性能
研究人员进一步将超稳定蛋白作为物理交联单元,构建蛋白水凝胶材料。结果显示,这些材料在高温灭菌等严苛处理后仍能保持完整结构,证明分子层面的稳定性提升可直接转化为宏观材料性能。
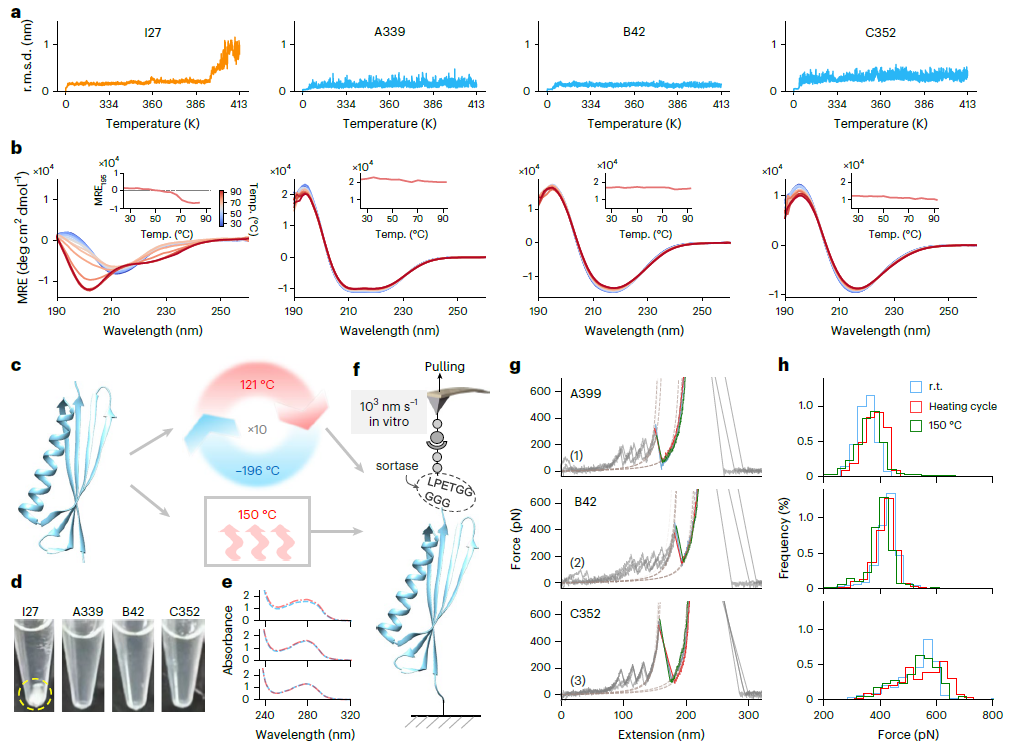
图 4|基于超稳定蛋白构建的耐高温蛋白水凝胶。
稳定性设计原则的可扩展性
系统性分析表明,该设计策略并非依赖特定序列,而是源于氢键网络与受力几何的通用化学原理,具备向更多蛋白体系推广的潜力。
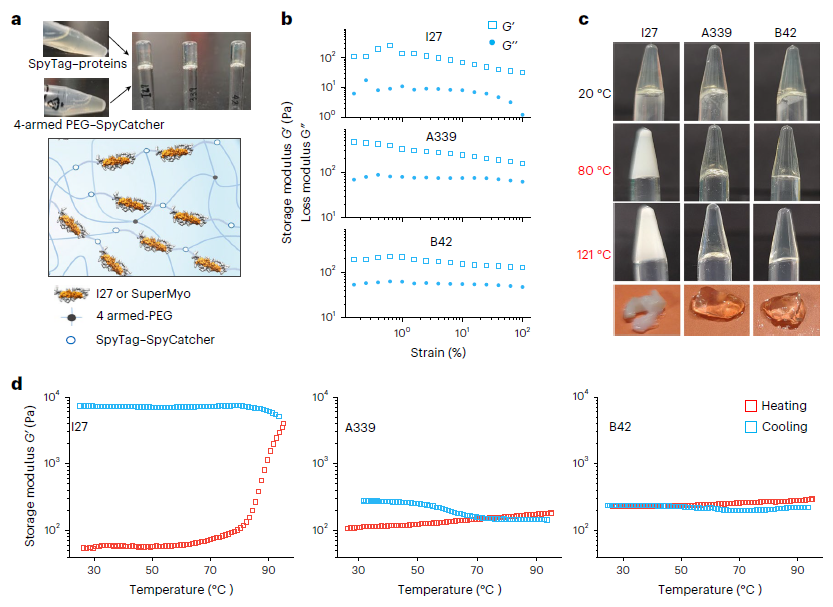
图 5|不同设计系列中稳定性提升的整体趋势
讨论
这项研究表明,通过将明确的化学稳定性原则嵌入人工智能驱动的蛋白设计流程,可以突破传统蛋白工程在稳定性提升上的上限。研究人员不仅在分子尺度上实现了接近自然极限的机械与热稳定性,还展示了这种增强如何在材料尺度上产生实际效应。
更重要的是,该工作提供了一种可推广的范式:**以物理化学原理为核心约束,结合生成式模型与高通量计算筛选,实现真正“可控”的蛋白从头设计。**这一思路有望推动面向极端环境、生物材料和合成生物学应用的下一代蛋白设计研究。
整理 | DrugOne团队
参考资料
Zheng, B., Lu, Z., Wang, S. et al. Computational design of superstable proteins through maximized hydrogen bonding. Nat. Chem. (2025).
https://doi.org/10.1038/s41557-025-01998-3
内容为【DrugOne】公众号原创|转载请注明来源
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2025-12-14,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

