Nat. Commun. | 基于深度学习的空间组学与肿瘤形态多尺度整合
Nat. Commun. | 基于深度学习的空间组学与肿瘤形态多尺度整合

DrugAI
发布于 2026-01-06 13:57:16
发布于 2026-01-06 13:57:16
DRUGONE
空间转录组学为理解肿瘤微环境结构、肿瘤发生与进展提供了前所未有的空间信息,但其高成本与技术壁垒限制了临床使用。与之相比,H&E 染色切片在临床中普遍可得。研究人员提出 MISO,一种基于深度学习的框架,能够从 H&E 预测空间转录组表达,并通过多尺度注意力机制捕获局部组织结构特征。在 72 个 Visium 样本上训练后,MISO 在多个基准中显著优于现有方法,并能生成近单细胞分辨率的空间基因表达图。研究人员进一步在 348 个多癌种样本验证了其稳健性,展示了 MISO 在跨癌种泛化中的优势。

传统转录组技术无法保留组织空间结构,从而掩盖了稀有细胞群及其相互作用的重要信号。虽然 Visium、Xenium 等空间组学技术提供空间信息,但其高成本、有限可用性与测序深度限制阻碍了临床推广。
H&E 切片作为肿瘤诊断的基础资料,蕴含丰富的形态学特征。近年来的深度学习研究已显示:高分辨率病理图像能够预测突变、分子表型甚至 bulk 级别的基因表达。
然而已有模型存在关键限制:
- 多数仅使用 tile 级图像信息,不捕获邻域空间结构
- 可用的空间组学数据有限,导致模型泛化差
- 现有方法难以从 H&E 中推断接近“单细胞”尺度的表达模式
为此,研究人员提出 MISO,以多尺度深度学习整合空间形态学与组学信号。
方法
MISO 以整个 H&E 切片的 tiles 作为输入,通过 Vision Transformer 提取 patch-level 特征,并使用 局部自注意力(Local Attention Multiple Instance Learning) 建模组织邻域结构。
训练时采用基于余弦相似度的损失,减少不同样本之间测序深度差异的影响。研究人员还提出使用理论上限指标筛选具有可预测性的基因,并通过知识蒸馏实现近单细胞的超分辨率表达预测。训练好的 MISO 推理时只需 H&E 切片即可生成空间表达图。
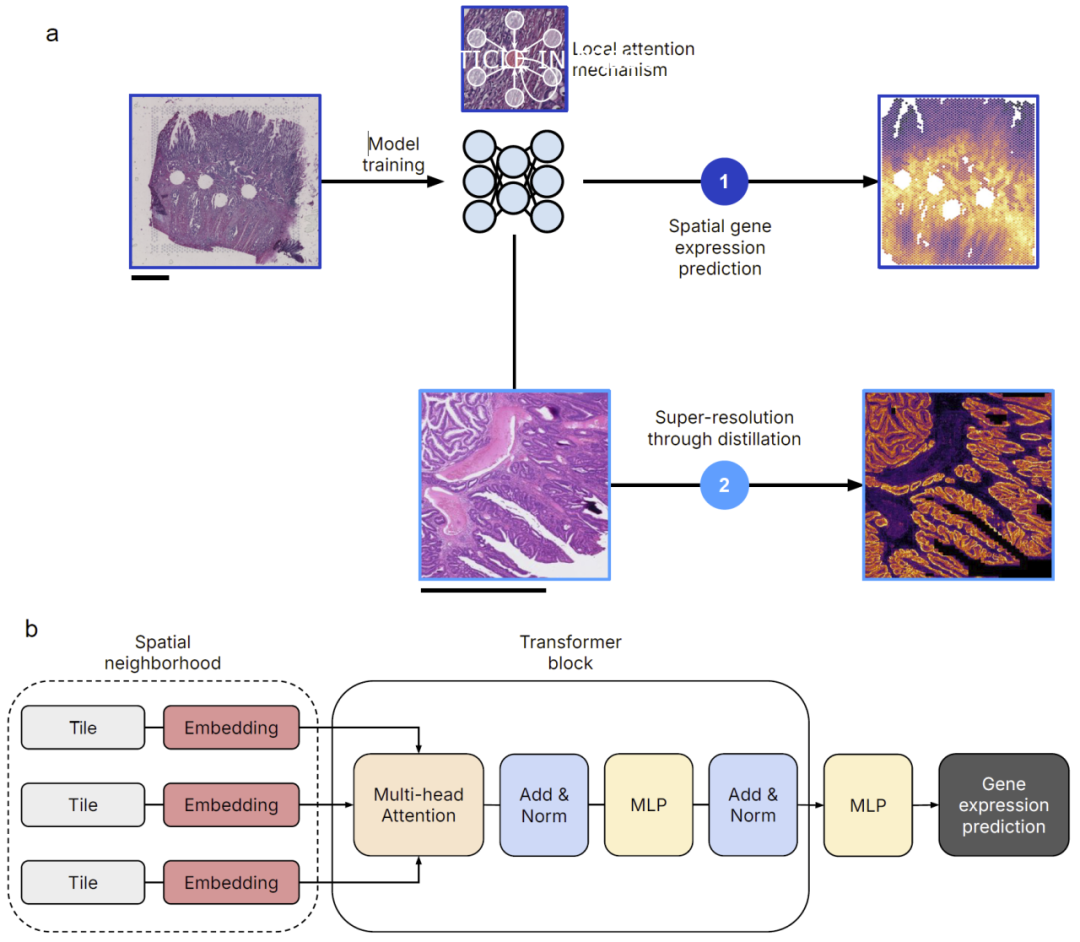
图1:MISO 结构与多尺度管线
结果
MISO 能稳健预测空间基因表达
MISO 在 48 个 PETACC8-Visium 训练样本中表现最佳:
- 显著优于 HisToGene、Hist2ST、iStar 等方法
- 训练效率高(Transformer 全局注意力计算量过大,而 MISO 的局部注意力降低了复杂度)
即使只依赖 H&E 图像,MISO 对肿瘤细胞、免疫细胞、基质结构的空间表达具有强预测能力。
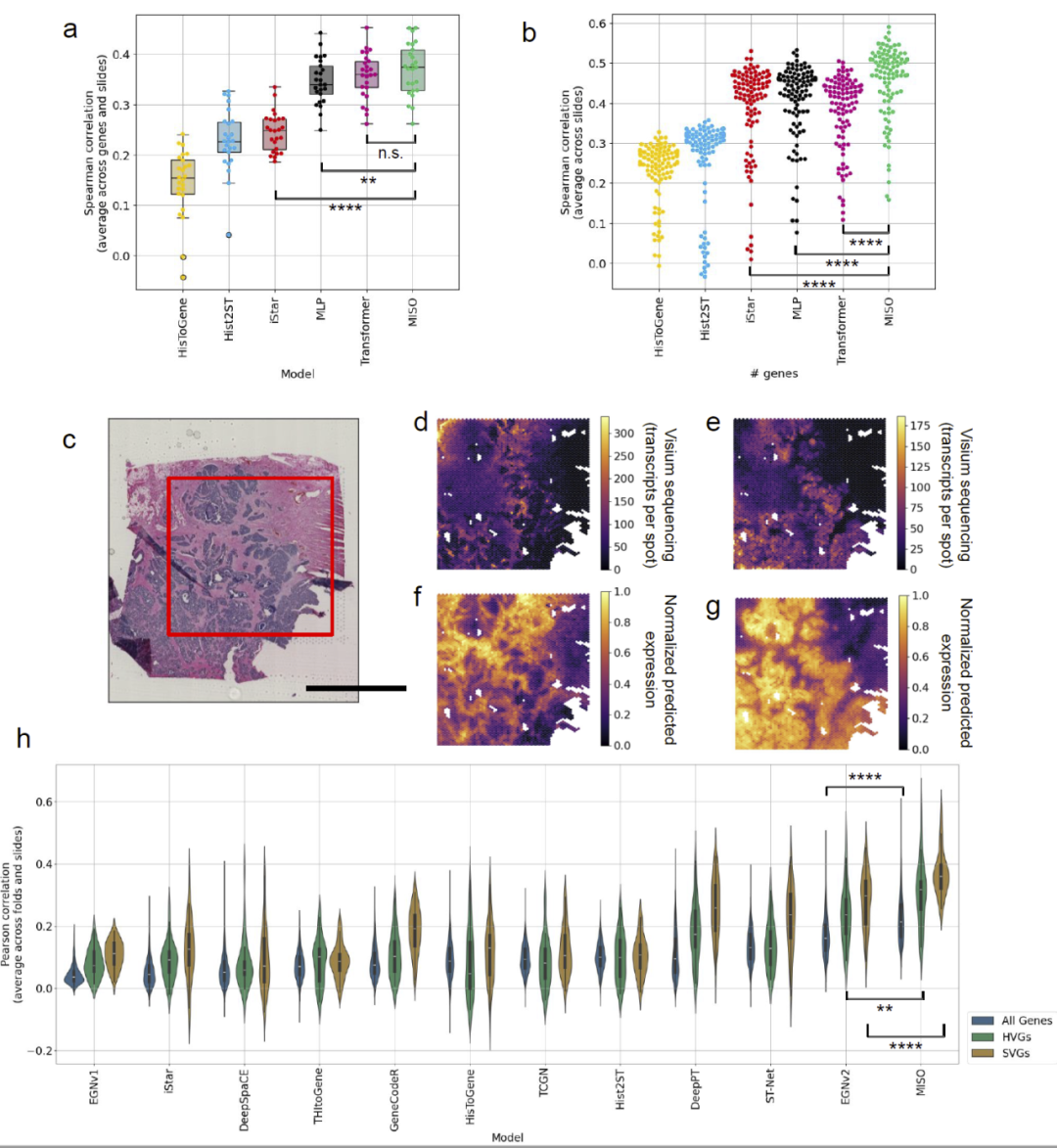
图2
MISO 在多个数据集上均优于对照模型
研究人员在多个场景中验证 MISO:
1. Visium 同癌种验证(In-domain)
- 在 24 个独立测试样本上,MISO 获得最高 Pearson/Spearman 相关系数
- 在全部 competing models 中表现最优
2. 异癌种泛化(Out-of-domain)
使用训练于结直肠癌的模型推断 HEST-1k 多癌种样本:
- 在 293 个 Visium 样本上仍保持良好表现
- 在乳腺癌、肺癌、内膜癌甚至非肿瘤组织中均具有可迁移性
此外,当训练集扩大到 MOSAIC(348 个样本,5 个癌种),MISO 的跨癌种泛化进一步增强。
MISO 可生成近单细胞分辨率的表达图
研究人员使用弱监督学习将 Visium spot 进一步细分为更小 patch,实现 7–10 μm 的空间尺度预测。
结果显示:
EPCAM 在肿瘤上皮区域强表达
IGKC 在浆细胞密集区域高表达
COL1A1 在纤维母细胞富集处高表达
与 Xenium 单细胞空间组学对照:
多个基因在 patch 级别的表达模式显著相关
超分辨率预测优于或可与 iStar 相当
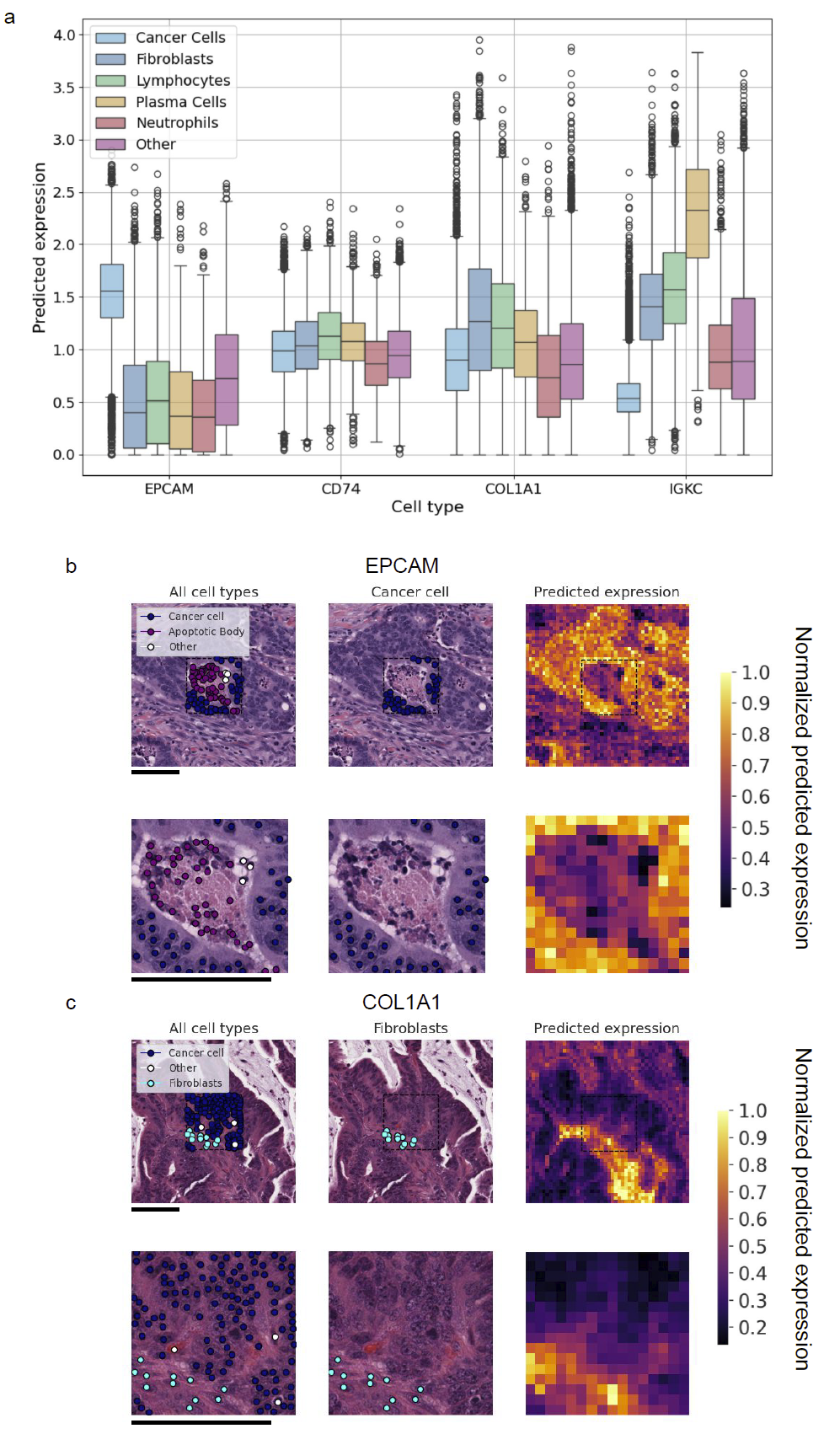
图3 :与细胞类型关联的超分辨率表达图
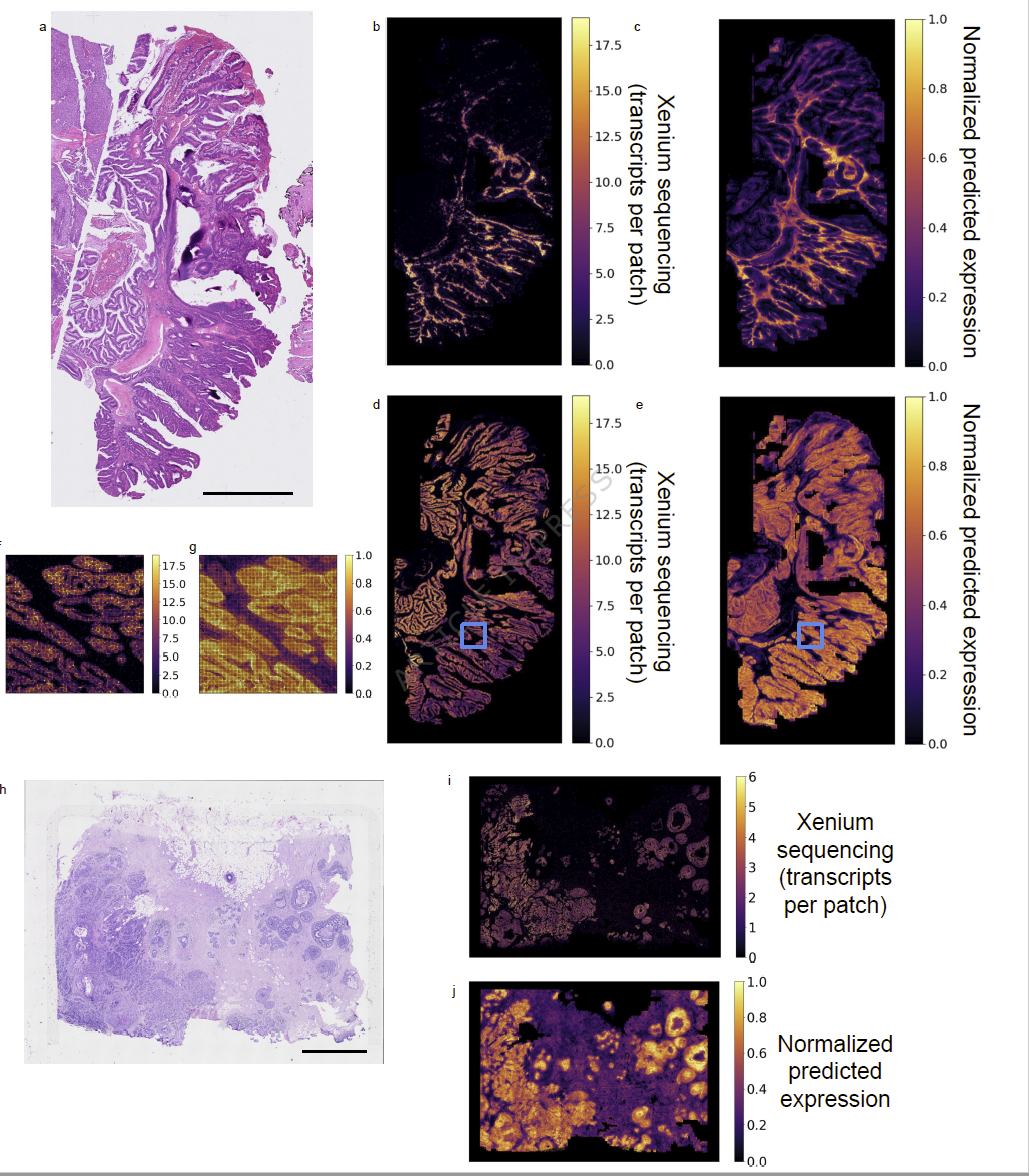
图4 :Xenium 单细胞空间组学对照
MISO 能识别与预后相关的空间表达模式
研究人员构建乳腺癌生存模型以识别高风险与低风险区域,并结合 MISO 的空间表达预测:
- 免疫球蛋白相关基因(IGKC、IGHG1 等)在 低风险区域 富集
- 细胞周期、代谢基因(MKI67、MYBL2、ENO1 等)在 高风险区域 上调
- Basal-like 亚型中,高 IGKC 在高风险区域的共定位提示更强的抗肿瘤免疫反应
这说明 MISO 不仅能预测基因表达,还能挖掘与临床结局相关的空间生物学信号。
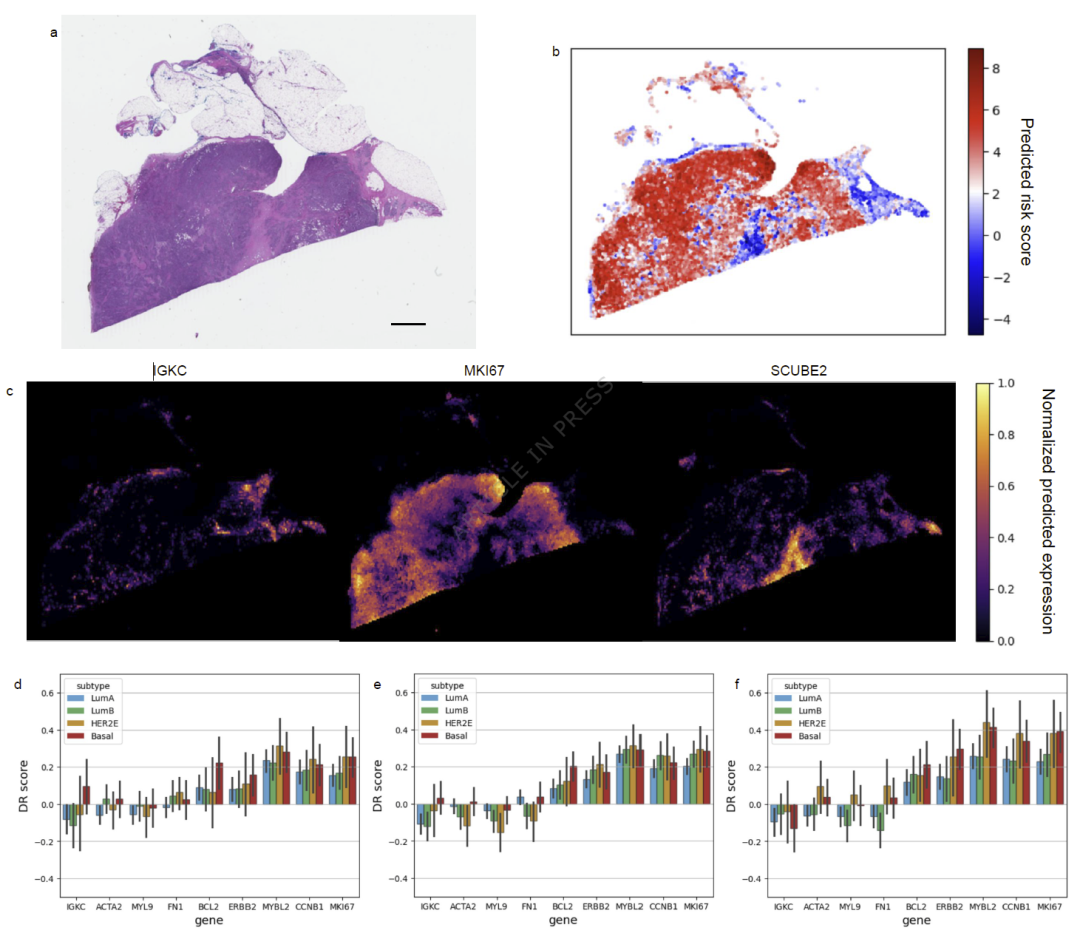
图5 :预后模型 + MISO 推断的空间基因表达热图
讨论
MISO 通过整合 H&E 形态学与空间组学,在多个层面展示关键进展:
- 多尺度空间建模能力
局部注意力机制有效捕获邻域组织交互,使模型更贴近真实细胞–细胞通讯模式。
- 跨癌种泛化表现优异
即使完全不使用目标癌种的空间组学数据,MISO 仍能稳健迁移到新组织类型。
- 实现接近单细胞的空间表达推断
MISO 在没有 Visium 输入的情况下仍能生成超分辨率表达图,以更低成本获得精细空间信息。
- 具备临床应用潜力
MISO 能帮助发现与预后相关的空间生物标志物,有助于理解肿瘤生态位结构与免疫排斥现象。
研究人员指出,未来可基于大规模 H&E 阵列开展药物靶点评估、免疫生态位识别及细胞通讯研究,为空间组学在临床中的广泛应用铺平道路。
整理 | DrugOne团队
参考资料
Schmauch, B., Herpin, L., Olivier, A. et al. A deep learning-based multiscale integration of spatial omics with tumor morphology. Nat Commun (2025).
https://doi.org/10.1038/s41467-025-66691-y
内容为【DrugOne】公众号原创|转载请注明来源
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2025-12-04,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

