Nat. Med. | AI驱动的LifeClock:在症状出现前多年预测疾病的新型生物钟
Nat. Med. | AI驱动的LifeClock:在症状出现前多年预测疾病的新型生物钟

DrugAI
发布于 2026-01-06 13:41:42
发布于 2026-01-06 13:41:42
DRUGONE
老龄化研究长期集中于成年阶段的衰老时钟,然而对于覆盖整个生命过程、尤其是婴幼儿与儿童时期的生物钟理解仍存在重大空白。研究人员提出了 LifeClock,一种基于常规电子病历与实验室检测数据的全生命周期生物钟模型,可在所有生命阶段预测个体的生物年龄。研究团队整合了来自 9,680,764 名个体、24,633,025 次临床随访 的异质性纵向数据,借助时间序列 Transformer 模型 EHRFormer,将虚拟患者表示映射到潜在空间,从而以高精度捕捉发育与衰老动态,建立跨年龄段的生物时钟。结果显示,儿童期和成年期呈现出截然不同的生物时钟特征:
- 儿童时钟与生长发育密切相关,能准确预测营养不良、生长迟缓、发育异常等主要儿科疾病;
- 成人时钟与老化过程显著相关,可预测糖尿病、肾衰、脑卒中及心血管疾病风险。
- LifeClock 区分了儿童发育与成人老化的本质差异,为精准健康管理提供了新框架。

衰老是一个复杂的多层次过程,涵盖分子、细胞、器官乃至全身系统的功能变化。传统的年龄指标反映的是时间流逝,而生物年龄(BA)则衡量生物系统相对于同龄个体的功能状态。生物年龄偏离时间年龄(CA)常提示疾病风险与健康衰退。早期研究依赖 DNA 甲基化、转录组等组学特征来估算 BA,而近年的多模态影像学与临床数据拓展了生物钟的维度。然而,这些研究主要聚焦成年人,对婴幼儿及儿童时期的生理“成熟时钟”缺乏系统刻画。儿童机体的快速生理变化体现的是发育进程而非衰老累积损伤,因此建立跨生命周期的统一模型具有重要意义。
方法
研究人员构建了一个 Transformer 架构的时间序列模型 EHRFormer,以整合大规模纵向电子病历(EHR)和实验室检测指标。模型通过多任务自监督学习完成特征重建、缺失值推断、下一次随访预测及批次效应消除,生成个体的数字化健康表征。数据来源包括中国健康老龄化调查(CHAI)及英国生物样本库(UK Biobank)等多队列共 约2500万条记录。
EHRFormer 在训练后用于回归预测时间年龄(CA),预测值即作为生物年龄(BA)的估计结果。模型进一步区分儿童期(<18岁)与成年期(≥18岁),以针对不同阶段的生理特征分别建立发育时钟与老化时钟。
结果
构建基于血液检测的全生命周期生物钟
研究人员从184个临床指标中提取特征,利用双随机掩码策略处理缺失数据并减少噪声。EHRFormer 在内部验证集上表现出高度准确性(MAE 约1.07–5.96,R²>0.8),可仅通过常规化验数据预测年龄。分析揭示了两种显著不同的时钟模式:
- 儿童阶段的时钟主要受 AST、肌酐和总蛋白等指标驱动;
- 成年阶段的时钟则与尿素、白蛋白和红细胞分布宽度等指标相关。
不同性别间模型性能稳定,但特征贡献略有差异。跨队列验证(UK Biobank)进一步证明了模型的普适性。
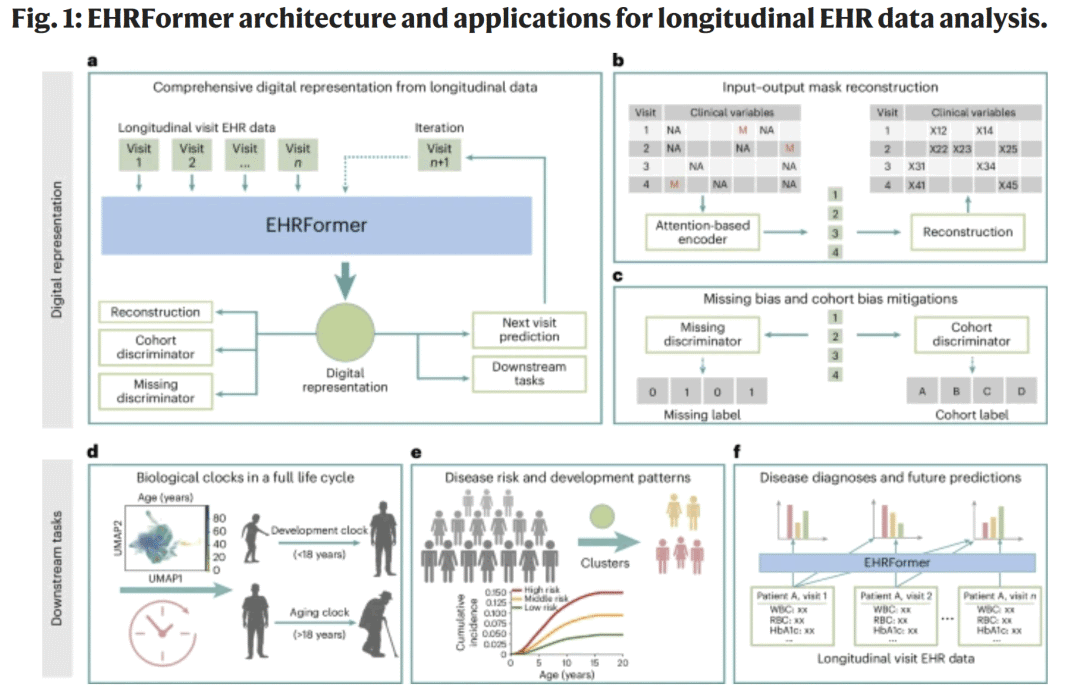
图1|EHRFormer 的架构与纵向临床数据分析应用
LifeClock 预测儿童与成人疾病风险
基于 EHR 表征进行主成分与 UMAP 降维后,研究人员发现年龄组之间可自然分群,提示EHR数据蕴含显著的年龄信息。通过 Leiden 聚类共得到64个亚群。研究人员计算个体的生物年龄差(BA–CA),并结合疾病发生率分析发现:
在同一簇中,生物年龄偏高(加速老化)的个体当前与未来的疾病风险均显著升高。
在儿童群体中,不同簇对应的疾病风险各异,例如:
- 簇14:垂体功能亢进与肥胖风险分别提升15.36倍与11.07倍;
- 簇12:疝气风险上升10倍;
- 簇3:病毒性脑膜炎风险上升4.7倍;
- 簇8:性早熟风险显著上升。
儿童发育时钟可区分发育迟缓与发育提前两类特征性疾病,表现出生理意义上的加速或减缓。
在成人群体中:
- 簇20 个体的肾衰竭风险上升37.7倍、低血压风险上升9倍;
- 簇16、52、20 的糖尿病风险分别增加约3–4倍。
这些结果表明模型能捕获潜在的疾病前状态。
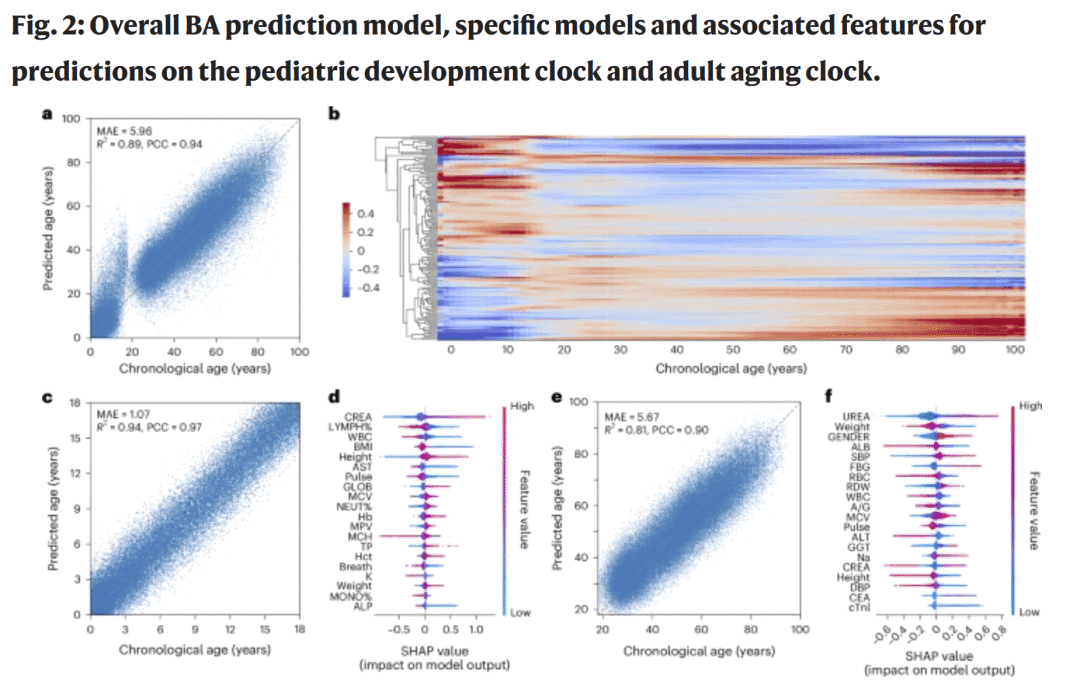
图2|全生命周期生物年龄(BA)预测模型及儿童与成人阶段的关键特征
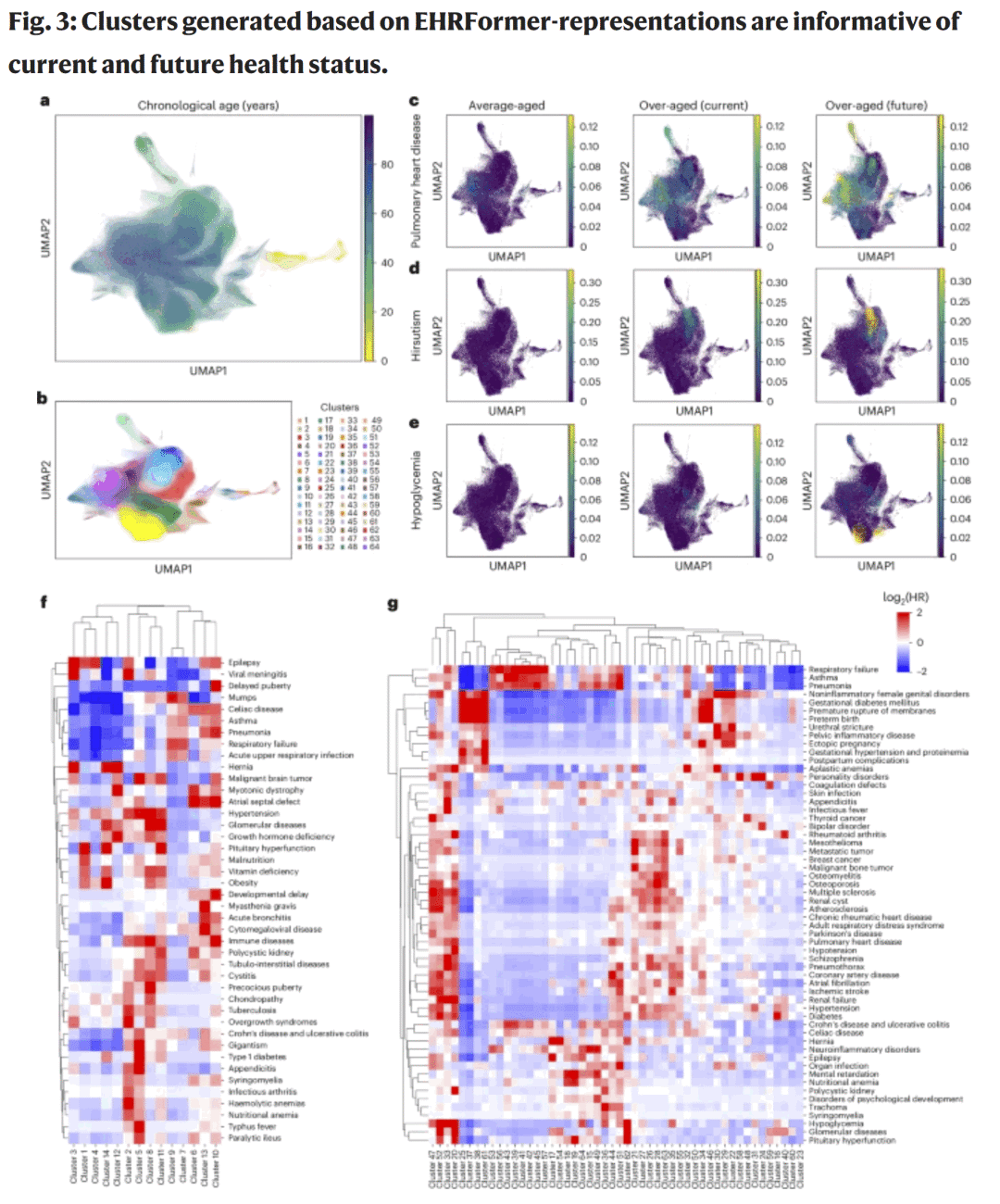
图3|基于EHRFormer 表征的患者聚类揭示当前与未来健康状态
特征与疾病模式解释
进一步分析显示,不同高风险簇具有特异的生理信号:
- 儿童簇5 与免疫相关疾病(如阑尾炎、溃疡性结肠炎)相关,特征为高 IL-6、IL-8、CRP 和白细胞数;
- 成人簇44 与心肺疾病风险高度相关,表现为高肌钙蛋白T和血钾、低血氧饱和度。
这说明聚类结果不仅反映统计分组,还对应生物学机制。
疾病预测性能
研究人员在疾病预测任务中微调EHRFormer,并将个体分为高、中、低风险组。结果显示模型在当前疾病诊断与未来风险预测中均表现出色:
- 诊断准确率:心血管疾病AUC高达0.95–0.98,神经系统疾病(帕金森、多发性硬化)AUC约0.94–0.96;
- 未来风险预测:各病种AUC普遍≥0.8,五年和十年发病预测AUC分别为0.80–0.91。
相比 RNN 与 XGBoost,EHRFormer 在所有任务上均取得更高AUROC(例如糖尿病预测0.911 vs 0.837/0.876)。外部验证(CHAI-External及UK Biobank)结果一致,表明模型具有优异的跨机构泛化能力。
此外,研究人员将0–10岁儿童与≥40岁成人分层后进行累积风险分析:
- 儿童阶段,高风险组未来肥胖、脑膜炎、哮喘等疾病的发病率显著更高;
- 成年阶段,高风险组心律失常、冠心病、糖尿病、卒中等疾病风险亦显著升高。
这表明早期EHR数据可用于长期健康风险评估。
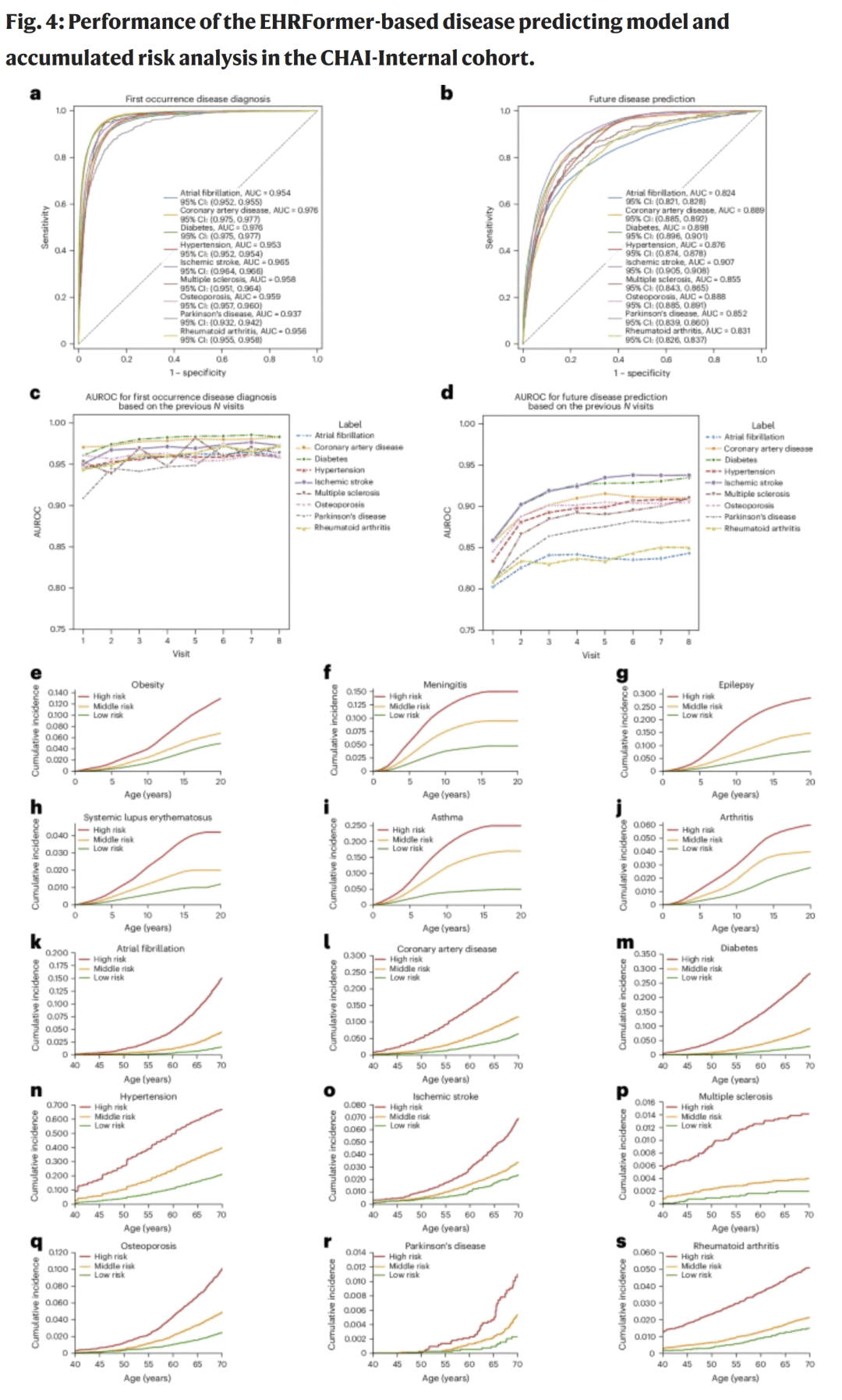
图4|EHRFormer 在疾病诊断与风险预测中的表现及累积风险分析
讨论
该研究首次基于常规临床数据实现了跨生命期的生物时钟建模,揭示了从婴儿到老年的连续发育-衰老轨迹。EHRFormer 不仅能准确估计生物年龄,还能通过聚类解析出具有生物学意义的亚群,实现疾病风险的早期识别与解释。
在儿童中,模型区分了从性早熟到发育迟缓的内分泌谱系;在成年人中,模型识别出代谢、免疫及心肺系统的功能衰退亚型。相比依赖昂贵多组学数据的传统模型(如OMICmAge),EHRFormer 仅需常规实验室数据即可获得高精度预测,具有更高的临床可推广性。
该模型的自回归结构可捕捉长期健康变化,实现个体全生命周期的动态表征。研究人员指出,未来可结合可穿戴设备、云端病历及环境传感数据,使生物钟从静态估计转向实时更新,从而推动个性化健康管理、疾病预警与精准干预。
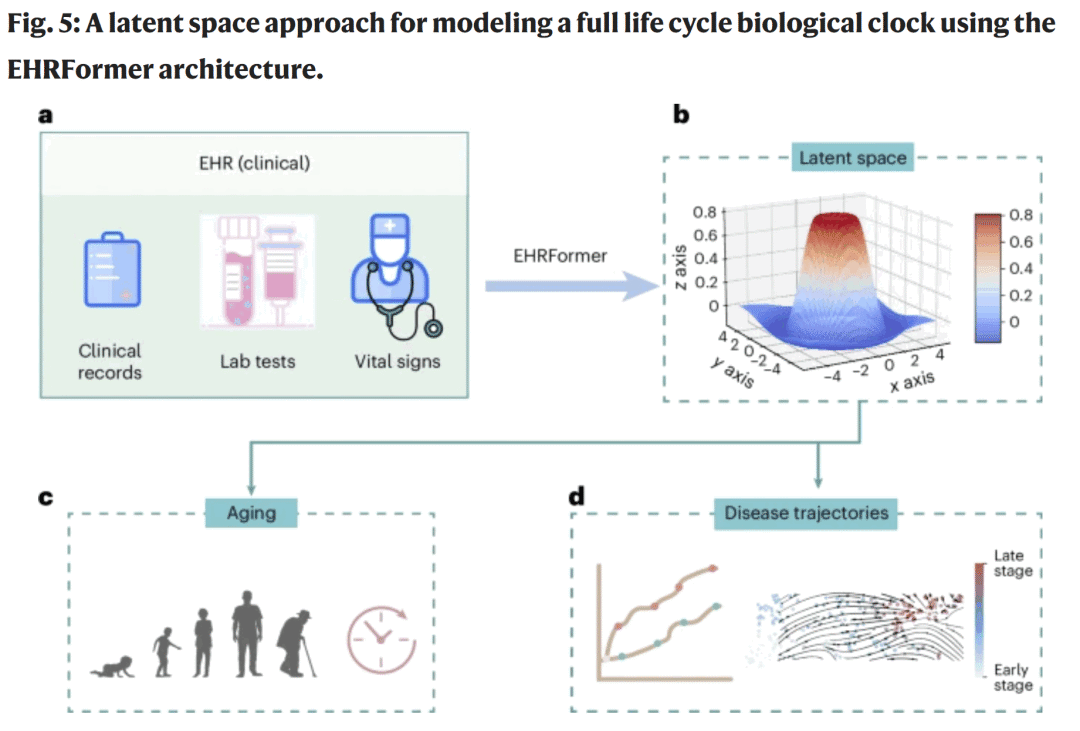
图5|基于 EHRFormer 的全生命周期生物钟潜在空间建模框架
整理 | DrugOne团队
参考资料
Wang, K., Liu, F., Wu, W. et al. A full life cycle biological clock based on routine clinical data and its impact in health and diseases. Nat Med (2025).
https://doi.org/10.1038/s41591-025-04006-w
内容为【DrugOne】公众号原创|转载请注明来源
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2025-10-29,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

