Nat. Commun. | 面向自动化有机–酶混合合成规划的虚拟平台
Nat. Commun. | 面向自动化有机–酶混合合成规划的虚拟平台

DrugOne
发布于 2025-12-17 17:02:50
发布于 2025-12-17 17:02:50
本文介绍一篇由浙江大学侯廷军教授、谢昌谕教授和澳门理工大学姚小军团队的关于混合有机—酶催化合成规划的最新研究工作。在这项研究中,作者提出了一个全新的 AI 驱动混合式合成规划平台 ChemEnzyRetroPlanner,旨在将有机合成与酶催化策略深度融合,为复杂分子的高效与绿色合成提供更加可行的解决方案。传统有机合成具备反应类型丰富的优势,而酶催化在对映选择性和温和条件下的反应效率方面具有显著潜力,但当前酶催化规划算法在路线整合与酶推荐方面仍存在灵活性不足的问题。ChemEnzyRetroPlanner 针对这些瓶颈,构建了一套涵盖混合逆合成设计、反应条件预测、可行性评估、酶反应识别、酶推荐与活性位点计算验证等模块的完整系统,并创新性地提出了 RetroRollout* 搜索算法,在多个基准数据集上均显著优于主流逆合成工具。平台同时提供可视化界面与程序化 API,配合链式推理策略与 Llama3.1 模型,可在多类任务场景中自主激活混合式路线规划,为提升分子合成效率与可持续性开辟了新的技术路径。研究团队已开放完整算法代码,并搭建了免费的 ChemEnzyRetroPlanner 在线计算服务(http://cadd.zju.edu.cn/retroplanner),供科研人员直接使用。

研究背景
有机合成与酶催化在分子构建中具有显著的互补性,两者的结合为复杂化合物的高效、绿色和立体选择性制备带来了新的发展方向。传统有机合成覆盖广泛的化学空间,反应类型多样,而酶催化在关键步骤中具备高度立体控制能力,并能在水相或温和溶剂中运行,显著减少保护–脱保护步骤及贵金属催化成本。随着定向进化技术不断拓展酶的底物范围,酶催化逐渐能够作用于非天然底物,使有机化学与生物催化的深度融合成为趋势。然而,现有逆合成模型大多基于以有机反应为主的数据集进行训练,对酶催化步骤预测能力有限;而全酶催化规划又因化学空间狭窄而难以适应更复杂的合成场景,凸显出发展混合有机–酶催化规划策略的迫切需求。
围绕混合式合成规划,已有研究提出了一系列算法,包括基于混合整数规划的路线优化、双模型协同预测有机与酶反应、在纯有机路线中替换效率较低步骤,以及采用 Transformer 架构分别构建有机与酶催化逆合成模型并结合启发式搜索等方法。然而,这些方法在识别酶催化步骤时普遍依赖模板匹配或反应相似度排序,限制了潜在路线的探索深度;同时,在反应–酶匹配的可行性验证方面仍显不足。此外,现有混合规划平台的自动化程度较低,用户仍需投入大量人工干预以配置任务与工具选择。随着 ChatGPT、Llama3 等大型语言模型的迅速发展,一批面向化学任务的 LLM Agent 相继出现,如 ChemCrow、Coscientist 和 LLM-RDF 等,已展示出利用链式推理与工具调度执行复杂化学流程的能力,为提升混合规划的自动化与智能化提供了新的可能性。
在此背景下,研究团队开发了混有机–酶催化合成规划平台 ChemEnzyRetroPlanner。该平台集成多步逆合成规划、单步预测、反应条件与反应速率预测、酶反应识别、酶推荐以及活性位点计算验证等七类核心模块,并通过程序化 API 支持在多种自动化场景中灵活调用(图1)。平台提出的 RetroRollout* 搜索框架引入 And-Or Tree 结构、在线模拟与跳节点策略,在搜索效率和目标路径解析率方面均取得显著提升。同时,平台整合来自多源数据的单步预测模型,使其能够在不同任务场景下自动选择最合适的混合规划策略。基于 Llama3.1:70B 模型构建的链式推理 Agent 则进一步提升了规划流程的自动化程度,能够协调调用丰富的化学工具与酶催化工具。此外,研究团队还开发了直观友好的Web图形界面,使该系统具备可解释、可扩展且易于使用的特点,为实现高效、可靠的混合有机–酶催化合成规划提供了新的技术路径。
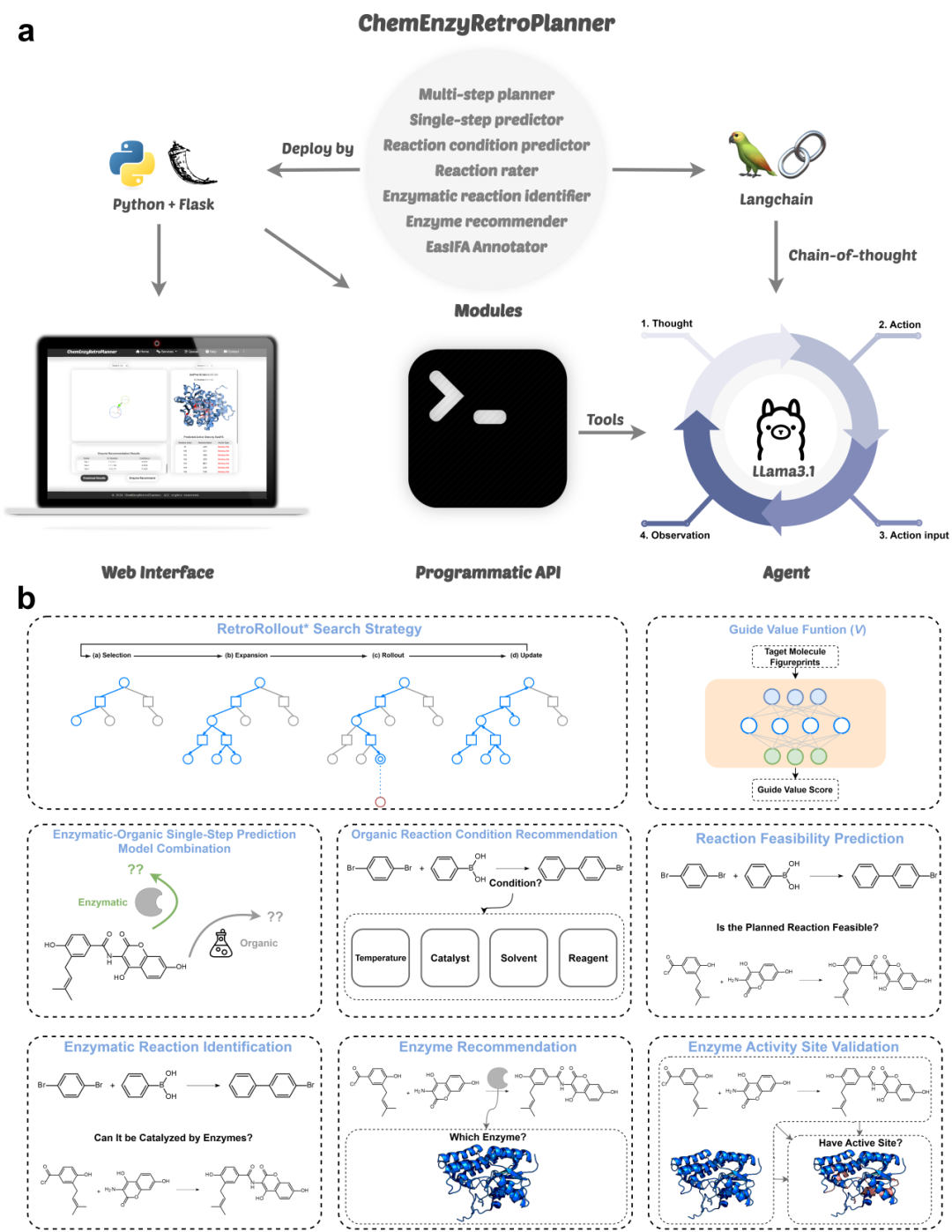
图1:ChemEnzyRetroPlanner 混合合成规划平台概览。(a)平台的技术框架及其支持的三种交互模式:图形界面、程序化 API 和智能 Agent。(b)平台包含的主要算法模块。
平台架构与算法设计简介
本研究首先在多步搜索与单步逆合成算法层面进行了核心优化。为了降低对价值函数估计的依赖并提升搜索效率,研究团队基于AND-OR树和Retro*算法的评分策略,提出了改进的RetroRollout多步搜索框架(图2)。该框架引入了类MCTS的Rollout步骤,包含选择、扩展、Rollout和更新四个阶段,并在Rollout阶段加入了针对成功姊妹节点的跳转搜索策略,同时利用基于分子指纹和多层感知机的路径深度导向函数来优化搜索方向。在单步逆合成方面,平台集成了基于六种不同数据分布训练的预测模型,涵盖了五种基于模板的算法(含酶促反应专用)和一种基于Transformer的混合反应预测算法,支持在多步搜索中同时调用多种模型,并通过归一化Softmax概率对预测结果进行统一排序和优选。
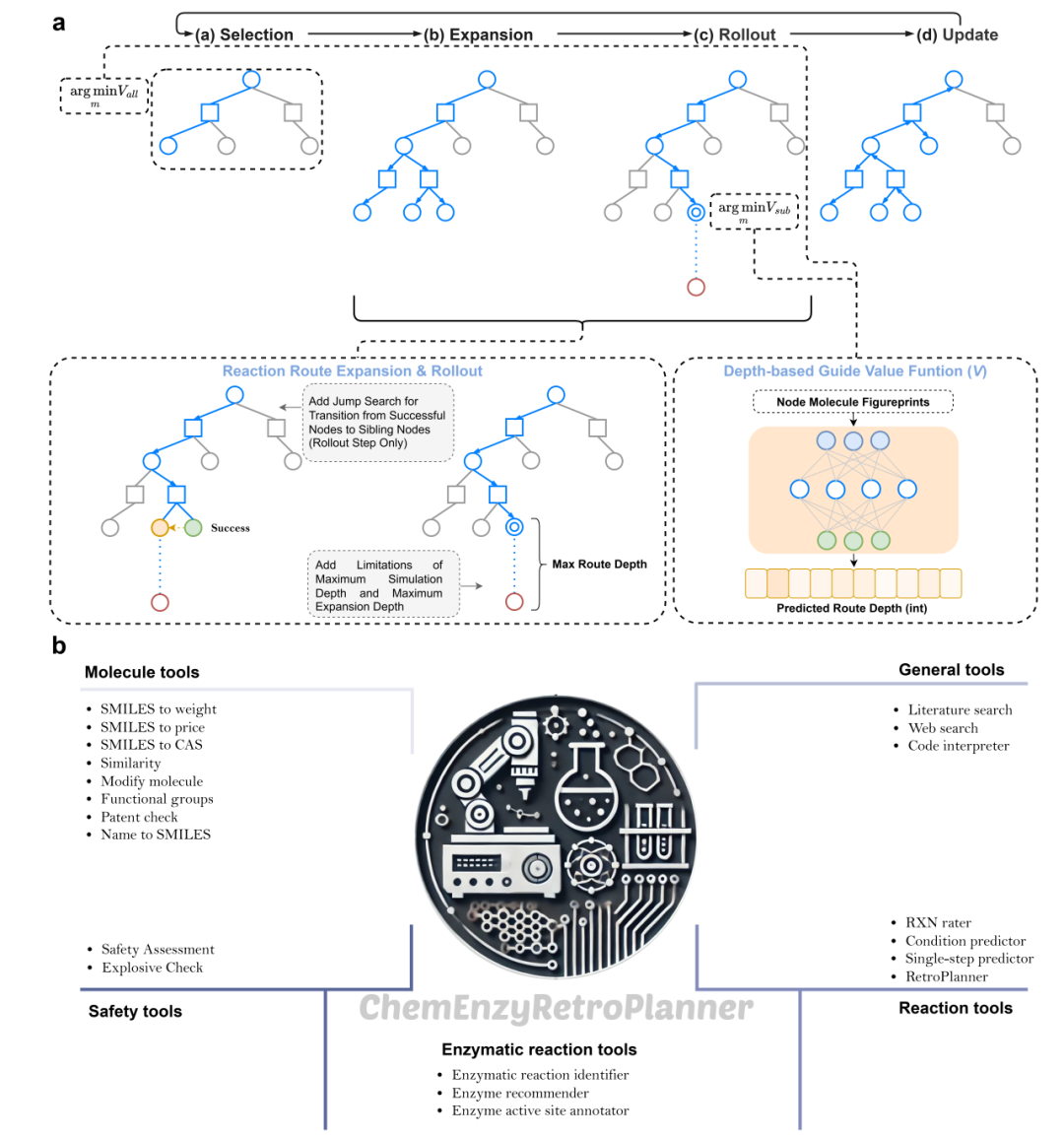
图2:ChemEnzyRetroPlanner 的搜索框架与 Agent 工具集。(a)RetroRollout* 的主要流程示意,包括选择、扩展、Rollout 与更新,并展示 Rollout 阶段的跳跃搜索。(b)Agent 工具集,包括分子工具、反应工具、安全评估工具、通用工具和酶反应工具。
为了实现高精度的混合有机-酶合成规划,平台内嵌了反应条件推荐、酶筛选及反应合理性评估等一系列功能模块。反应条件推荐模块集成了RCR和Parrot模型,采用规划后离线推理的方式为生成的反应路径补充条件信息。针对生物催化步骤,开发了基于RXNFP指纹和多层感知机的酶促反应识别与酶推荐模型,能够精准识别酶催化步骤并推荐EC编号;在此基础上,进一步集成了EasIFA工具,结合UniProt数据和AlphaFold预测的PDB结构,对推荐酶的活性位点进行注释和可视化,为酶的定向进化提供依据。此外,为了过滤单步模型产生的不可行反应,系统部署了基于Morgan指纹双分支架构的反应合理性评估器,该模型在构建的大规模专利基准数据集上表现优异,显著提升了路径的化学合理性。
结果与讨论
多步合成规划基准测试
本研究使用涵盖三种不同多步合成场景的测试集,对平台的多步规划能力进行了评估。这些测试集包括两个源自有机合成专利的测试集和一个基于天然产物的测试集。具体而言,这些测试集包括:由Chen等人在评估Retro*算法时初步整理并被后续研究广泛使用的USPTO-multistep-190测试集;由Genheden等人编制的用于评估多步逆合成算法的标准评估数据集PaRoutes-Set-n1和Set-n5的随机子集(包含多步合成路径数据、评估期间使用的单步反应训练数据以及构建块分子数据集);以及Zeng等人用于评估BioNavi平台的天然产物测试集及其配套的构建块分子数据集。
USPTO-multistep-190测试集中的基准测试。 本节比较了搜索框架、跳转搜索策略、引导函数类型、可购买构建块分子数据集的质量以及单步逆合成模型性能对目标分子合成路径搜索表现的影响。所选用的基线算法为原始Retro*,测试分子为Chen等人从USPTO中提取的190个具有代表性的复杂化合物。评估结果如表1所示。
表1: RetroRollout* 在 USPTO-multistep-190 测试集上与 Retro* 的性能比较。加粗表示最优结果。
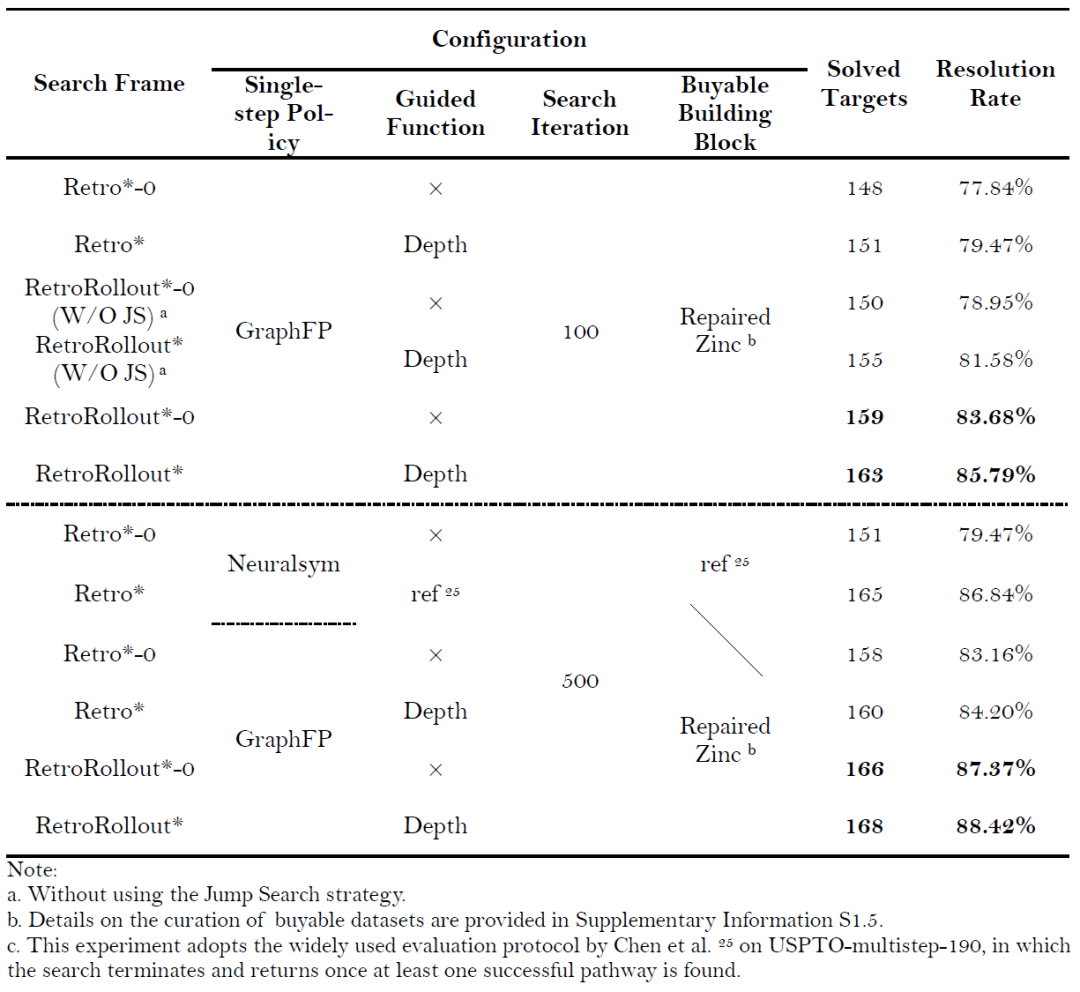
研究将不使用引导函数的搜索框架标记为“Search Frame Name-0”。当搜索迭代次数限制为100次,使用GraphFP作为单步逆合成策略,并采用修正后的Zinc可购买构建块分子数据集时,无论是否使用引导函数,本研究提出的Retro-Rollout*算法框架成功解析出合成方案的分子数量均多于Retro*。与Retro-0相比,RetroRollout*-0额外多解决了11个分子,解析率提高了5.79%;RetroRollout比Retro多解决了12个分子,解析率提高了6.32%。对比使用与不使用基于深度的引导函数的算法效果,可以明显看出引导函数有效地增加了被解决的目标分子数量。研究还对比了原始Retro*模型(使用Neuralsym作为单步策略网络,采用原始引导函数模型配置及可购买构建块分子数据集),发现在相同轮次下,RetroRollout*解决的分子数量多于Chen等人提出的原始Retro*,且对引导函数的依赖更小。即便不使用引导函数,RetroRollout*-0解决的分子数量也比使用反应成本引导函数的Retro*多出0.53%。
此外,研究对跳转搜索策略进行了消融实验,以评估其对搜索性能的具体影响。在此实验中,引入了两个不含跳转搜索的变体,分别命名为RetroRollout*-0 (W/O JS)和RetroRollout* (W/O JS),分别对应不带引导函数和带有基于深度引导函数的搜索框架。结果显示,与带有跳转搜索的原始RetroRollout*-0和RetroRollout*相比,这些变体解决的目标分子数量分别减少了4.7%和4.2%,证明了跳转搜索策略在提高搜索效率和成功率方面的有效性。研究还对比了Retro*-0和Retro*方法。在相同的单步预测模型和引导函数设置下,本研究提出的搜索框架即便不使用跳转搜索策略,仍比原始方法多解决1.1%和2.1%的目标分子,进一步表明了该搜索框架的内在优势。这些结果突显了RetroRollout*相对于Retro*在路线质量、搜索效率以及解决高难度合成目标能力方面的卓越平衡。
PaRoutes随机选择测试集中的基准测试。 本节采用标准化的多步逆合成评估方法,全面评估多步逆合成算法框架的性能。研究利用从USPTO反应数据集中提取的两个反应路径子集PaRoutes Set-n1和PaRoutes Set-n5分别训练单步逆合成预测模型GraphFP。研究使用这两个数据集中路径的叶节点分子作为可购买构建块分子数据集,并分别为Set-n1和Set-n5训练了基于深度的引导函数。Set-n1的分布更接近USPTO反应数据集的整体分布,而Set-n5包含更多具有较长合成路径的样本。评估标准不仅包括已解决目标分子的数量,还包括路径搜索的平均时间、完整合成路线命中的Top-k准确率,以及两个反映路线质量的指标:规划出的较短合成路径的比例和叶节点分子的平均重叠率。评估结果如表2所示。路线的评分和排名是根据Badowski等人报道的方法进行的。
表2: RetroRollout* 与 Retro* 在 PaRoutes 测试集上的性能比较。加粗表示最优结果。
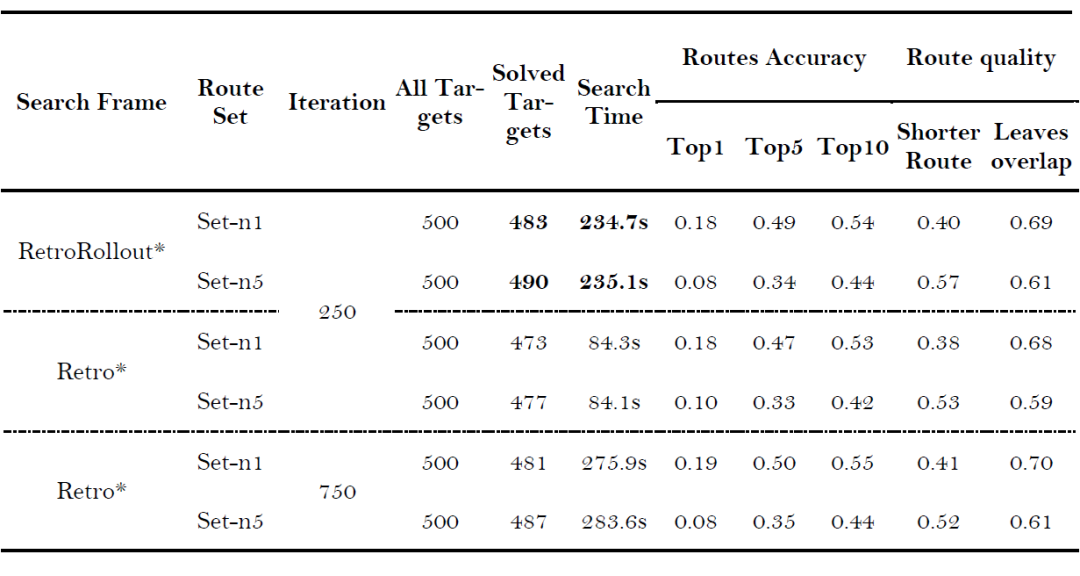
当搜索迭代次数限制为250次时,观察到在Set-n1中,RetroRollout*解决了500个目标分子中的483个,而Retro*仅解决了473个。两个算法框架在Top-1准确率上相当,但RetroRollout*在Top-5和Top-10准确率上更高,其规划的路径平均更短,且与标准路径在叶节点上的重叠率更高。在Set-n5中,RetroRollout*解决了490个分子的路径,而Retro*解决了477个,Retro*在Top-1准确率上略优于RetroRollout*,但RetroRollout*在Top-10准确率上领先。尽管两种算法在Set-n5数据集的Top-k准确率上各有所长,但RetroRollout*规划的路线质量更高,具有更短的路线和更高的标准路线叶节点重叠率。
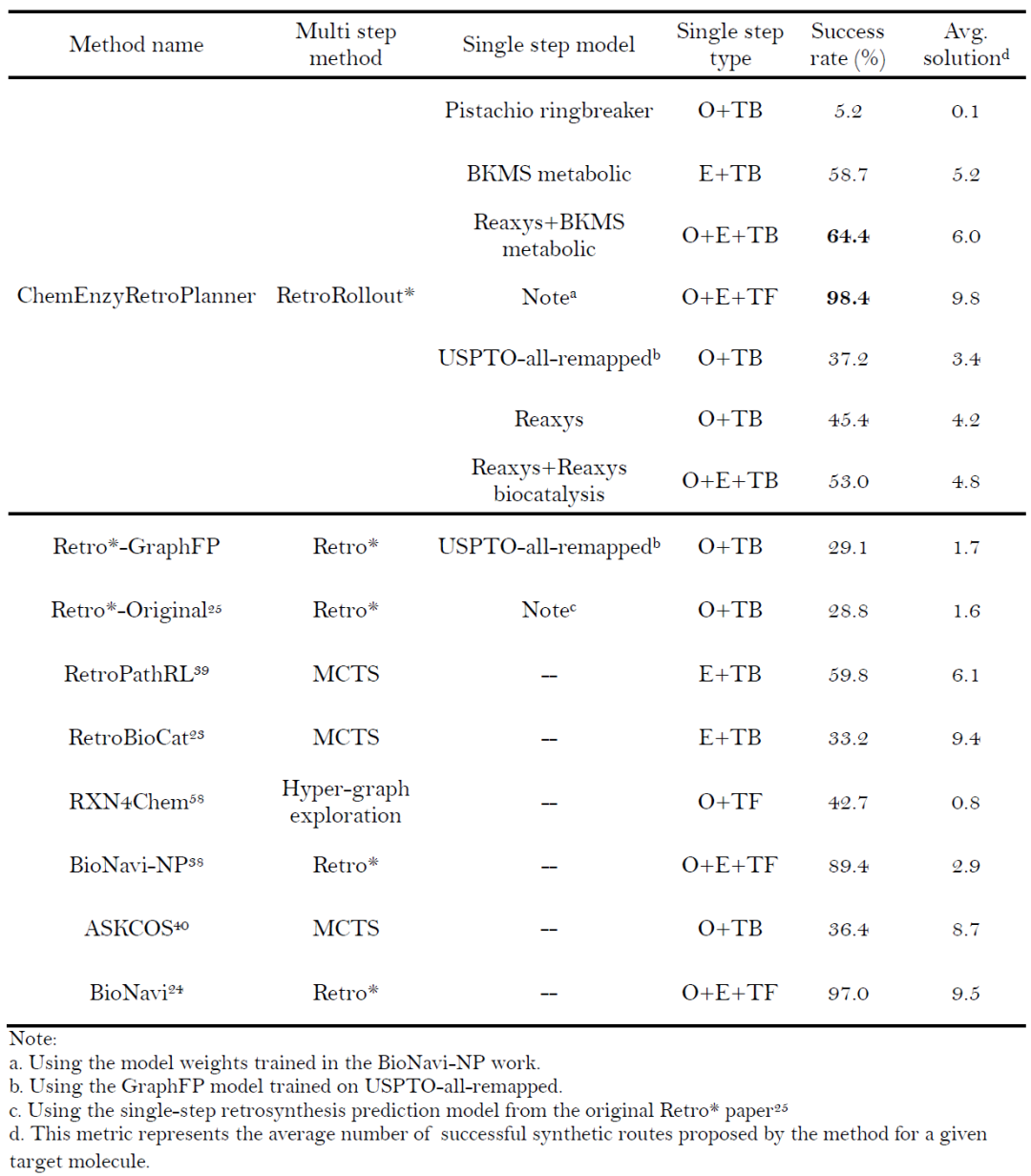
天然产物数据集基准测试。本节使用Zeng等人使用的天然产物数据集评估了ChemEnzyRetroPlanner平台解析分子路径的能力,并将其性能与其他已报道的平台进行了比较。ChemEnzyRetroPlanner测试了各种单步策略模型在路径搜索中的有效性。这些单步模型在研究中根据其来源的训练数据集命名,包括来自ASCKOS的四种基于模板的单步逆合成预测算法:Pistachio ringbreaker、BKMS metabolic、Reaxys和Reaxys biocatalysis。此外,研究还测试了在USPTO-all-remapped数据集上训练的基准模型(GraphFP,与USPTO-multistep-190测试集中的基准相同)以及Zheng等人报道的在酶促和有机反应混合数据集上训练的基于Transformer的单步逆合成预测模型。本节的测试结果如表3所示。结果表明,当ChemEnzyRetroPlanner平台结合RetroRollout*和其他主流开源单步逆合成预测模型时,显著提高了路径解析的成功率。具体而言,结合两种不同的基于模板的单步逆合成预测模型(分别在Reaxys和BKMS metabolic数据集上训练)的策略优于RetroPathRL、RetroBioCat、ASKCOS和原始Retro*等基准模型,实现了64.4%的路径解析成功率,显著高于表现最佳的基于模板的基准方法RetroPathRL(59.8%)。此外,当RetroRollout*搜索策略与BioNavi-NP中使用的相同的无模板方法相结合时,也获得了更高的路径解析成功率。目标分子的合成路径解析成功率达到98.4%,略微超过了在更广泛数据集上训练的BioNavi方法。
表3: RetroRollout* 与其他方法在天然产物数据集上的性能比较。单步逆合成预测模型以其训练数据集名称标注。缩写说明:O —— 有机反应单步模型;E —— 酶反应单步模型;TB —— 基于模板的单步模型;TF —— 无模板单步模型。加粗表示最优结果。
酶反应识别模型与酶推荐器的基准评估
本节系统评估了嵌入在ChemEnzyRetroPlanner平台中的酶促反应识别模型和酶推荐器的性能,并将其与当前最先进的基准方法进行了比较。
对于酶促反应识别模型,研究选择了一种广泛采用的基于反应模板匹配的基准方法。该方法利用RetroBioCat平台发布的135个酶促反应模板,通过检查给定反应步骤是否与任何预定义模板匹配来确定其是否为酶促反应。研究在一个由混合数据集组成的测试集上评估了内置模型和这种经典方法的性能,评估结果总结于表4。结果显示,内置的基于RXNFP的酶促反应识别模型在区分酶促与非酶促步骤的二分类任务上表现出色。除召回率(0.9895)外,所有评估指标均超过0.9900,且模型的推理速度比模板匹配基准快约五倍。相比之下,基于模板匹配的方法分类性能相当低,主要归因于其严重依赖手工整理的反应规则的判别能力。如表4所示,其预测能力无法满足平台的高精度需求。通过将酶促反应识别构建为二分类问题并利用带有注意力机制的可学习反应指纹,本研究的模型实现了稳健且可扩展的性能,为合成规划中的大规模酶促反应筛选奠定了坚实基础。
表4: ChemEnzyRetroPlanner 内置酶反应识别模型与基于反应模板匹配的方法对比的基准测试结果。加粗表示最优结果。
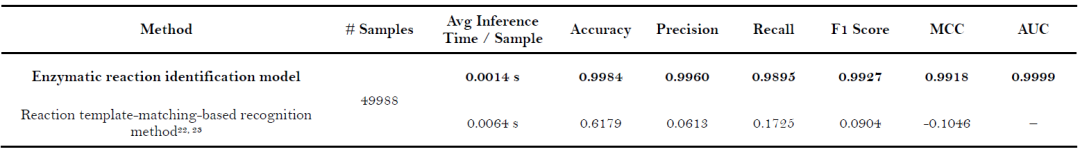
表5: ChemEnzyRetroPlanner 内置酶推荐模型与其他主流酶推荐方法的基准测试结果。加粗表示最优结果。
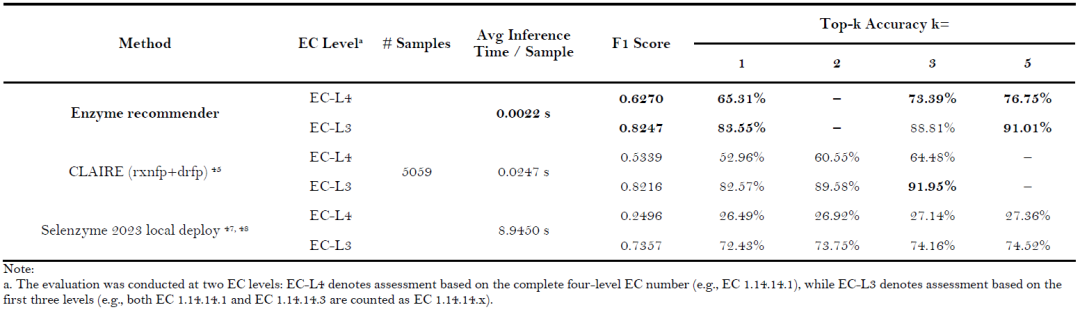
对于酶推荐器,核心任务是将酶促反应分类到其对应的EC编号。研究将该方法与两种具有代表性的主流方法进行了比较:CLAIRE和Selenzyme 2023,比较结果总结于表5。在EC-L3预测任务上,嵌入ChemEnzyRetroPlanner的酶推荐器表现与CLAIRE相当。然而,在更具挑战性的EC-L4预测中,本研究的酶推荐器实现了65.31%的Top-1准确率,显著优于CLAIRE的52.96%。Selenzyme 2023在EC-L3级别实现了72.43%的Top-1准确率,但在EC-L4级别性能大幅下降,Top-1准确率仅为26.49%。在推理速度方面,ChemEnzyRetroPlanner中的酶推荐器比CLAIRE快约10倍,比Selenzyme 2023快约4000倍,展示了极高的计算效率。这使其特别适合集成到合成规划工作流中,以满足对大量反应节点进行快速频繁预测的需求。
反应可行性评估器的基准测试
研究首先利用来自USPTO的反应数据构建了一个基准数据集(称为模板混洗数据集),用于评估反应合理性评估器的基线性能。研究评估了三种类型的反应表示:Morgan指纹、RXNFP和DRFP。其中,基于Morgan指纹和双分支多层感知机架构的模型实现了最佳的整体性能。在确定最佳模型结构和反应表示后,研究在一个更大规模的反应合理性预测数据集(称为Faiss-Template采样数据集)上对模型进行了训练。为了进一步比较模型区分不同类型反应样本的能力,研究从Faiss-Template采样数据集的测试集中提取了44,280个样本,构建了一个与基准数据集无重叠的通用测试集。研究比较了RXN Filter-benchmark、RXN Filter-deployed以及ASKCOSv2系统中内置的快速过滤器(fast filter)的性能。结果表明,RXN Filter-deployed模型在该测试集上表现最为均衡。相比之下,仅在模板混洗数据上训练的RXN Filter-benchmark模型表现出高得多的假阳性率。同样,ASKCOSv2快速过滤器也表现出类似的特征。总之,RXN Filter-deployed提供了更准确和稳健的分类,使其成为在实际合成规划工作流中检测化学上不合理反应的更合适的过滤模块。
Web 服务器界面展示
在输入和选项方面,平台支持直接粘贴SMILES,以及点击“Draw”按钮在JSME容器中绘制分子。在本研究中,分子CCCC(=O)O被用作输入示例,如图3a所示。用户可以点击“Options”按钮选择混合合成规划平台运行的若干参数。这些包括“Keep search after solved one route”(解决一条路线后继续搜索)、“Use reaction plausibility evaluator”(使用反应合理性评估器)、“Use guiding function”(使用引导函数)、“Predict reaction conditions”(预测反应条件)、“Identify enzymatic reactions”(识别酶促反应)和“Recommend enzymes”(推荐酶)。用户可以从平台提供的四个预定义可购买构建块数据集中进行选择。可以同时选择多个数据集。此外,平台提供七种可选的单步逆合成预测模型,其中包括三种在常规有机反应数据集上训练的模型——GraphFP (USPTO-all-remapped)、Pistachio Ringbreaker和Reaxys——以及三种在酶促反应数据集上训练的模型——Transformer (USPTO-NPL+BioChem)、BKMS Metabolic和Reaxys Biocatalysis(这些模型根据用于训练的数据集命名,采用MLP和基于反应模板的单步算法)。在单步逆合成模型选择框中,可以同时选择多个模型进行协同搜索。结合酶促反应单步逆合成模型(如BKMS Metabolic)与有机反应单步逆合成模型(如Reaxys)有助于规划混合合成路径。此外,用户可以根据需要设置搜索算法的迭代次数。配置完所有参数后,点击“Submit”按钮启动对输入目标分子的合成路线搜索。所有算法输出均显示在“Log”框中,平台返回一个用于查看结果的密钥(key)。搜索完成后,“View Results”按钮变为激活状态。点击此按钮将用户重定向到结果界面,用户可以通过上传相应的密钥查看计算结果。
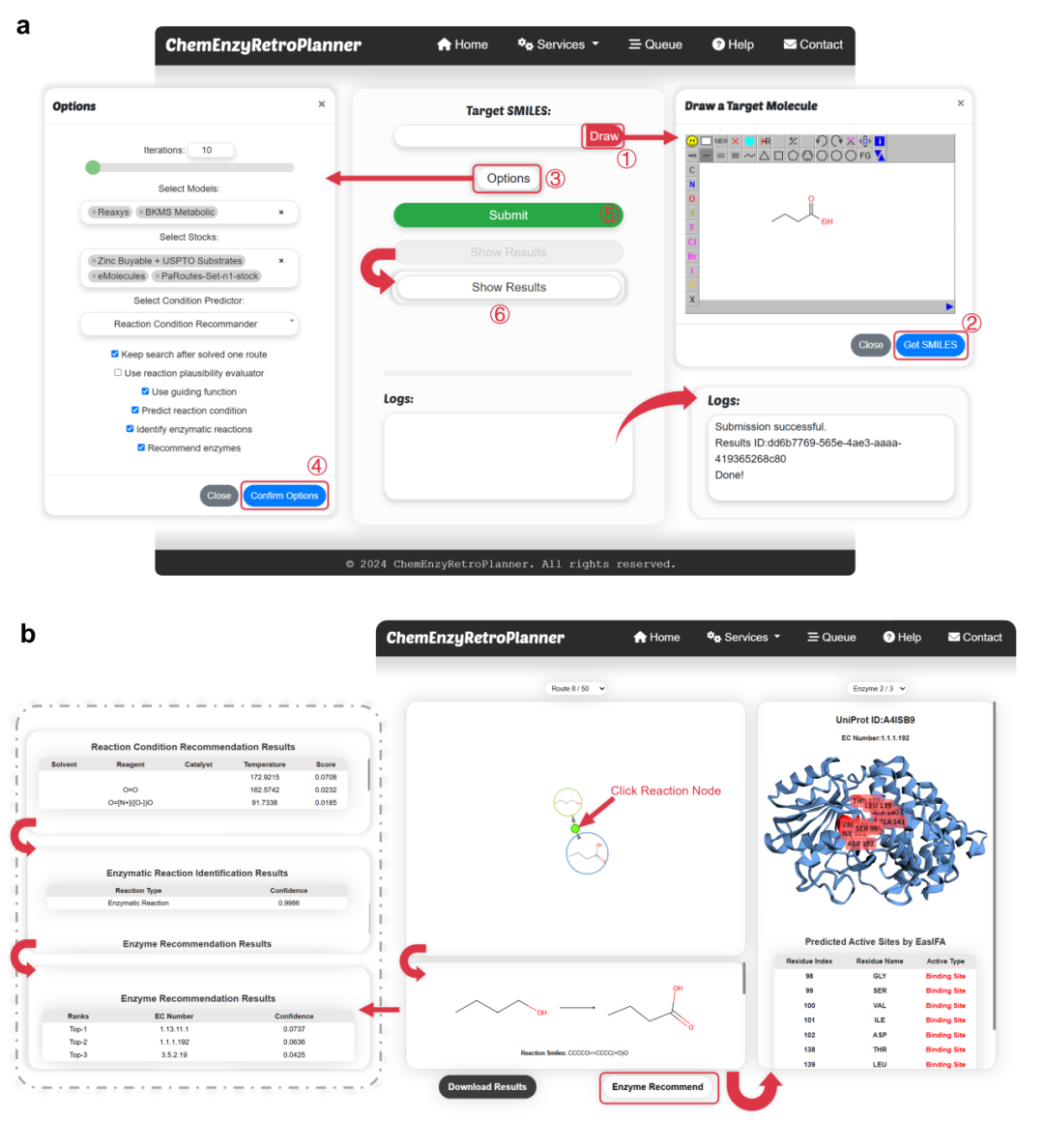
图3:ChemEnzyRetroPlanner 平台输入界面及结果界面。
在结果显示方面,用户提供相应的密钥文件后,界面将跳转至结果页面,如图3b上半部分所示。结果页面包含三个主要部分:用于在多条合成路线之间切换的下拉菜单、交互式合成路线展示图和单步反应显示框。对于每条显示的合成路线,用户可以点击反应节点(酶促反应显示为绿色,常规有机反应显示为黄色)以查看该步骤的详细信息。此信息显示在单步反应显示框中,依次显示单步反应方程式、平台推荐的反应条件、酶促反应的识别结果和酶推荐结果。一旦单步反应被识别为酶促反应,“Enzyme Recommend”按钮即变为激活状态。点击此按钮,平台将调用UniProt数据库API以查找推荐EC编号下的酶,并使用EasIFA算法预测活性位点。此时,酶结构显示栏将弹出,允许交互式查看酶的结构。详细的活性位点信息也显示在结构下方的表格中。
合成规划案例研究
为了进一步评估ChemEnzyRetroPlanner的实用性,研究将其应用于六种药学相关或生物活性化合物的逆合成路线规划。算法采用了一种基于模板的可解释单步逆合成预测器,集成了Reaxys和BKMS代谢反应知识库。其中,Esmolol、Desmethylxanthohumol和3-(Benzenesulfonyl)-6-methyl-4-(4-methylpiperidin-1-yl)quinoline的预测路线反映了混合酶-有机合成策略,而Celiprolol、S-(-)-Warfarin和AZD7545的预测路线对应于全有机路径。这六个具有代表性的例子不仅展示了ChemEnzyRetroPlanner在复杂生物活性化合物逆合成规划中的广泛适用性,也突显了其在设计具有高准确性和实用性的混合酶-有机路线及常规有机合成方面的双重能力。
Agent 案例研究
ChemEnzyRetroPlanner包含一个基于编程API的智能体APP,除了执行ChemCrow支持的全离线部署的合成规划任务外,还可以处理反应步骤内的酶促步骤规划和验证任务。图4a展示了工作流程,其中智能体自主评估单步反应的可行性,确定其是否为酶促反应,并推荐酶。智能体首先使用ReactionRater工具评估4-(hydroxymethyl)-2-furancarboxaldehyde phosphate (4-HFC-P)的合成反应是否可行。一旦确认反应可行,即使用EnzymaticRXNIdentifier来确定该反应步骤是否可以由酶催化(即是否为酶促反应)。该工具以0.9975的置信度识别出该单步反应为酶促反应。智能体随后调用EnzymeRecommender,推荐最有可能催化该反应的五种酶类别,其中最可能的酶具有EC编号4.2.3.153。所有推理结果均准确无误。图4b进一步展示了EasIFA模块在推荐最可能的酶实体以及使用活性位点预测来检查推荐酶中是否存在针对给定酶促反应的活性位点方面的应用。结果显示,EasIFA模块推荐了UniProt ID为Q58499的酶,即(5-formylfuran-3-yl)methyl phosphate synthase,其含有两个活性位点LYS27和LYS85,与UniProt中记录的反应位点信息相对应。

图4:ChemEnzyRetroPlanner Agent 的酶推荐案例研究。
此外,在更复杂的合成规划任务中,ChemEnzyRetroPlanner智能体展现了强大的自动决策能力。该系统能够自主确定和优化单步逆合成预测模型的混合配置策略,从而为处于不同化学空间的分子更高效地规划合成路径。例如,图5展示了智能体对天然产物苯氧基自由基VII(大豆中异甘草素生物合成hispidol的中间体)合成路径的分析。智能体首先评估该化合物是否为受控化学品。在确认其与受控化学品相似度低后,它调用RetroPlannerRetrosynthesis工具进行路径规划。最初,智能体采用了纯有机合成规划策略,但未能为该天然产物生成路径。随后,智能体自主决定切换到混合合成规划策略,结合有机合成和酶法合成方法。这成功生成了131条候选合成路径,其中最佳路径与天然产物苯氧基自由基VII的实际生物合成路径精确匹配。此外,智能体全面总结了该最佳路径每一步所需的基本反应条件,并在采用酶法合成策略时适当地推荐了应优先考虑的酶类型。

图5:Agent 对天然产物 phenoxy radical VII 的合成规划分析结果。
结论
本研究开发了一个混合酶-有机合成规划平台 ChemEnzyRetroPlanner,它整合了一套全面的有机合成规划工具,以及用于酶合成规划的计算与验证工具。该平台实现了有机单步逆合成预测模型和酶促反应单步逆合成预测模型之间的联合搜索功能。ChemEnzyRetroPlanner 在多个与有机合成和天然产物相关的测试集中,展现出优于同类算法平台的显著优势。此外,研究团队开发了自动化配置流程并构建了基于 Web 服务器的用户友好型图形界面,以增强用户体验。更进一步,研究团队为平台工具开发了编程 API,并构建了一个完全开源的智能体应用,为自主实验室部署和可扩展性提供了强大的潜力。总而言之,ChemEnzyRetroPlanner 能够规划结合有机反应和酶促反应的混合合成路线,支持合成路径规划中的反应条件预测、酶类别推荐以及酶活性位点注释。这个开源平台旨在协助药物研究人员识别更合理、更具成本效益、且环境可持续的合成路线,同时为酶促反应的应用提供必要的活性位点验证信息,从而提供具备坚实基础的合成解决方案。
参考资料
Wang, X.#, Yin, X.#, Zhang, X., Zhao, H., Gu, S., Wu, Z., Zhang, O., Qian, W., Huang, Y., Li, Y., Jiang, D., Wang, M., Liu, H., Yao, X.*, Hsieh, C.-Y.*, & Hou, T.* (2025). A Virtual Platform for Automated Hybrid Organic–Enzymatic Synthesis Planning. Nature Communications.
doi: 10.1038/s41467-025-65898-3
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2025-11-29,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

