单细胞空间--抗原呈递癌症相关成纤维细胞生态位的单细胞分辨率空间分析
原创单细胞空间--抗原呈递癌症相关成纤维细胞生态位的单细胞分辨率空间分析
原创
追风少年i
发布于 2025-10-05 13:30:29
发布于 2025-10-05 13:30:29
作者,Evil Genius
国庆一直下雨是怎么了?那些黑心、拖欠工资、不顾别人死活的老板,所作所为让老天爷发怒了?
酌情考虑在11月开一个番外,培训大家linux、环境搭建以及python语言,不知道大家有多少兴趣参加。
我现在理解为什么当初上学老师们拼命让我们学习,可是我们就是不学,叛逆。我在县里上的初中,初中老师说的话我印象最深,让你们学习你们以为是干什么呢?是往你们口袋里装钱呢,而你们呢,就是摁住口袋不让装。
当初要是把上学浪费的钱都拿去买资料学习,没有经常去网吧,我觉得算下来装在口袋里的钱,买个房应该是没问题了,不像现在租的房子。
研究生宿舍4个人,我混的最差,真的是难受了,运气怎么老是不站在我这边?
今天我们分享文献,王凌华的影响还是很大。

知识积累
近期研究发现了一种被称为抗原呈递癌症相关成纤维细胞(apCAFs)的特殊亚型。
成纤维细胞作为间充质细胞,在维持组织完整性、调控炎症反应与纤维化进程以及促进伤口修复中发挥着关键作用。癌症常被喻为"永不愈合的创伤",这使得成纤维细胞成为肿瘤微环境的核心组分。在该环境中,它们通过合成与修饰细胞外基质、与癌细胞进行复杂信号传导以及与浸润免疫细胞相互作用等方式行使多种功能。因此,癌症相关成纤维细胞(CAFs)已成为提升癌症治疗效力的重要靶标。
新近证据表明,CAFs在表型上可根据分子特征分为三大亚型:炎症型CAFs(iCAFs)、肌纤维母细胞型CAFs(myCAFs)和抗原呈递型CAFs(apCAFs)。
apCAFs以表达人类白细胞抗原II类(HLA-II,人源)或主要组织相容性复合体II类(MHC-II,鼠源)分子为特征,能有效呈递抗原并调控T细胞反应。
关于apCAFs的核心科学问题包括:其在人类肿瘤中的存在性、不同癌症类型中的细胞起源以及所处的空间生态位。
为解析两种apCAF群体形成的基质生态位,采用高分辨率单细胞空间成像平台对图谱衍生的CAF亚型特征进行空间解卷积。该分析显示间皮样apCAFs邻近癌细胞分布,而纤维细胞样apCAFs则富集于淋巴细胞密集区域。
结果1、癌症相关成纤维细胞表型在多种癌症中高度保守
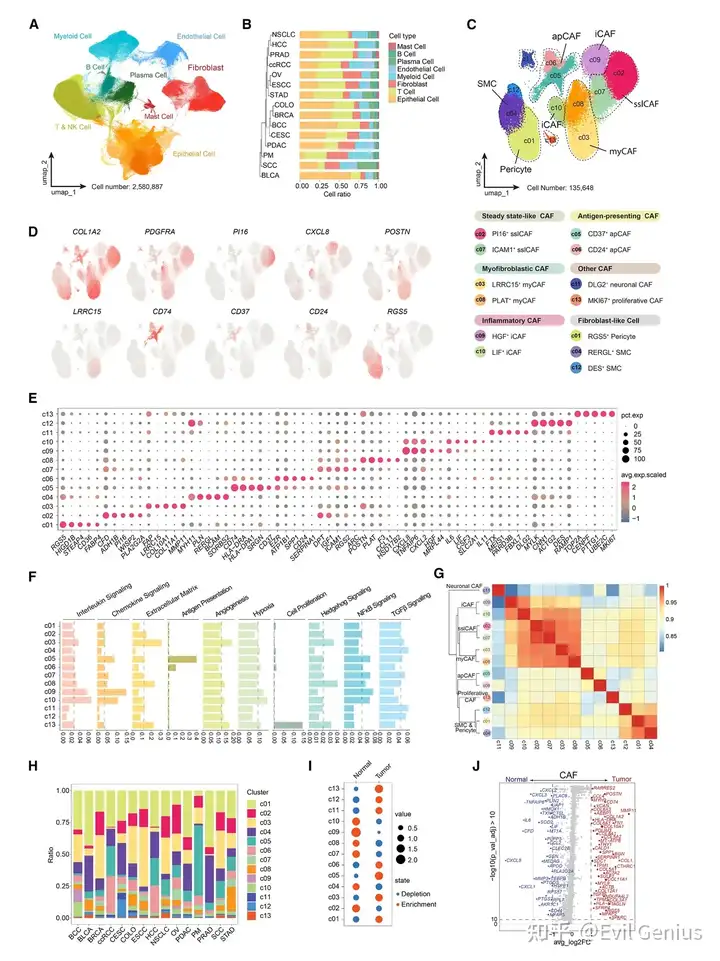
单细胞RNA测序跨癌种数据集。通过滤除检测基因数<200或>6000的细胞、线粒体UMI占比>15%的细胞,实施了严格的质量控制。同时去除在<3个细胞中检测到的基因并排除潜在双细胞。经过批次效应校正与整合聚类,最终构建了包含532个样本、逾250万个细胞的高质量单细胞图谱。
根据特征标记与信号通路,这些成纤维细胞形成6大亚型:iCAFs(c09、c10)、myCAFs(c03、c08)、apCAFs(c05、c06)、稳态样CAFs(sslCAFs,c02、c07)、神经元样CAFs(c11)和增殖性CAFs(c13)。iCAFs高表达炎症基因(CXCL2、CXCL8、IL6),富集白细胞介素/趋化因子/NFkB信号及缺氧特征。myCAFs表达POSTN与MMP11,具细胞外基质与Hedgehog信号特征(c03以LRRC15为标记,c08以PLAT为标记)。值得注意的是,常见活化CAF标记ACTA2与FAP并不具myCAF特异性。研究发现两个稳定的apCAF亚群(c05、c06),均以HLAⅡ类基因(CD74、HLA-DRA、HLA-DPA1)及抗原呈递功能为特征,其中c05特异性表达SRGN、CD37和C1Q基因,c06则表达CD24与SERPINA1。sslCAFs表达通用驻留成纤维细胞标记DPT与CD34,其中c02同时表达祖细胞标记PI16,可能作为iCAFs与myCAFs的前体细胞。
两个次要亚群中,c11呈现神经元特征(DGL2、PIEZO2),c13具增殖特性(MKI67)。TGFβ信号在c03 myCAFs、c07 sslCAFs、c11神经元样CAFs及平滑肌细胞中活性最高。
与正常组织相比,肿瘤中的成纤维细胞整体呈现肌纤维母细胞与抗原呈递特征增强、炎症特征减弱的表现。
结果2、两种不同抗原呈递癌症相关成纤维细胞群体的鉴定
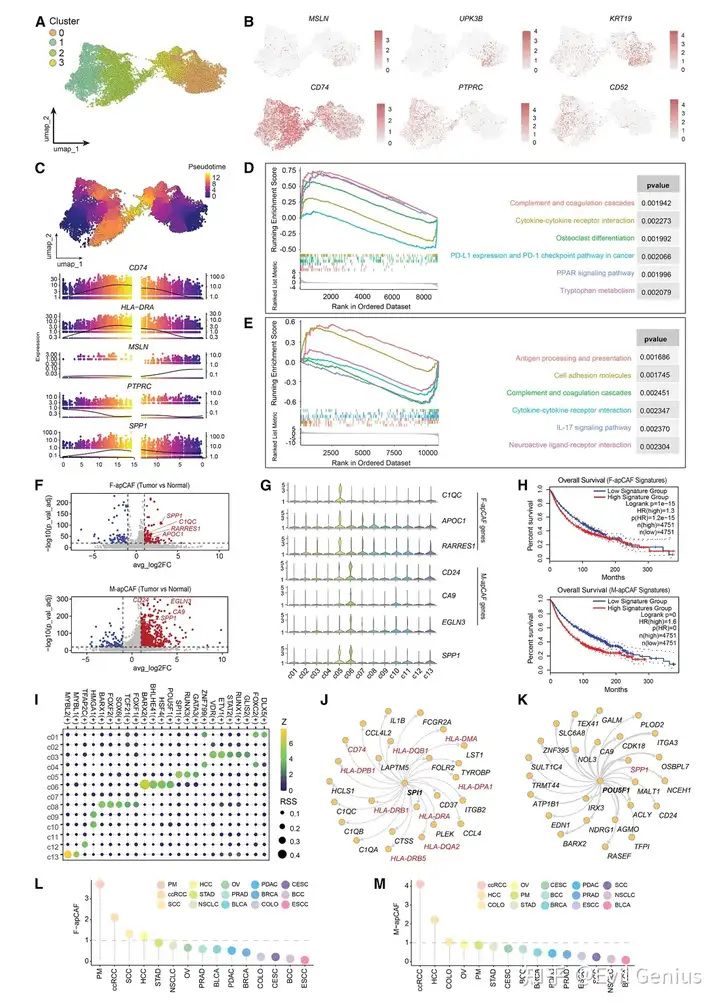
为深入探究两种apCAF群体的起源与分子特征,从图谱中提取c05和c06细胞进行重新聚类分析,结果显示其由4个亚群构成的两个独立群体。其中一个群体(cluster0、3)携带以间皮基因(MSLN、UPK3B、KRT19)为标志的间皮样特征。此外,该群体还表达CD24——一种新近报道的天然免疫检查点,参与调控细胞干性与分化。
对比发现,另一apCAF群体(cluster1、2)具有纤维细胞特征。已知纤维细胞源于造血系统,能同时表达CD45等造血标记及细胞外基质蛋白等成纤维标记,并可迁移至伤口部位促进炎症与纤维化反应。分析发现纤维细胞样apCAFs高表达多种造血基因,如PTPRC(编码CD45)、CD37和CD52。据此,本研究将间皮相关群体命名为M-apCAFs,纤维细胞相关群体命名为F-apCAFs。
拟时序分析显示apCAF群体存在两条不同的动态转化轨迹。沿轨迹方向,M-apCAFs中MSLN表达下调,F-apCAFs中PTPRC表达下调,同时伴随HLAⅡ类基因(CD74、HLA-DRA)的上调。通路分析表明F-apCAFs与M-apCAFs均深度参与免疫调节活动。然而,两种apCAF群体均缺乏CD40、CD80、CD86等主要共刺激分子的表达,这与在小鼠PDAC模型中的发现一致——apCAFs能呈递抗原但缺失共刺激信号,从而导致调节性T细胞的诱导。
通过比较两种apCAF群体在正常与癌组织中的差异表达基因,鉴定出F-apCAFs最具特异性的三个基因(C1QC、APOC1、RARRES1)及M-apCAFs特异性基因(CD24、CA9、EGLN3)。这两种三基因特征均与癌症患者不良预后显著相关。值得注意的是,SPP1在两种apCAF群体中普遍上调,且其表达水平显著高于其他CAF亚群。沿拟时序轨迹,两种apCAF群体中SPP1表达均持续增加,其高表达亦是患者生存的强负向预后标志。
为解析apCAFs的调控网络,开展SCENIC分析,发现驱动F-apCAFs(SPI1、RUNX3、GATA3)与M-apCAFs(BARX2、BHLHE41、HSF4、POU5F1)基因程序的特异性转录因子。这些转录因子可能直接调控关键apCAF特征的转录,例如SPI1可能调控F-apCAFs中HLAⅡ类基因(CD74、HLA-DRA等)的转录,而调控干性的主要转录因子POU5F1(编码OCT4)可能调节M-apCAFs中SPP1的表达。
进一步分析两种apCAF群体在各类癌症中的丰度,发现F-apCAFs在腹膜转移瘤、肾透明细胞癌、鳞状细胞癌、肝细胞癌和胃癌中富集度最高,M-apCAFs则在肾透明细胞癌、肝细胞癌、结直肠癌、卵巢癌和腹膜转移瘤中最为富集。基于此,后续研究选择腹膜转移瘤作为深入解析apCAFs的关键模型。
结果3、腹膜转移瘤的基质异质性
腹膜是由间皮细胞、成纤维细胞、内皮细胞及免疫细胞等多种基质细胞构成的复杂组织。这种特殊微环境可能促进转移过程中apCAFs的形成。结肠癌是腹膜转移最常见起源之一,约20%结肠癌患者会发生腹膜转移。根据上皮发育程序,原发结肠癌细胞可分为两种内在上皮表型(iCMS2和iCMS3)。因此,腹膜转移瘤很可能也源于两种不同癌细胞系,并具有异质性基质。
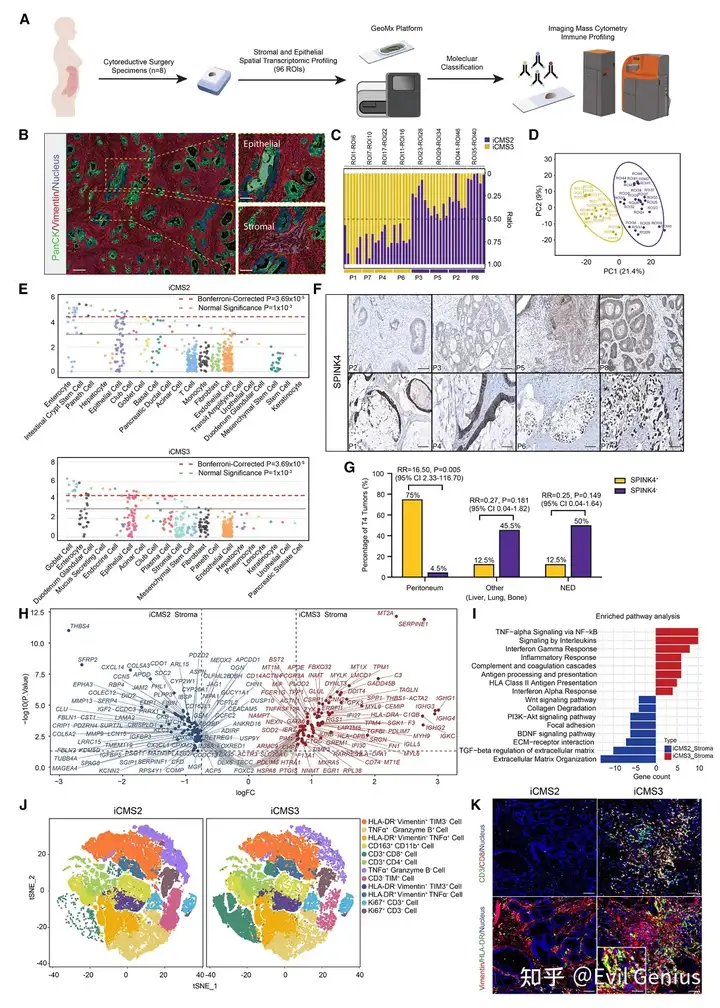
通过Nanostring GeoMx全转录组空间RNA分析,分析肿瘤上皮区与邻近基质区的分子特征
对上皮感兴趣区域(ROIs)特征进行解卷积与主成分分析,揭示出两种分子亚型:iCMS2样与iCMS3样。细胞类型特异性富集分析显示iCMS2上皮细胞类似肠上皮细胞,而iCMS3上皮细胞类似杯状细胞,表明腹膜转移癌细胞中存在两种细胞系程序。
采用成像质谱流式技术分析发现,iCMS3腹膜转移中T细胞与HLAⅡ阳性/Vimentin阳性基质细胞呈现增多趋势。在更大规模腹膜转移样本中验证了T细胞数量变化,进一步支持iCMS3腹膜转移具有更强免疫活性。
结果4、F-抗原呈递癌症相关成纤维细胞生态位的空间分析
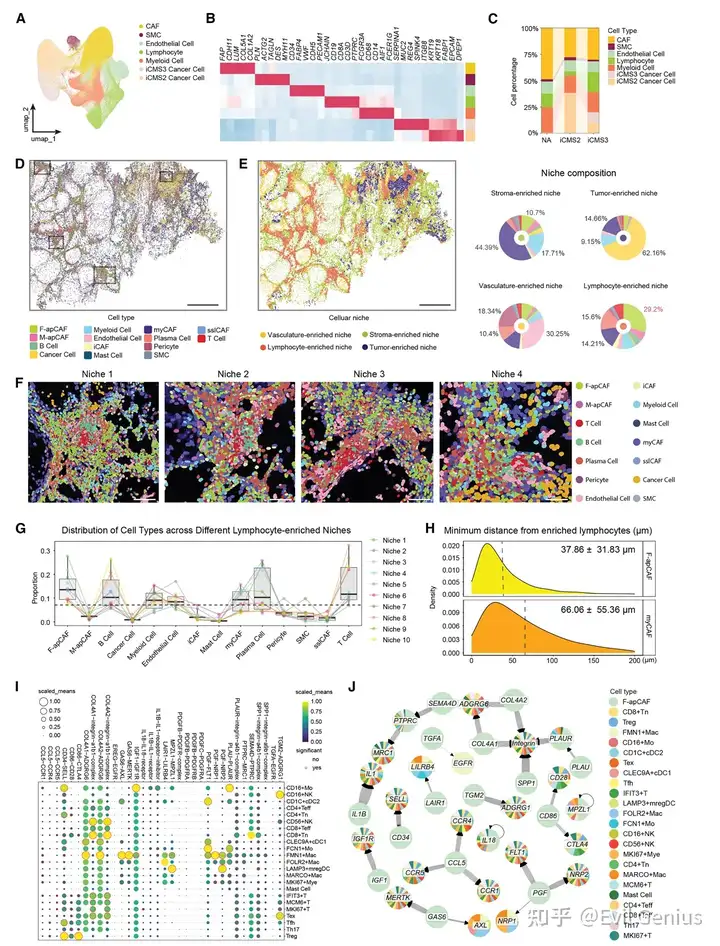
为在单细胞分辨率下解析apCAFs的空间分布及相关生态位,采用Xenium原位高通量空间成像平台,基于已构建的单细胞RNA测序图谱定制了包含480个基因的探针 panel。对8例结肠源腹膜转移样本(含1例癌旁组织)进行Xenium检测,共获得799,455个高质量细胞。无监督聚类分析成功鉴定主要细胞类型:CAFs、平滑肌细胞、内皮细胞、淋巴细胞、髓系细胞及iCMS2/iCMS3癌细胞。
通过基于泛癌单细胞图谱构建的参照系统,对空间转录组数据进行稳健细胞类型解卷积及生态位组成分析。在淋巴细胞浸润显著的iCMS3样本中,鉴定出四种特征性空间生态位:血管富集区、淋巴细胞富集区、基质富集区与肿瘤富集区。生态位组成分析显示:基质区与肿瘤区以myCAFs和髓系细胞为主,血管区主要由内皮细胞和周细胞构成;而淋巴细胞富集区中F-apCAFs占比最高。为验证该空间关联,在含iCMS3癌细胞的样本中选取10个淋巴细胞富集区进行细胞类型定量,确认F-apCAFs是该区域最主要的CAF亚型。
针对F-apCAFs共表达造血标记与成纤维细胞标记的特性,通过三重验证确认其独特细胞身份:
与泛癌图谱中主要免疫细胞群(巨噬细胞、单核细胞、树突状细胞、B细胞、浆细胞、T细胞)对比显示,F-apCAFs虽表达PTPRC(CD45),但特异性高表达成纤维细胞标志基因(COL1A2、COL1A1、COL3A1、PDGFRA),而免疫细胞群完全不表达这些基因;
与脾脏纤维细胞研究中提取的滤泡树突状细胞标记基因对比,发现F-apCAFs与M-apCAFs均不表达CXCL13、SPIB、CR2、CCL19等特征基因,明确排除其滤泡树突状细胞属性;
通过多重免疫组化验证淋巴细胞富集区中PDGFRα+HLA-DRA+CD45+ F-apCAFs的存在。
这些证据共同确立F-apCAFs为兼具造血系标记与功能性成纤维细胞特征的独特纤维细胞样群体。
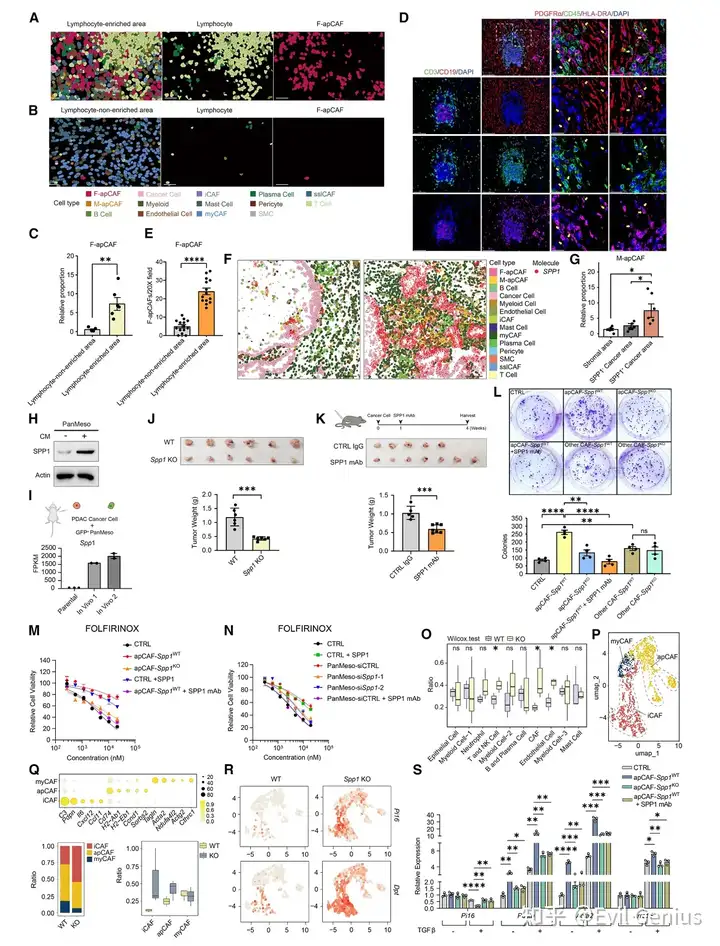
尽管myCAFs在淋巴细胞富集区也占相当比例,但F-apCAFs具有更高密度且与淋巴细胞团距离更近(平均距离37.86μm vs. 66.06μm)。为探究F-apCAFs与免疫细胞的相互作用,先从泛癌单细胞图谱中鉴定髓系与淋巴细胞亚群,再通过配体-受体互作分析发现F-apCAFs来源的配体与免疫细胞受体间存在多条重要信号通路。例如:趋化因子CCL5可能介导T细胞/单核细胞招募;同时检测到免疫抑制基因SPP1与LAIR1,提示F-apCAFs在炎症性肿瘤中具有复杂功能。
结果5、M-抗原呈递癌症相关成纤维细胞生态位的空间分析
与F-apCAFs相比,M-apCAFs呈现更强的环境依赖性空间分布特征。由于腹膜表面由间皮细胞覆盖,癌细胞转移至该部位可能通过直接间皮相互作用诱导M-apCAF形成。M-apCAFs表达细胞角蛋白基因,免疫组化染色显示细胞角蛋白阳性CAFs浸润于PM基质,通常定位于细胞角蛋白阳性间皮层附近。通过癌细胞标记物(SPINK4)与CAF标记物(PDGFRα)的多重免疫组化证实这些CAFs非癌细胞来源
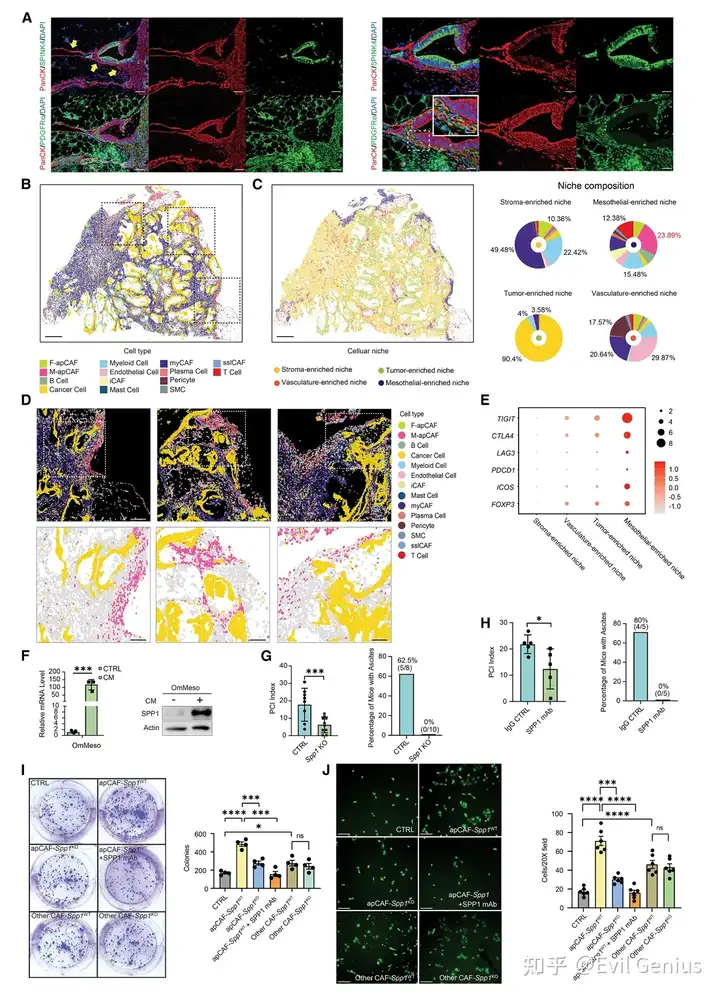
在具有显著细胞角蛋白阳性CAF浸润的样本中,空间转录组细胞类型解卷积与生态位组成分析鉴定出独特的间皮富集生态位,以及基质富集、血管富集和肿瘤富集生态位。这些间皮生态位以M-apCAFs(23.89%)、髓系细胞(15.48%)和T细胞(12.38%)为主要基质组分。部分间皮富集生态位与正常间皮层(以MSLN、UPK3B为标记)保持连续,提示间皮向M-apCAF分化过程。大多数间皮富集生态位与肿瘤上皮相邻,表明M-apCAFs可能与免疫细胞及癌细胞密切相互作用。
研究发现间皮富集生态位内的T细胞高表达抑制性标记(TIGIT、CTLA4、LAG3、PDCD1、ICOS、FOXP3)。进一步的配体-受体互作分析提示SPP1是介导M-apCAFs与免疫细胞或癌细胞相互作用的关键配体。
宿主分泌性磷蛋白1基因敲除导致腹膜转移与腹水形成减少
SPP1(骨桥蛋白)是一种高度磷酸化的分泌蛋白,通常在骨骼中作为细胞外结构蛋白发挥作用。在创伤和癌症环境中,SPP1作为急性期蛋白上调表达,与炎症和纤维化反应相关。在癌症中,SPP1通过促进癌细胞可塑性与化疗耐药、作为T细胞免疫检查点等机制发挥多效性促瘤功能,但其在PM中的作用未知。
有趣的是,观察到iCMS3型PM往往具有更高水平的基质来源SPP1,这可能与该PM亚型的腹膜定向转移特性相关。SPP1可由癌细胞、髓系细胞和CAFs表达。事实上,前期乳腺癌研究已报道apCAFs是重要SPP1生产者。计算数据进一步表明apCAFs是CAF亚型中SPP1的主要来源。通过检测MC38鼠结肠癌细胞建立的体内PM结节中癌细胞(EpCAM+)、髓系细胞(CD11b+)、apCAFs(PDGFRα+MHCII+)及其他CAFs(PDGFRα+MHCII-)的总SPP1与分泌型SPP1表达,验证发现apCAFs产生的SPP1水平显著高于其他基质细胞。此外,用肿瘤条件培养基处理正常小鼠大网膜来源间皮细胞(OmMeso细胞)后,观察到OmMeso细胞中SPP1表达显著升高。
为验证SPP1对癌细胞迁移与侵袭的影响,采用划痕实验与基质胶侵袭实验发现:添加SPP1蛋白显著增强MC38细胞迁移侵袭能力,而抗SPP1单克隆抗体则抑制该过程。通过向野生型与Spp1基因敲除小鼠腹腔注射MC38细胞,发现宿主Spp1敲除显著减少PM与腹水形成。该表型在抗SPP1单抗治疗PM荷瘤野生型小鼠实验中得到重现。为评估apCAF来源SPP1的重要性,使用MC38细胞在野生型与Spp1敲除小鼠中建立PM结节,分离apCAFs(PDGFRα+MHCII+)及其他CAFs(PDGFRα+MHCII-)与MC38细胞共培养进行集落形成与基质胶侵袭实验。apCAFs分泌的SPP1显著增强MC38细胞的集落形成与侵袭能力,该效应可被抗SPP1单抗抑制。这些数据共同表明基质来源SPP1可能驱动PM形成,而apCAFs通过产生SPP1促进该进程。
结果6、M-抗原呈递癌症相关成纤维细胞在胰腺导管腺癌中与SPP1阳性生态位相关
研究通过整合单细胞RNA测序与高分辨率空间成像技术,系统解析了抗原呈递癌症相关成纤维细胞(apCAFs)的异质性起源与空间分布特征。研究团队构建了涵盖15种组织类型、532个样本、逾250万细胞的泛癌成纤维细胞图谱,首次鉴定出两个独立的apCAF亚群:间皮来源的M-apCAFs(表达MSLN、UPK3B等间皮标记)和造血来源的F-apCAFs(共表达PTPRC/CD45与成纤维细胞标记)。空间分析显示F-apCAFs特异性富集于淋巴细胞区域,通过分泌CCL5等趋化因子招募免疫细胞;而M-apCAFs则定位于肿瘤-间皮交界区,与免疫抑制性T细胞(高表达TIGIT、CTLA4等检查点)形成免疫抑制微环境。
抗原呈递癌症相关成纤维细胞来源的分泌性磷蛋白1促进胰腺导管腺癌纤维化屏障形成
关键机制研究发现两个apCAF亚群均高表达分泌性磷蛋白1(SPP1)。在胰腺导管腺癌和腹膜转移模型中,证实apCAFs是基质SPP1的主要来源:通过基因敲除实验显示宿主Spp1缺失可显著抑制肿瘤进展与腹水形成;抗体阻断实验进一步验证SPP1能促进癌细胞侵袭、化疗抵抗及肌纤维母细胞分化。单细胞转录组分析揭示SPP1缺失导致肿瘤微环境重塑——myCAFs比例下降而稳态样CAFs增加,伴随T细胞浸润显著增强。
最后来看看方法
单细胞部分


Xenium部分

生活很好,有你更好
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
评论
登录后参与评论
推荐阅读
目录

