文章分享---化疗诱导卵巢癌骨髓驱动的空间限制性T细胞衰竭
原创文章分享---化疗诱导卵巢癌骨髓驱动的空间限制性T细胞衰竭
原创
追风少年i
发布于 2024-12-10 15:45:13
发布于 2024-12-10 15:45:13
作者,Evil Genius
现在都卷起来了,失业的情绪蔓延开来。AI的时代来的太快了。
生物信息这行业,不知道还能做多久。
人只会倒霉一时?还是一直会这样?
今日参考文献
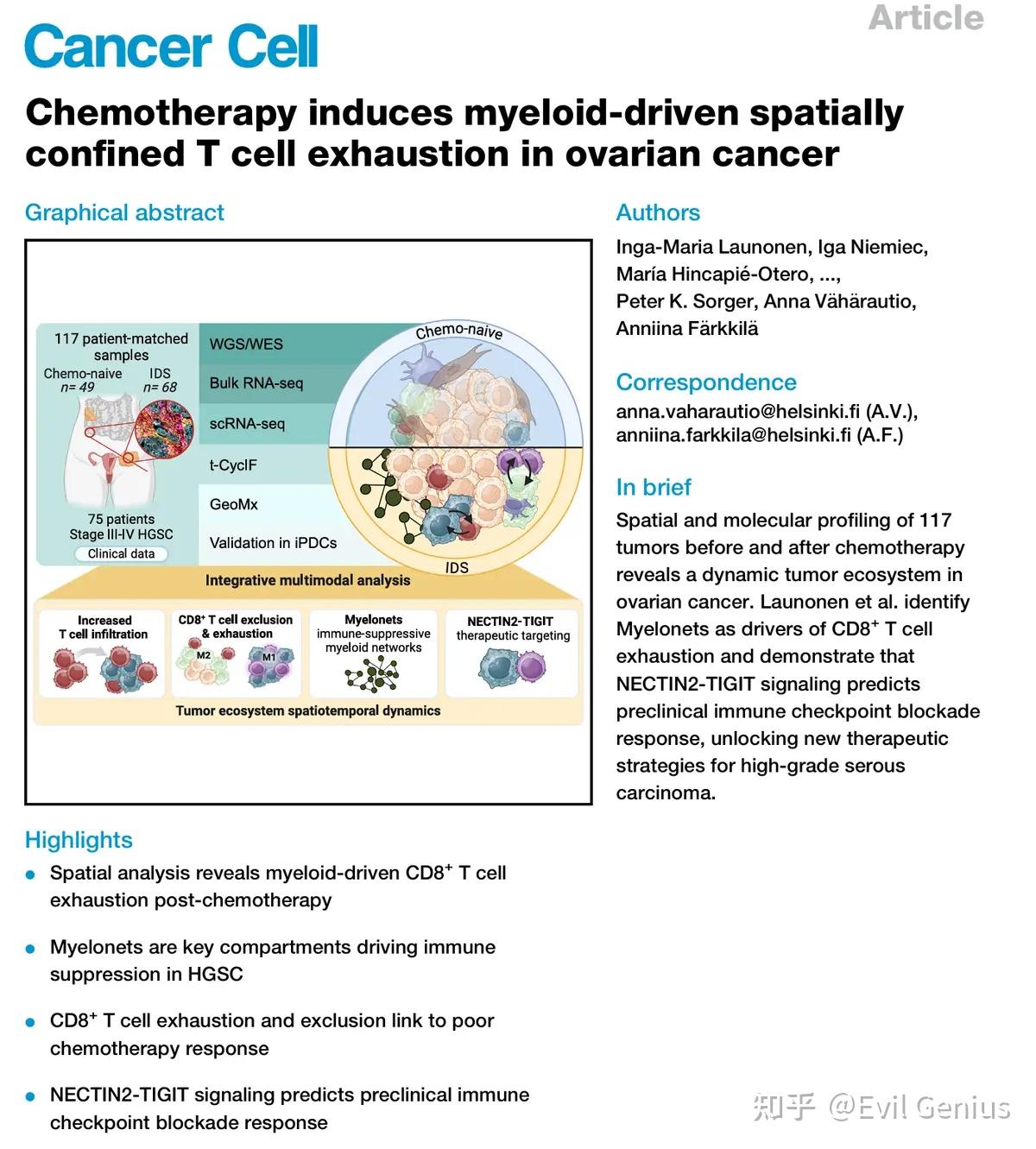
抗肿瘤免疫对高级别浆液性卵巢癌(HGSC)的预后至关重要,但其对标准化疗的适应性仍知之甚少。对化疗前后采集的117份HGSC样本进行了空间和分子表征。单细胞和空间分析揭示了越来越多的免疫细胞状态形成时空动态微群落。
知识积累
- 肿瘤发生和癌症进展依赖于恶性细胞通过细胞群之间复杂的空间相互作用逃避宿主免疫系统。
- 高级别浆液性卵巢癌(HGSC)是最常见的卵巢癌亚型,是一种高度侵袭性疾病,其特征是TP53普遍存在有害突变,基因组不稳定,肿瘤异质性高,缺乏复发性基因组改变一线新辅助化疗(NACT)通常用于无法切除的疾病或合并症患者。无论对一线铂类化疗的反应如何,大多数患者最终都会出现治疗耐药。
- 抗肿瘤免疫在HGSC治疗反应和临床结果中起着关键作用,但标准化疗如何调节它却知之甚少。
- 空间定位决定细胞表型,空间相互作用在肿瘤细胞如何逃避免疫攻击中起着至关重要的作用。
- ICBs的疗效取决于具有不同激活状态的相邻细胞之间的空间相互作用。
- ICB和PARP抑制剂的反应受功能和空间免疫微环境的影响。
- 为了加强卵巢癌的治疗,深入了解化疗期间肿瘤生态系统重塑的空间动力学是必不可少的。
- 结合了多组学分析,使用基因组学、单细胞RNA测序(scRNA-seq)、高维组织成像和空间转录组学,从117例患者样本中捕获了超过2500万个单细胞和316个空间转录组结构域。通过结合铂基化疗前后收集的患者匹配HGSC样本的基因组、单细胞和空间数据,分析了在NACT期间,空间分解的细胞-细胞相互作用邻域和转录程序是如何动态变化的,从而导致可靶向的、髓细胞驱动的空间受限T细胞衰竭模式。
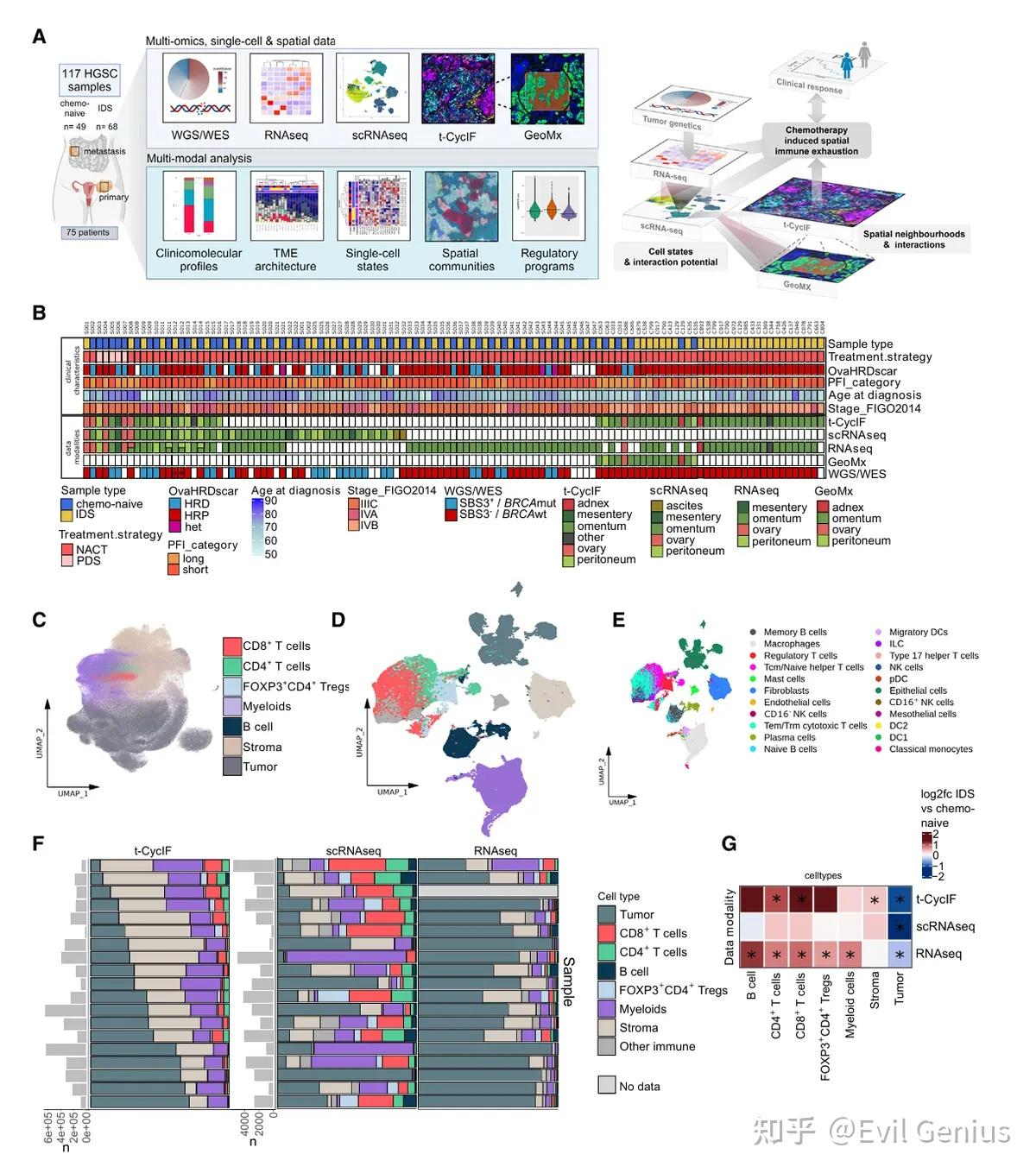
结果1、多组学特征显示NACT期间免疫浸润增强
整体免疫TME组成在化疗过程中并不稳定。化疗驱动的免疫TME的浸润和激活普遍增强,而不是患者特异性的初始TME组成。
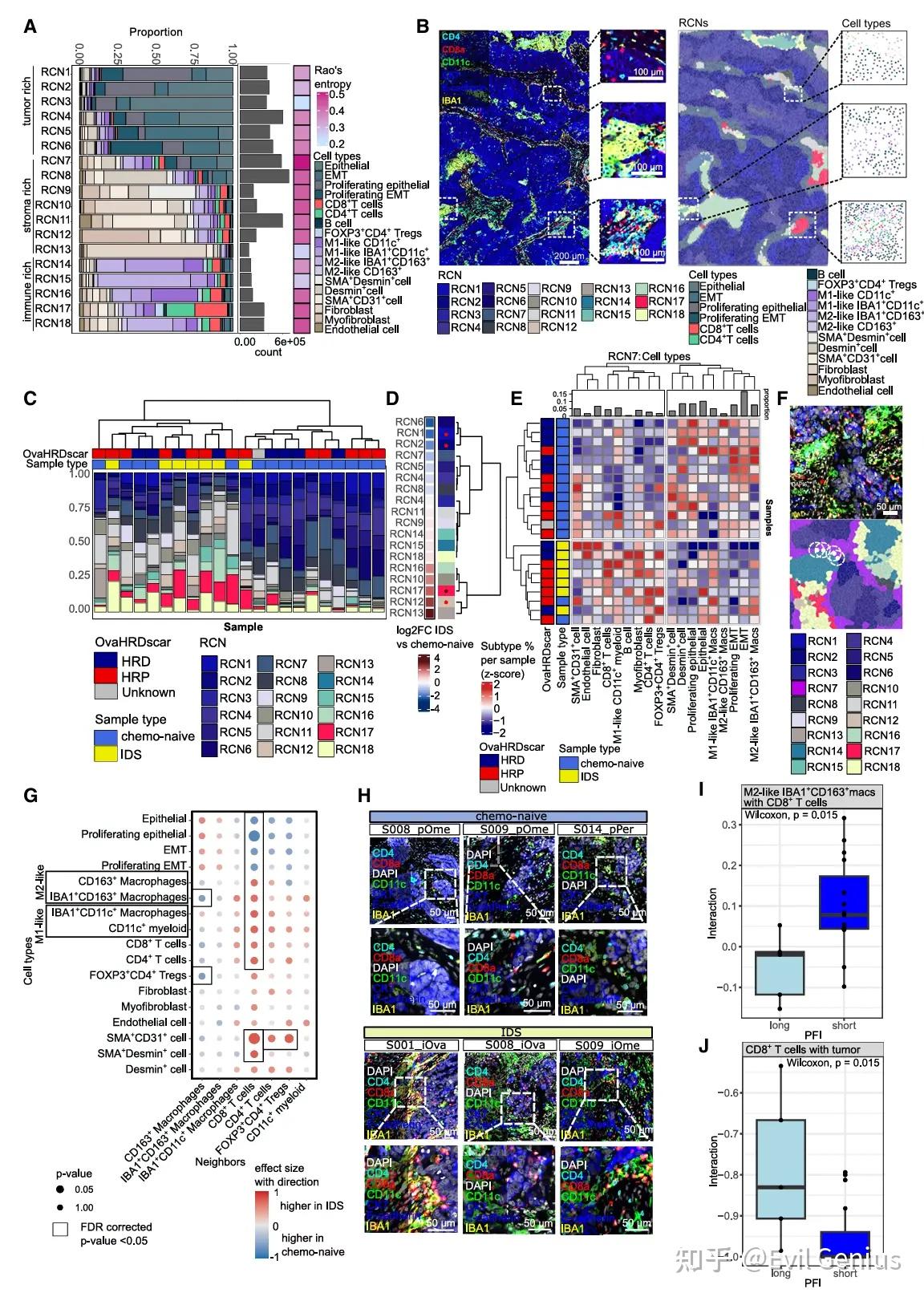
结果2、化疗驱动TME的空间景观变化
为了系统地分析HGSC TME内细胞群落的空间景观,通过细胞型邻域矩阵聚类标注了18个不同的空间cluster或复发细胞邻域。
邻域的细胞富集程度。
对样本中每个RCN细胞类型比例的分层聚类来评估化疗的效果。
空间邻域RCN7 (TSI)具有最高的多样性和相互作用潜力,对化疗期间的变化反应最敏感。化疗导致TSI处CD8+ T细胞和髓样细胞之间的相互作用增加,其中M2样相互作用与治疗反应较短相关。相反,持续的CD8+ T细胞与肿瘤细胞相互作用与M2样巨噬细胞相互作用相互排斥,并与延长的PFI相关。总之,这些结果表明,M2样巨噬细胞相互作用限制了CD8+ T细胞与肿瘤细胞的相互作用,导致预后不良。
结果3、髓细胞相互作用塑造CD8+ T细胞表型
化疗期间CD8+ T细胞和骨髓细胞的空间和功能动态,化疗促进了RCN内CD8+ T细胞的空间重新分布。
化疗诱导CD8+ T细胞在髓系rcn以及许多间质和肿瘤RCN上的浸润显著增加。随着NACT后浸润的增加,浸润的CD8+ T细胞表现出明显的耗竭(TIM3+)表型和降低的激活状态(pSTAT1+),表明T细胞耗竭是受空间控制的。
化疗诱导从空间受限的免疫表型到免疫浸润的TME的转变。
NACT在TME中诱导了空间限制性的激活和耗竭模式,在NACT之前,耗竭的TIM3+ CD8+ T细胞主要位于tumor islets,而在NACT之后,它们向髓系附近转移。
巨噬细胞和CD8+ T细胞之间功能相关的空间串扰,导致NACT期间CD8+ T细胞的激活和衰竭增强。
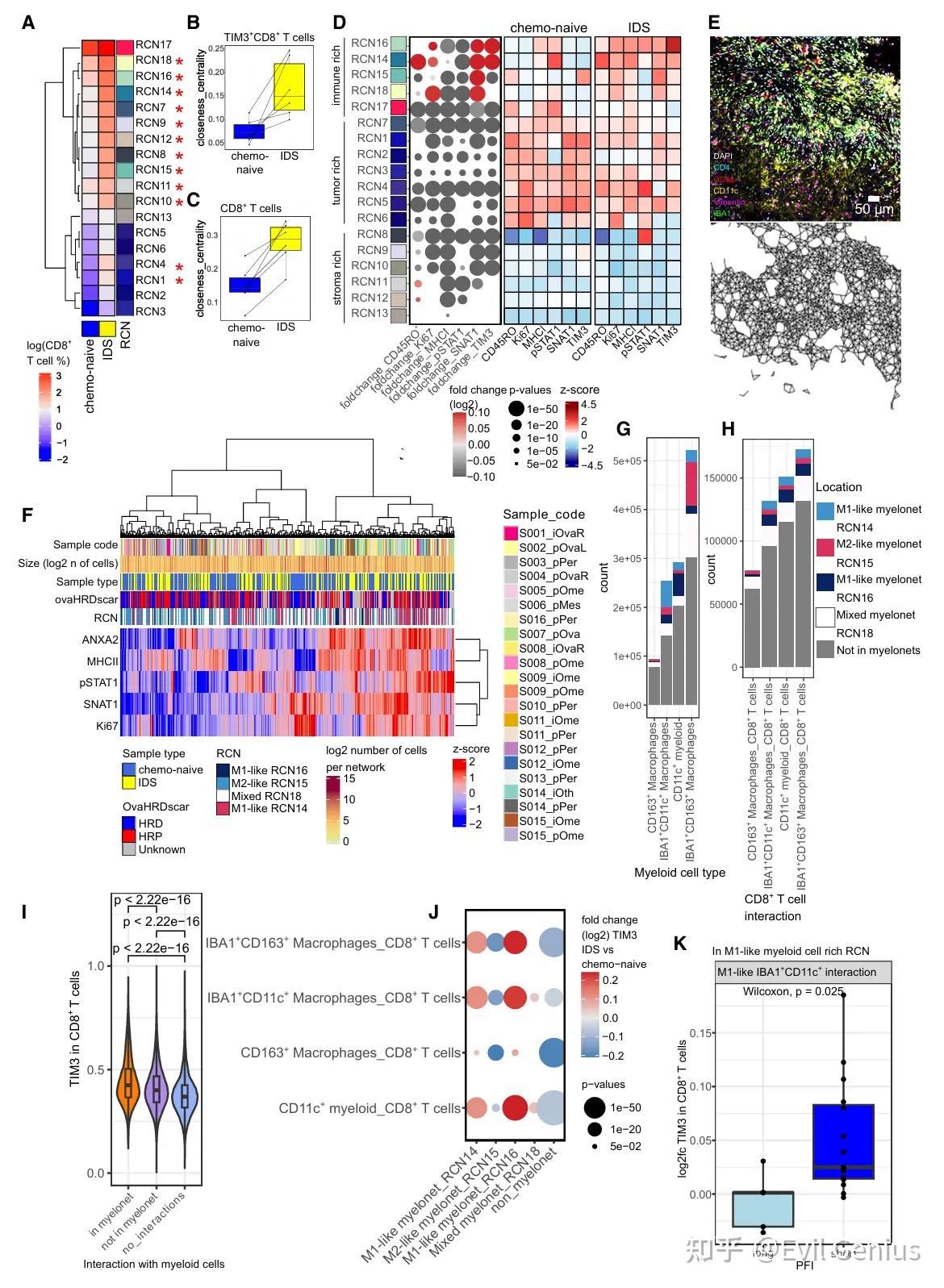
结果4、髓细胞-髓细胞亚群相互连接的功能网络
骨髓细胞经常形成空间簇。使用Delaunay聚类,识别具有直接细胞接触的细胞,发现了空间结构“髓系网”,它形成了由9个以上相互连接的髓系细胞组成的相互连接的髓系网络。
髓细胞是T细胞-髓细胞相互作用的中心枢纽,驱动T细胞衰竭,并在化疗暴露的HGSC TME中导致化疗反应差。
结果5、化疗增强了巨噬细胞和CD8+ T细胞的相互作用潜力
化疗后巨噬细胞出现新的状态,表明其多功能性增加。
细胞之间的通讯分析。
肿瘤的基因组特征、突变变化或患者对化疗的反应都不能解释NACT诱导的免疫调节配体受体动力学。
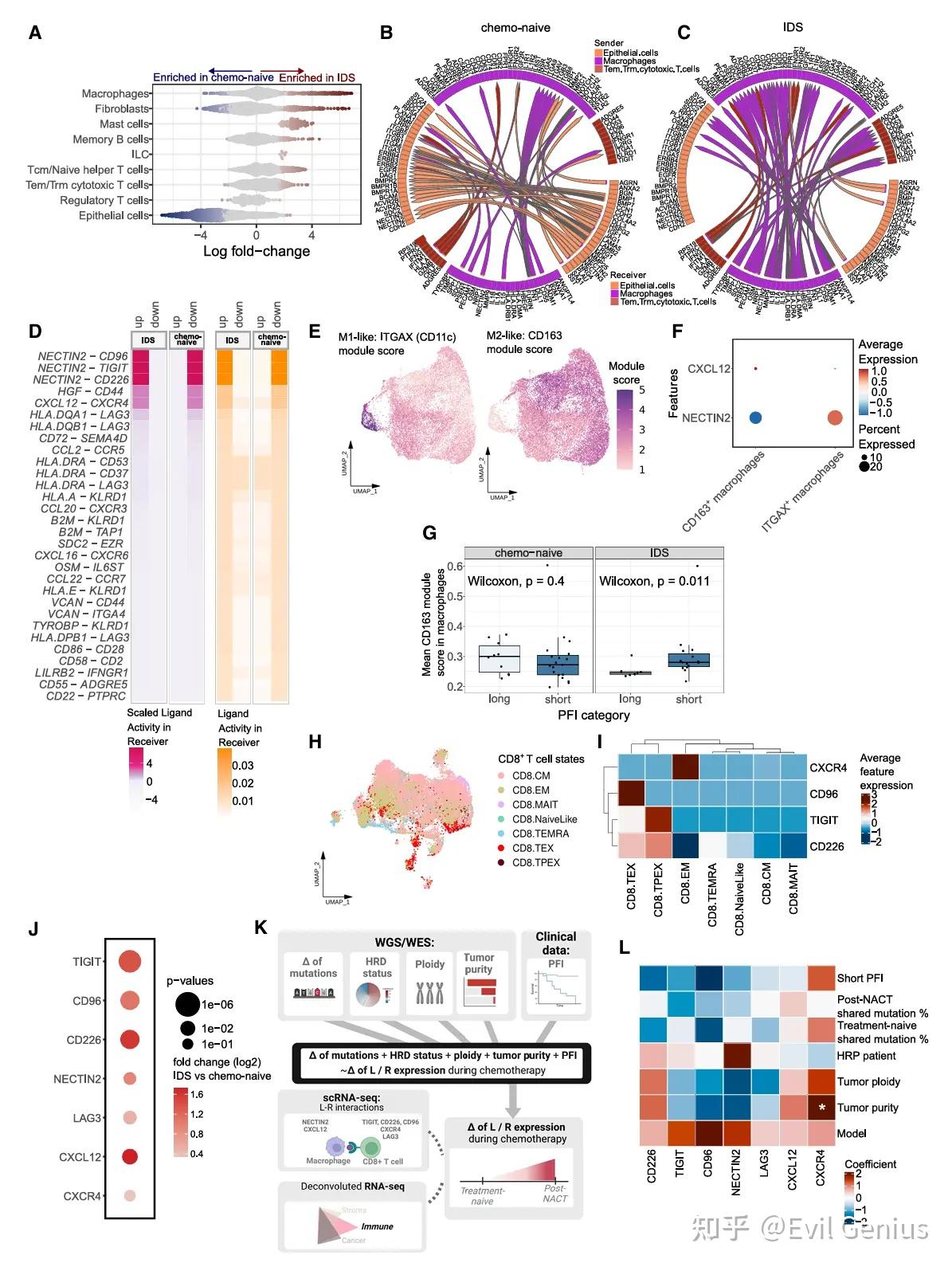
结果6、空间骨髓- T细胞串扰的转录决定因素
化疗诱导了突出的M1极化与TSI处耗尽的CD8+ T细胞共定位。
综合空间转录组学分析表明,化疗驱动激活的、高度抗原呈递的、NECTIN2+、M1样巨噬细胞,以及细胞毒性但耗尽的、免疫检查点阳性的CD8+ T细胞与肿瘤周围基质内的巨噬细胞共定位。
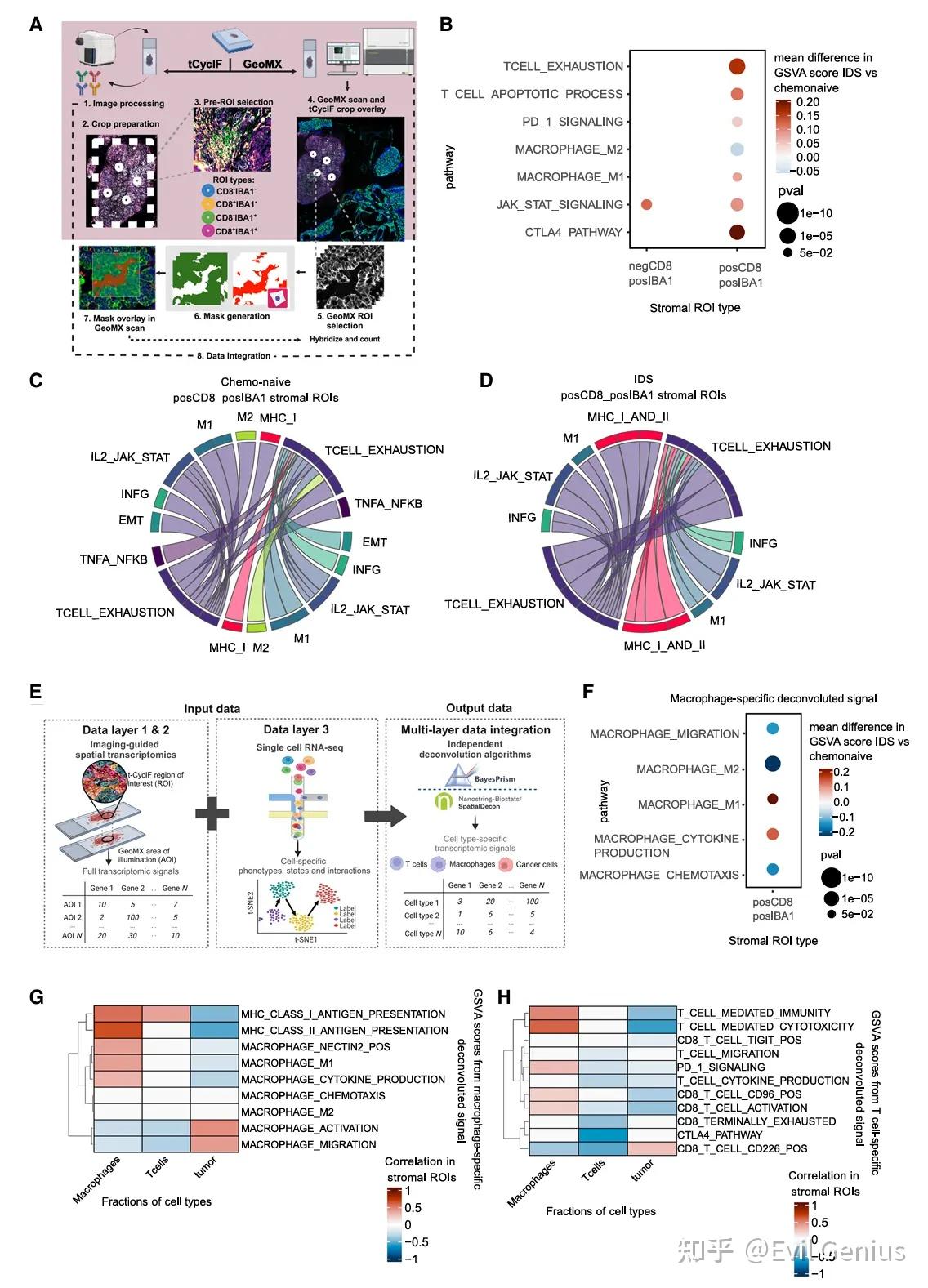
结果7、靶向化疗诱导的TIGIT-NECTIN2与ICB的相互作用增强了CD8+ T细胞的活化
在HGSC中,巨噬细胞驱动的CD8+ T细胞耗竭可以有效地靶向ICB,特别是在化疗后给药时。此外,这些治疗的益处似乎与肿瘤中NECTIN2-TIGIT信号环的存在存在内在联系。
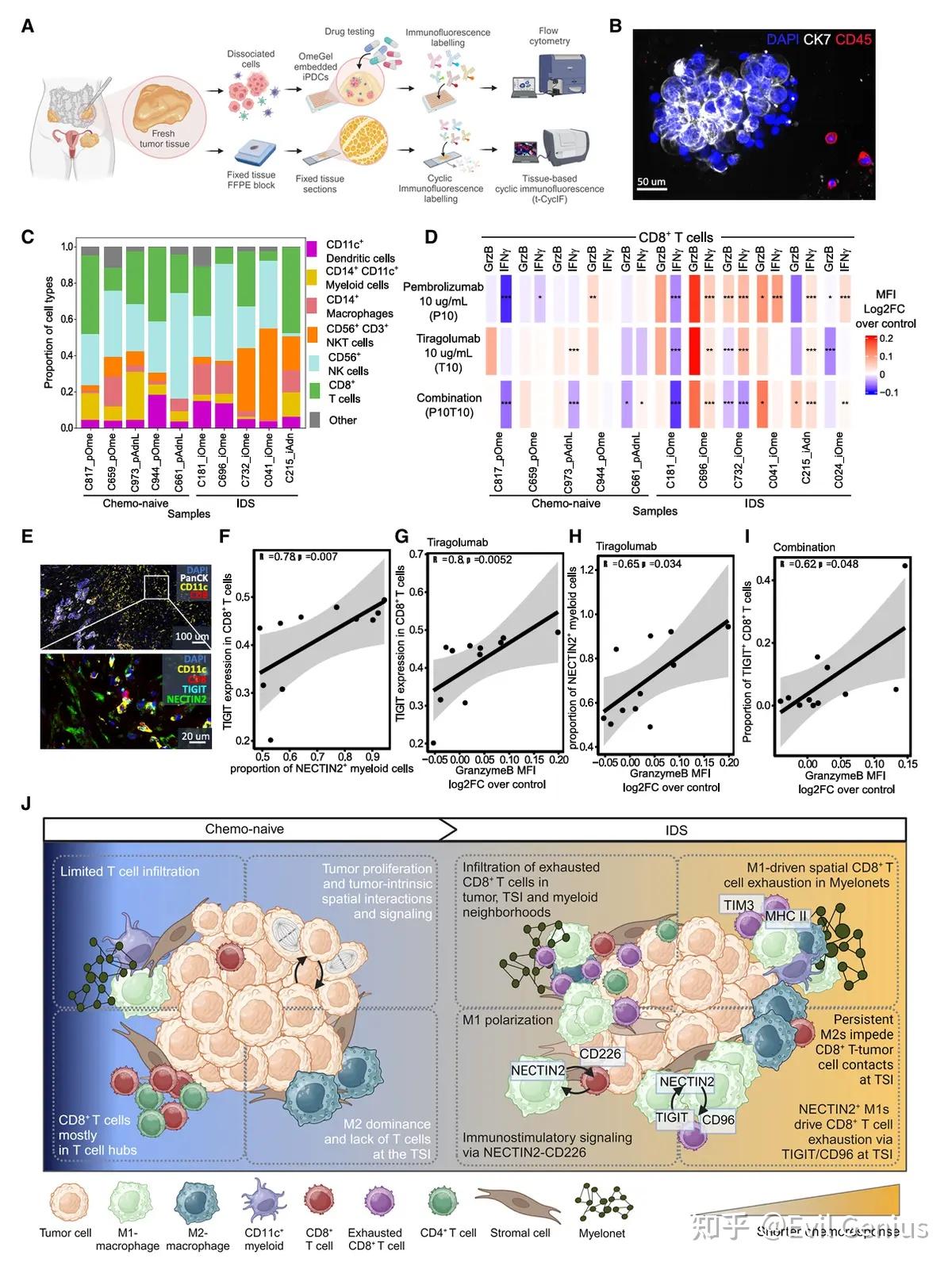
生活很好,有你更好
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
评论
登录后参与评论
推荐阅读
目录

