AI驱动的抗结核抑制剂发现:MenT3毒素抑制剂的计算筛选研究
AI驱动的抗结核抑制剂发现:MenT3毒素抑制剂的计算筛选研究

DrugIntel
发布于 2026-04-28 13:02:04
发布于 2026-04-28 13:02:04

标题: Identification of potential MenT3 inhibitors for Mycobacterium tuberculosis using the generative artificial intelligence and SilicoXplore platform 作者: Ibrahim A. Alsarra, Vikramsinh Sardarsinh Suryawanshi, Abdullah M. Al-Mohizea, Pritee Chunarkar Patil, Rupesh Chikhale, Md Ataul Islam 期刊:Scientific Reports DOI:10.1038/s41598-026-49174-y
一、研究背景与科学问题
1.1 结核病的全球威胁与耐药危机
根据WHO 2024年全球结核病报告,结核病(Tuberculosis, TB)已重新成为全球单一传染性病原体致死的首位疾病,每年感染人数超过1000万,且自2021年起病例数持续上升。结核分枝杆菌(Mycobacterium tuberculosis, Mtb)的致病能力与其独特的细胞壁结构密切相关:
- • 分枝菌酸(Mycolic acid):以共价键连接于肽聚糖-阿拉伯半乳聚糖复合体上,形成高度疏水的脂质屏障,显著降低抗生素渗透效率
- • 脂阿拉伯甘露聚糖(Lipoarabinomannan, LAM):外层多糖抗原,帮助Mtb在宿主巨噬细胞内存活
更严峻的是,耐多药结核(MDR-TB)和广泛耐药结核(XDR-TB)的出现使现有一线药物(异烟肼、利福平等)的疗效大幅降低,开发针对新靶点的抗结核药物已成为全球公共卫生的迫切需求。
1.2 毒素-抗毒素系统:被低估的药物靶点
细菌毒素-抗毒素(Toxin-Antitoxin, TA)系统是一类广泛存在于细菌基因组中的双组分调控模块,参与调控:
复制 · 转录 · 翻译 · 应激反应 · 生物膜形成 · 细胞存活
在正常生理条件下,抗毒素(Antitoxin)与毒素结合并中和其活性;在宿主胞内缺氧、营养匮乏等极端压力下,抗毒素被蛋白酶降解,毒素被释放激活,诱导细菌进入持留(persistence)状态。
Mtb基因组编码了数十个TA系统,这种持留状态被认为是结核潜伏感染和抗生素耐药的核心机制之一。
1.3 MenT3:一个精妙的分子靶点
本研究聚焦的MenT3(Mycobacterial nucleotidyltransferase Toxin 3)是Mtb TA系统中的一个核苷酸转移酶毒素,其作用机制高度特异:
分子机制: MenT3通过将CMP(胞苷一磷酸)共价添加至tRNA^Ser的3'-CCA氨基酸受体末端,使该tRNA无法被氨酰化(aminoacylation),从而阻断蛋白质合成过程中的关键步骤。
生理意义:
- • 正常状态:抗毒素MenA3与MenT3结合,抑制其磷酸化及与tRNA^Ser的相互作用
- • 应激状态:MenA3降解 → MenT3激活 → 蛋白合成减慢 → 细菌节能存活
- • 遗传证据:MenT3/MenT4双基因敲除菌株在小鼠和豚鼠模型中毒力显著减弱,并能诱导保护性免疫
结构基础: MenT3晶体结构(PDB ID: 8XHR,分辨率2.10 Å)揭示其由两个结构域组成:
- • N端结构域:反平行β-折叠,含三个潜在催化羧酸基团(D/D/E motif)
- • C端结构域:五个α-螺旋
天然底物CTP(胞苷三磷酸)结合于两个结构域之间的裂隙,形成广泛的氢键网络:
磷酸基团 | 相互作用残基 |
|---|---|
α-磷酸氧 | K79, R205(氢键) |
β-磷酸氧 | K189, H207(氢键) |
γ-磷酸氧 | R76, H207(氢键) |
核糖2'-OH | E188(氢键) |
胞嘧啶碱基 | M122(π堆叠),P120羰基氧,R238(N3/O2) |
这一高度保守的结合位点为竞争性抑制剂设计提供了理想的分子基础。
二、研究方法:多层级计算筛选管线
本研究构建了一条集生成式AI、机器学习ADMET预测、药效团建模、分子对接、分子动力学模拟、结合自由能计算和量子化学计算于一体的完整药物发现管线,依托SilicoXplore云平台实现一站式执行。
整体工作流程如下:
REINVENT4 de novo生成
↓(100,000个分子)
ADMET-AI药代动力学过滤
↓(11,655个分子)
PharmacoNet药效团筛选
↓(1,724个分子)
AutoDock Vina三轮对接
↓(1,481个分子)
SimSearch相似性筛选(Tanimoto ≥ 0.5)
↓(59个分子)
吡嗪环结构过滤
↓(14个分子)
20 ns MD模拟 + MM-GBSA初筛
↓(Top 5分子)
100 ns 延伸MD模拟 + 全面统计分析
↓
DFT量子化学计算(HOMO-LUMO / MEP / 反应性描述符)
↓
最终候选分子:MenT3_M1 ~ MenT3_M52.1 生成式AI分子库构建:REINVENT4
REINVENT4是一个基于Python3开发的开源生成式AI框架,核心采用循环神经网络(RNN) 结合**强化学习(RL)**驱动分子生成。其预训练模型在ChEMBL和PubChem的大规模药物样分子数据集上通过teacher forcing进行无监督预训练,学习有效SMILES字符串的语法和概率分布。
本研究采用de novo(无约束)设计模式:
- • 无需提供骨架约束文件
- • 通过逐原子序列生成全新化合物
- • 强化学习奖励函数整合多组分评分,包括:
评分组件 | 说明 |
|---|---|
QED drug-likeness | 类药性综合评分 |
Crippen SLogP | 脂水分配系数 |
MW, TPSA | 分子量与极性表面积 |
HBA/HBD | 氢键受体/供体数量 |
可旋转键数 | 柔韧性评估 |
sp³碳分数 | 三维性评估 |
PMI形状描述符 | 分子形状 |
DockStream对接评分 | 靶点亲和力 |
最终生成100,000个分子,去重后保留98,207个结构多样的类药分子。
2.2 ADMET药代动力学过滤
采用ADMET-AI(基于Chemprop-RDKit图神经网络架构)对98,207个分子进行系统药代评估,筛选标准如下:
参数 | 阈值 |
|---|---|
分子量(MW) | ≤ 500 Da |
logP | ≤ 5 |
氢键受体(HBA) | ≤ 10 |
氢键供体(HBD) | ≤ 5 |
类药性评分(QED) | ≥ 0.5 |
极性表面积(TPSA) | ≤ 150 Ų |
Ames致突变性 | ≤ 0.5 |
口服生物利用度 | ≥ 0.6 |
致癌性(Lagunin) | ≤ 0.5 |
药物性肝损伤(DILI) | ≤ 0.5 |
过滤后保留11,655个符合药代要求的无毒分子。
2.3 药效团建模与筛选
采用深度学习工具PharmacoNet基于MenT3-CTP共晶结构自动生成三维蛋白药效团模型,识别关键特征:
- • 氢键供体/受体位点
- • 疏水芳香环区域
- • 静电作用区域
药效团拟合评分(fit score)> 100为筛选阈值(文献通常以80为一般标准,本研究采用更严格的100分),最终保留1,724个高拟合度分子。
2.4 分子对接与验证
蛋白准备:
- • 晶体结构:PDB ID 8XHR(Mtb MenT3,2.10 Å)
- • 使用SilicoXplore的LigandLock模块处理
- • 去除水分子和非蛋白实体,保留CTP共晶配体
- • 生理pH下质子化,添加Gasteiger电荷
对接参数:
- • 活性位点坐标:x=7.936, y=-4.369, z=36.793
- • 格点维度:40×50×45 Å
- • 穷举度(exhaustiveness):8
- • 每个分子输出9个构象
- • 随机种子:42(保证可重复性)
自对接验证: CTP三次自对接的RMSD分别为1.670 Å、1.231 Å和1.457 Å,均低于2 Å的验证标准,CTP参考结合能均值为**-6.3 kcal/mol**。
以该均值为阈值,筛选结合能优于CTP的分子,获得1,481个候选化合物。
2.5 相似性搜索与结构过滤
使用SilicoXplore的SimSearch模块进行结构相似性分析:
- • 相似性度量:Tanimoto系数(范围0~1)
- • 阈值:≥ 0.5(中等相似性标准)
- • 共59个分子满足条件
进一步要求候选分子含有吡嗪环(pyrimidine ring)骨架(与CTP中胞嘧啶核心一致,有利于类似的氢键网络形成),最终确定14个候选分子进入动力学模拟。
2.6 分子动力学模拟
初步筛选阶段(20 ns): 对14个分子与MenT3形成的复合物各进行20 ns MD模拟,计算MM-GBSA结合自由能,以CTP复合物的**-38.32 kcal/mol**为筛选基准,选出Top 5分子。
扩展验证阶段(100 ns): 对5个候选分子延伸至100 ns模拟,同时对MenT3-CTP复合物进行等长对照模拟。
模拟参数:
参数 | 设置 |
|---|---|
软件 | GROMACS 2023.4 |
力场 | CHARMM36(蛋白) |
小分子拓扑 | SwissParam网络工具 |
水模型 | TIP3P |
周期性边界 | 立方盒 |
时间步长 | 2 fs |
压力 | 1 atm(恒压) |
温度 | 300 K(恒温) |
分析指标:
- • 蛋白骨架RMSD / 配体RMSD
- • 残基RMSF(逐残基柔韧性)
- • 回旋半径(RoG,系统紧实性)
- • 分子间氢键数量
- • 溶剂可及表面积(SASA)
- • 主成分分析(PCA)
- • 自由能景观(FEL,基于Gibbs自由能)
2.7 结合自由能计算(MM-GBSA)
采用gmx_MMPBSA包从MD轨迹计算结合自由能,每个轨迹含10,000帧,每隔5帧提取,共使用2,000帧计算。
计算公式体系:
其中极性溶剂化自由能(ΔG_pol)由广义Born(GB)模型计算,非极性项(ΔG_npol)由LCPO算法基于SASA估算,熵贡献(TΔS)通过**简正模式分析(NMA)结合相互作用熵(IE)**估算。
2.8 密度泛函理论(DFT)量子化学计算
采用PSI4量子化学软件包,在**B3LYP/6-31G(d)**理论水平下对Top 5分子及CTP进行DFT计算,获取:
- • HOMO/LUMO轨道能量及能隙:评估化学稳定性与反应活性
- • 分子静电势图(MEP):可视化电荷分布,预测亲电/亲核作用位点
- • Mulliken原子电荷:电子结构分析
- • 全局反应性描述符:
描述符 | 物理意义 |
|---|---|
电离势(IP) | 失去电子所需最低能量 |
电子亲和能(EA) | 得电子释放的能量 |
硬度(η) | 抗电荷转移/变形能力 |
软度(σ) | 易变形程度 |
电负性(χ) | 吸引电子对的趋势 |
化学势(μ) | 系统自由能随粒子数变化率 |
亲电指数(ω) | 亲电作用能力综合指标 |
三、主要结果与分析
3.1 分子对接结合相互作用分析
Top 5候选分子的对接结合能及关键相互作用汇总如下:
分子 | 结合能(kcal/mol) | 氢键残基 | 其他关键相互作用 |
|---|---|---|---|
MenT3_M1 | -8.6 | Lys61, Arg205 | Lys79/Ala80/Val119/Ala192/Ala195(疏水);Arg205(π-阳离子) |
MenT3_M2 | -8.0 | Lys61, Asp82, Lys189, Arg205 | Lys79/Ala80/Val119/Ala192(疏水);Lys79(π-阳离子) |
MenT3_M3 | -8.5 | Arg76, Lys79, Arg205 | Lys79(疏水);Asp82/Glu146(盐桥) |
MenT3_M4 | -8.5 | Lys189, Arg205 | Lys79/Val119/Ala192/Arg205(疏水);Asp82(盐桥) |
MenT3_M5 | -6.8 | Gly63, Lys189 | Lys79/Val119/Ala192(疏水);Lys79/His207(π-阳离子) |
CTP(参考) | -6.3 | Lys61, Gly63, Pro120, Lys189, Arg238 | Val119(疏水);Arg76/Lys79/Lys189/Arg205/His207(盐桥) |
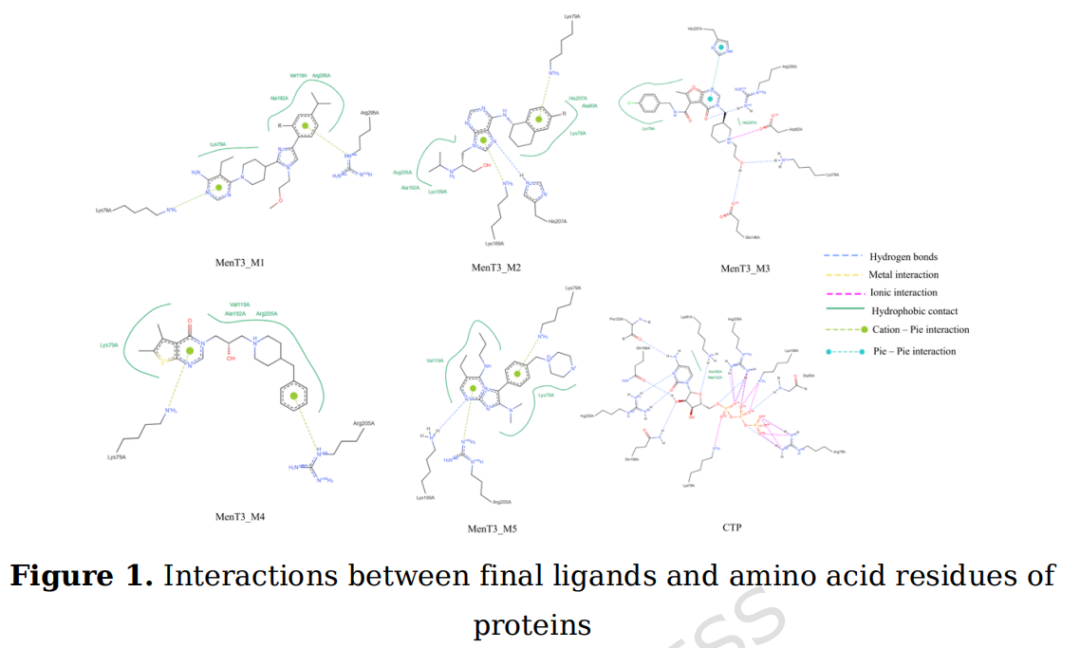
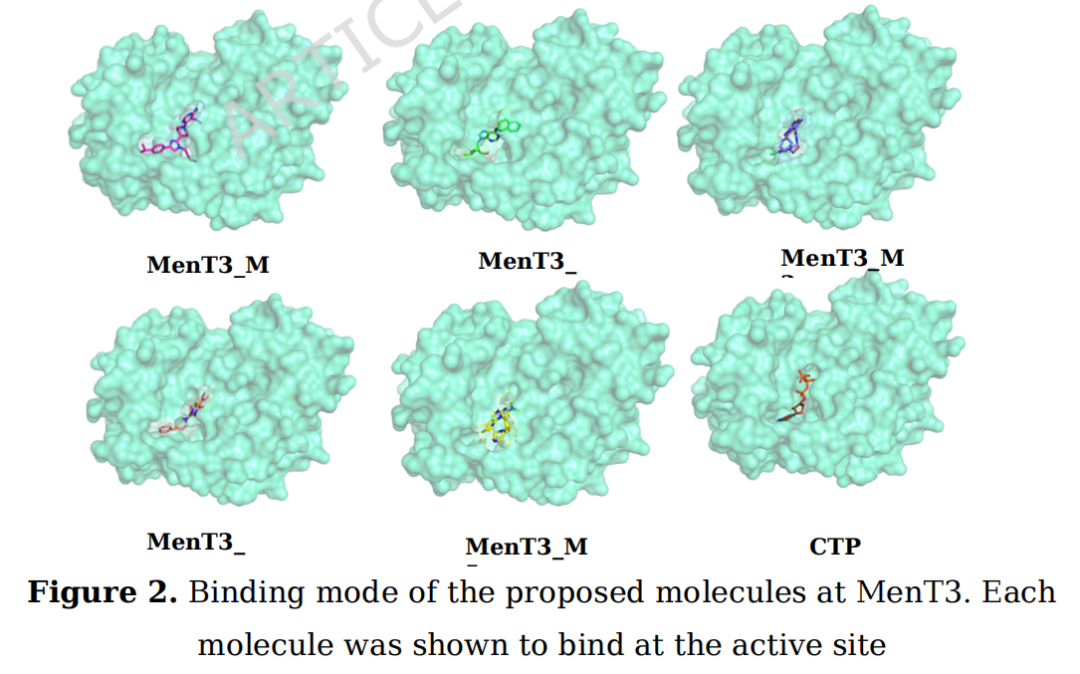
关键发现: 所有候选分子均与Val119形成疏水接触(与CTP一致),且与Lys61、Arg205的氢键相互作用高度保守,提示它们占据相同的活性位点。MenT3_M3额外形成Asp82-Glu146盐桥,可能赋予更强的静电稳定性。
3.2 100 ns 分子动力学模拟结果
3.2.1 骨架RMSD:蛋白结构稳定性
分子 | 平均RMSD(nm) | 最大RMSD(nm) |
|---|---|---|
MenT3_M1 | 0.16 | 0.26 |
MenT3_M2 | 0.16 | 0.22 |
MenT3_M3 | 0.13 | 0.24 |
MenT3_M4 | 0.19 | 0.26 |
MenT3_M5 | 0.15 | 0.29 |
CTP | 0.11 | 0.20 |
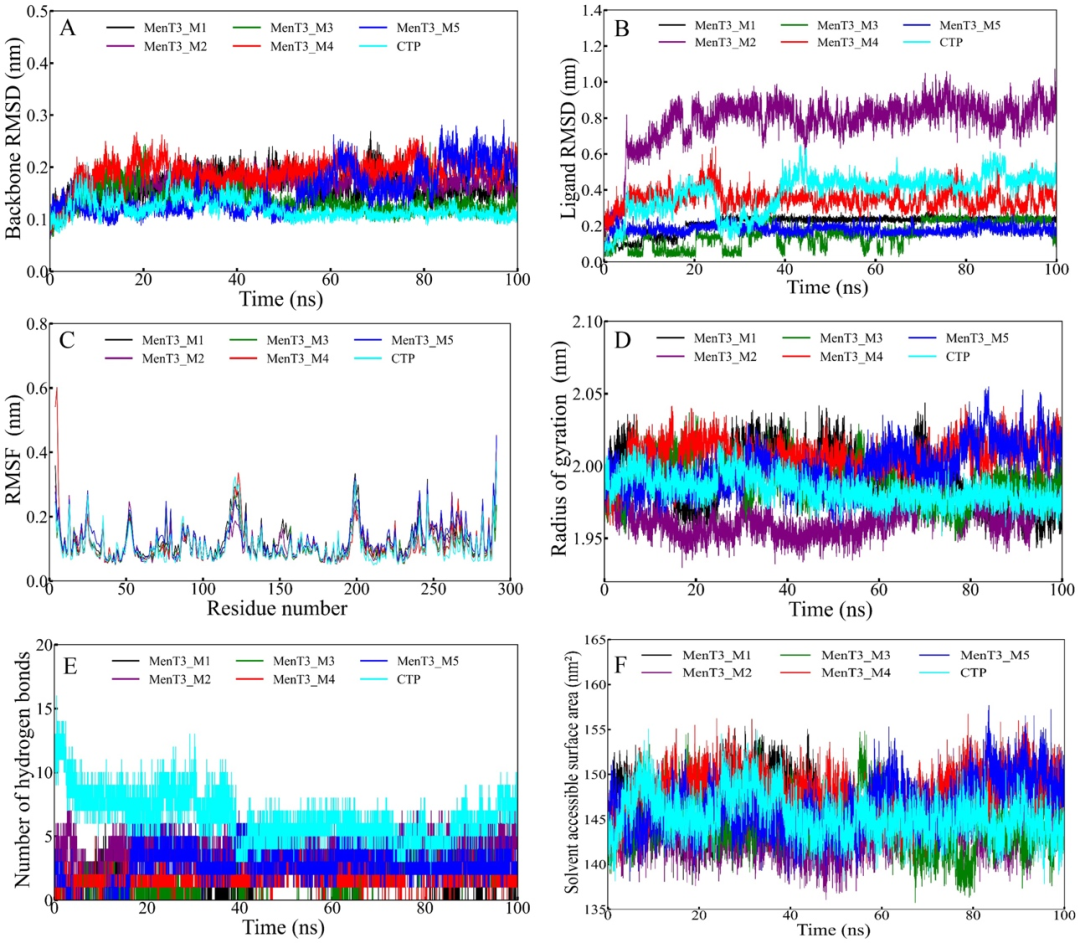

所有复合物蛋白骨架RMSD均维持在合理范围,表明候选分子未引起MenT3构象的显著扰动,与CTP行为高度相似。
3.2.2 配体RMSD:结合稳定性分析
MenT3_M2(紫色)和MenT3_M4(红色)的配体RMSD与CTP最为接近,始终维持在0~2 nm,结合最为稳定。MenT3_M3(绿色)配体RMSD高达8 nm,提示其在活性位点内发生了较大构象重排,结合稳定性相对较弱。
3.2.3 RMSF:残基柔韧性
所有复合物的残基RMSF最大波动在0.30~0.60 nm之间,整体模式与MenT3-CTP复合物高度一致,表明不同配体对MenT3氨基酸动态行为的影响极小。
3.2.4 回旋半径(RoG):系统紧实性
所有6个复合物的RoG全程维持在1.94~2.05 nm,最大偏差范围仅0.06~0.10 nm,明确证明各体系在整个模拟过程中保持了高度的结构紧实性和刚性。
3.2.5 氢键数量
CTP与MenT3形成的氢键数量最多(约8~12个),候选分子略少但均维持显著氢键数。无氢键帧通常由疏水接触和范德华力补偿,确保配体不会从活性位点解离。
3.2.6 SASA:溶剂可及表面积
各体系SASA均维持在140~155 nm²区间,平均值分别为147.09(M1)、143.55(M2)、144.61(M3)、147.93(M4)、146.46(M5)和145.41 nm²(CTP),无显著差异,提示蛋白折叠状态在结合配体后保持一致。
3.2.7 主成分分析(PCA)
- • MenT3_M1:点群密集,构象探索范围窄,结构柔韧性低
- • MenT3_M2:呈现两个明显簇,体系在两种构象态之间转换
- • MenT3_M3:分布均匀紧凑,动力学稳定
- • MenT3_M4:分布最宽,构象灵活性最高
- • MenT3_M5:点群较分散,提示多构象态探索
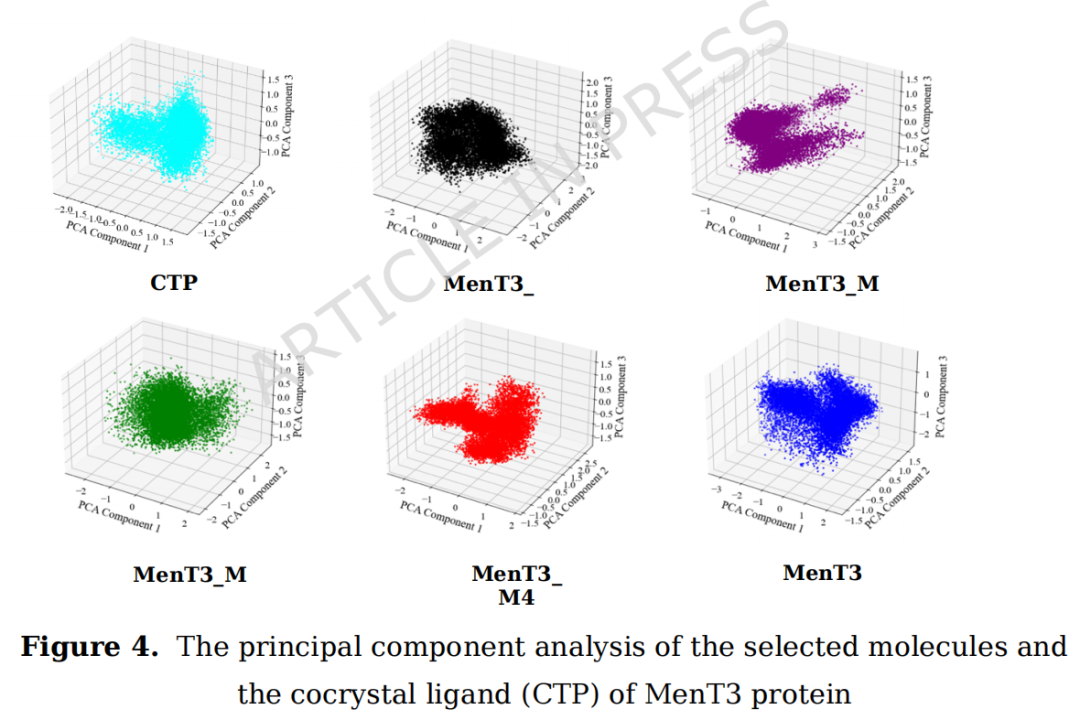
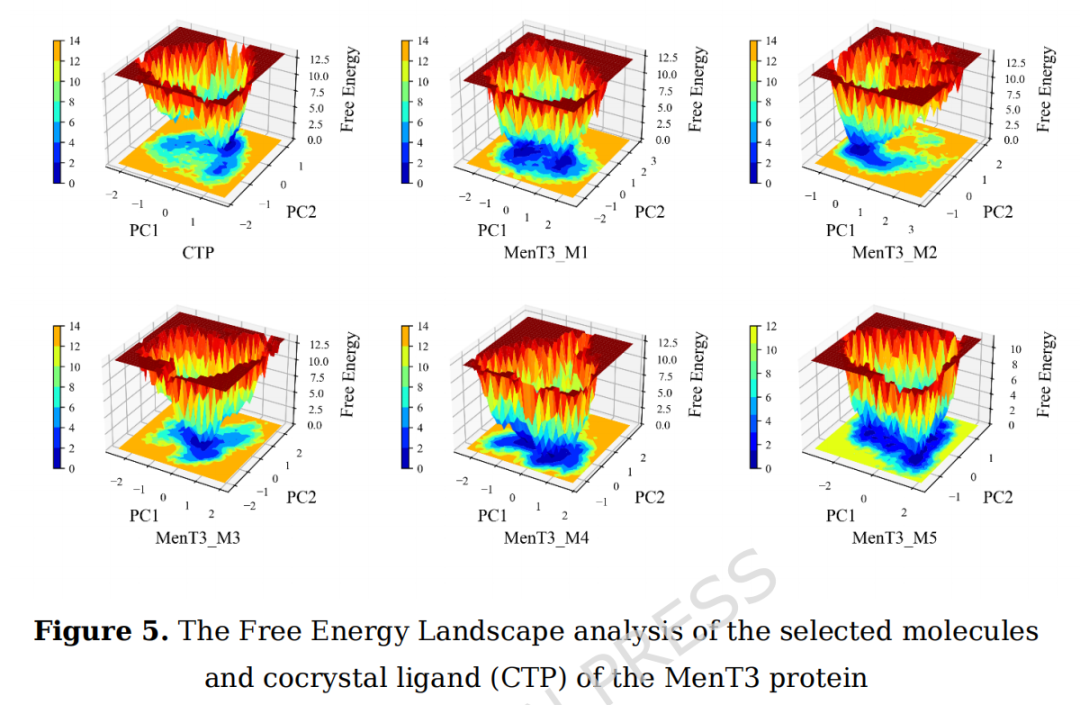
3.2.8 自由能景观(FEL)
基于PCA-Gibbs自由能分析:
- • MenT3_M1和MenT3_M3:能量盆地窄且深,稳定性最优
- • MenT3_M2:中心盆地略有偏移,构象探索较活跃
- • MenT3_M4:能量盆地最宽,峰值平坦,高度构象灵活
- • MenT3_M5:深浅盆地共存,稳定性与灵活性平衡
3.3 MM-GBSA结合自由能(100 ns轨迹)
化合物 | 平均ΔGbind(kcal/mol) | 标准差(±) | 与CTP比较 |
|---|---|---|---|
MenT3_M1 | -11.76 | 3.71 | 劣于CTP |
MenT3_M2 | -46.71 | 9.59 | 显著优于CTP |
MenT3_M3 | -11.13 | 19.72 | 劣于CTP(波动大) |
MenT3_M4 | -32.91 | 7.17 | 优于CTP |
MenT3_M5 | -36.43 | 2.34 | 优于CTP(最稳定) |
CTP(参考) | -29.81 | 24.40 | 基准 |
核心结论:MenT3_M2、MenT3_M4、MenT3_M5三个分子的结合自由能均优于天然底物CTP,尤其MenT3_M2以-46.71 kcal/mol展示出最强结合亲和力。值得注意的是CTP自身的标准差(24.40)较大,而MenT3_M5的标准差最小(2.34),表现出最高的结合一致性。
3.4 DFT量子化学计算结果
3.4.1 HOMO-LUMO能隙
化合物 | HOMO(Hartree) | LUMO(Hartree) | 能隙(eV) |
|---|---|---|---|
MenT3_M1 | -0.247 | 0.013 | 6.753 |
MenT3_M2 | -0.251 | 0.008 | 7.077 |
MenT3_M3 | -0.280 | -0.020 | 7.601 |
MenT3_M4 | -0.254 | -0.003 | 6.909 |
MenT3_M5 | -0.215 | 0.010 | 6.870 |
CTP | -0.285 | 0.003 | 7.875 |
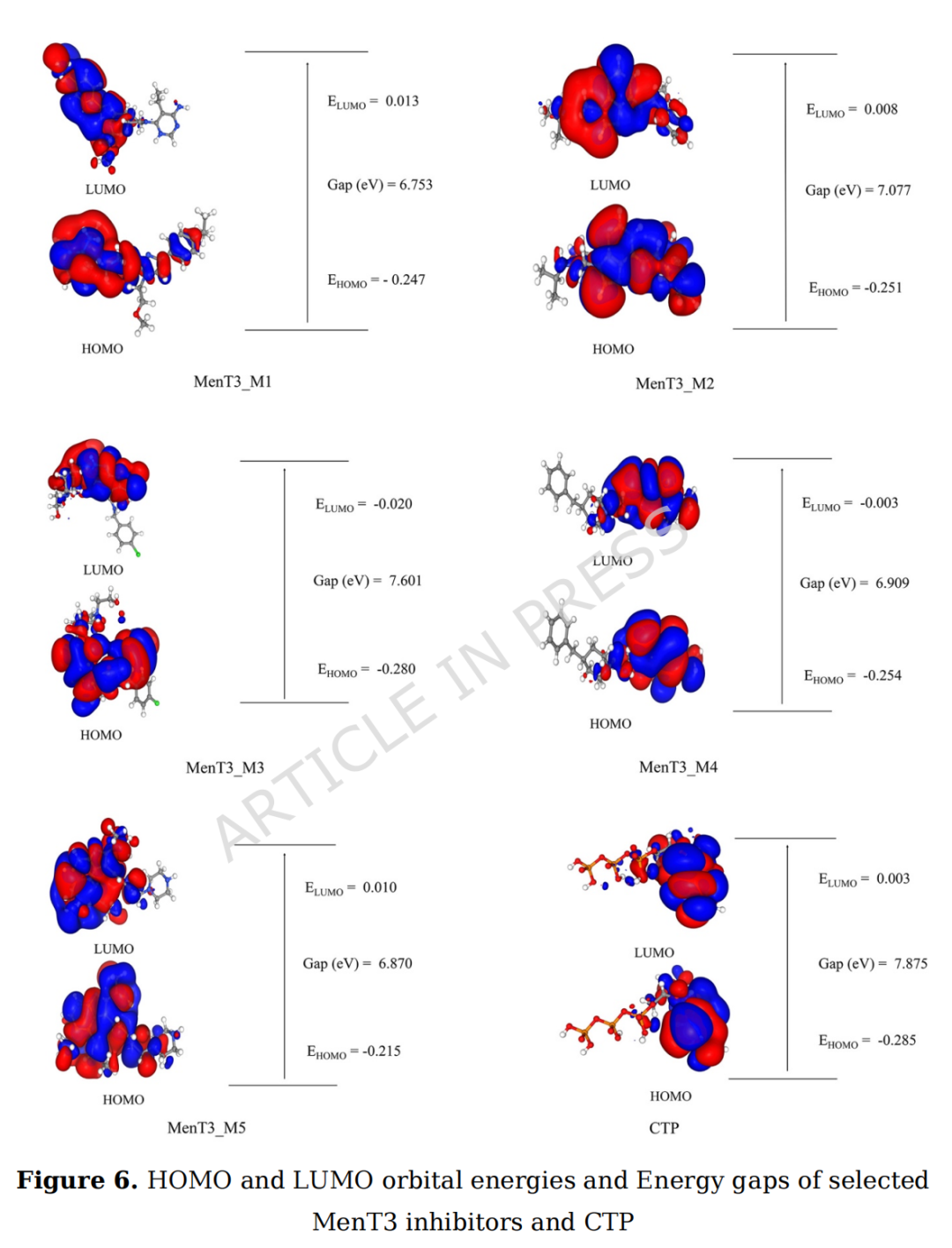
五个候选分子的HOMO-LUMO能隙均在6.75~7.60 eV之间,与CTP(7.875 eV)高度可比。大于6 eV的能隙表明这些分子具有足够的化学稳定性,同时保持适度的反应活性以与靶蛋白形成持续相互作用。
3.4.2 全局反应性描述符
描述符 | M1 | M2 | M3 | M4 | M5 | CTP |
|---|---|---|---|---|---|---|
IP(Hartree) | 0.247 | 0.251 | 0.280 | 0.254 | 0.215 | 0.285 |
EA(Hartree) | -0.013 | -0.008 | 0.020 | 0.003 | -0.010 | -0.004 |
η(硬度) | 0.130 | 0.130 | 0.129 | 0.125 | 0.112 | 0.144 |
σ(软度) | 7.660 | 7.689 | 7.705 | 7.977 | 8.868 | 6.910 |
χ(电负性) | 0.117 | 0.121 | 0.150 | 0.128 | 0.102 | 0.140 |
ω(亲电指数) | 0.052 | 0.057 | 0.087 | 0.066 | 0.046 | 0.068 |
MenT3_M3在电离势、正电子亲和能、电负性和亲电指数上均与CTP最为接近,展示出最强的电荷转移参与能力。MenT3_M5软度最高(8.868 Hartree⁻¹),化学反应性最强但稳定性相对较弱。
3.4.3 分子静电势(MEP)分析
MEP图揭示所有候选分子均存在明显的:
- • 电子富集区(红色):集中于羰基氧原子、氮杂原子等亲电活性位点,有利于与蛋白中电子供体残基(如Lys、Arg)形成氢键
- • 电子缺失区(蓝色):对应含氢氮原子及烷基氢,可与蛋白亲核位点形成互补接触
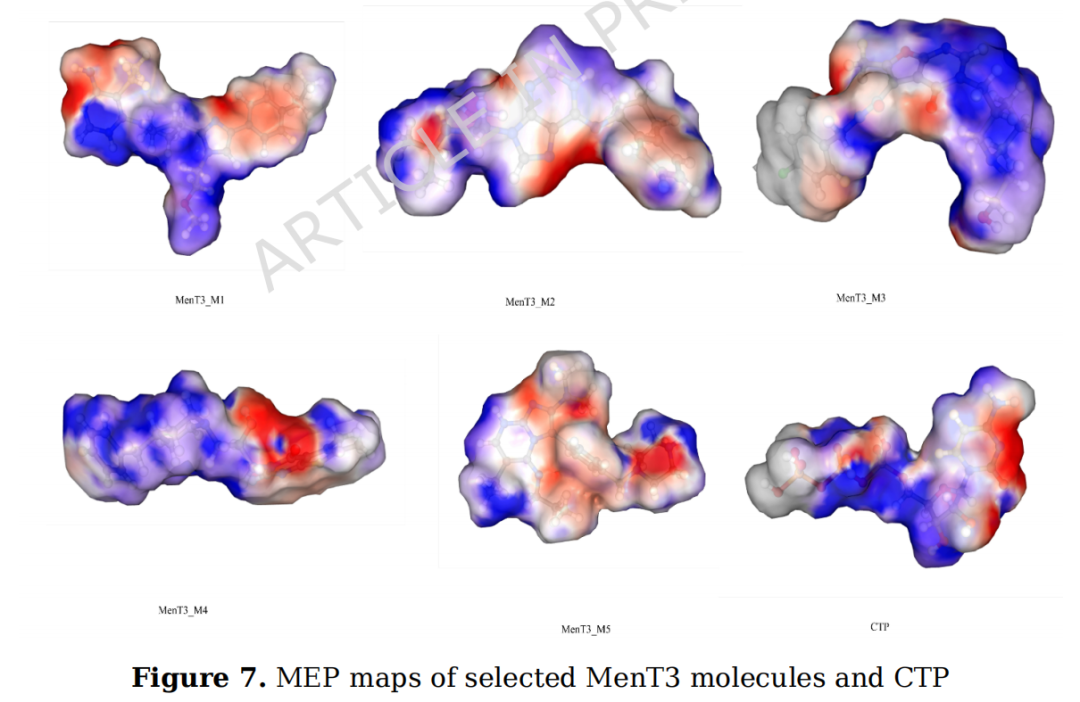
这种互补的电荷分布模式与CTP在MenT3活性位点中的作用方式高度一致,支持其作为有效竞争性抑制剂的合理性。
四、研究局限性
作者诚实且全面地讨论了以下局限:
局限类型 | 具体说明 |
|---|---|
方法论局限 | 分子对接假设蛋白半刚性,忽略完整构象熵贡献及溶剂动力学,可能导致假阳性或结合亲和力排序偏差 |
DFT局限 | 量子化学计算在孤立配体环境下进行,未考虑蛋白微环境效应,直接转化为结合背景参数时存在偏差 |
实验缺失 | 无体外(in vitro)酶活抑制、全细胞抗Mtb活性、细胞毒性测试或靶点接合验证数据,候选分子的实际效力、选择性和细胞渗透性均未经验证 |
靶点单一性 | 未考虑脱靶效应、多药理学特征或Mtb复杂系统中的耐药发展问题 |
模拟时间尺度 | 100 ns模拟对于某些慢动力学过程(如构象选择、结合/解离事件)可能仍不足够 |
小结
研究亮点
- • 完整管线示范:从百万级化学空间生成到5个候选分子的全流程可重复管线
- • 多维度交叉验证:结合能计算、动力学稳定性分析和量子化学描述符形成互补的证据体系
- • 新颖靶点:MenT3作为TA系统毒素代表了与现有抗结核药物完全不同的作用机制,有望克服耐药性问题
- • 平台整合:SilicoXplore云平台的使用降低了计算门槛,具有推广价值
需关注的问题
- • MenT3_M3在100 ns模拟中配体RMSD高达8 nm,结合稳定性存疑,但其DFT性质与CTP最为接近,两种评估结果之间的矛盾值得深入探讨
- • MenT3_M1和MenT3_M3的100 ns MM-GBSA结合自由能(约-11 kcal/mol)显著低于20 ns初筛结果(-46.86和-48.92 kcal/mol),提示短时模拟结果存在过估计风险,更长时间尺度的模拟对于准确评估结合自由能重要
- • CTP作为参考分子的MM-GBSA标准差高达24.40 kcal/mol,提示其自身在动力学轨迹中结合模式存在波动,参考价值需审慎解读
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-04-22,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读
目录

