Nat. Commun. | 利用脑类器官与深度学习筛选加速Leigh综合征药物发现
Nat. Commun. | 利用脑类器官与深度学习筛选加速Leigh综合征药物发现

DrugAI
发布于 2026-04-28 10:19:00
发布于 2026-04-28 10:19:00
DRUGONE
Leigh综合征是一种严重的线粒体疾病,目前尚无有效治疗方法,其特征包括乳酸酸中毒以及基底节和中脑区域的病变,最终导致神经功能退化和早逝。研究人员此前发现,在携带SURF1突变的脑类器官中,神经元形态发生受到显著损害。
基于这一疾病表型,研究人员开发了一种针对特定细胞类型的深度学习药物重定位筛选方法,并结合酵母模型开展生存筛选实验。两种独立策略最终均指向唑类化合物,其中他拉罗唑(talarozole)和舍他康唑(sertaconazole)能够恢复Leigh神经元的形态发生,同时降低乳酸释放并改善中脑类器官的生长状态。机制研究表明,这些化合物通过调控维甲酸信号通路以及膜相关脂质代谢发挥作用。整体来看,该研究展示了将计算筛选与人源脑类器官结合的潜力,为罕见神经发育疾病的药物发现提供了一种新方法。
Leigh综合征是一种由线粒体功能缺陷引起的神经代谢疾病,通常由核基因或线粒体DNA突变导致氧化磷酸化系统失效。由于神经系统对能量需求极高,该疾病主要影响基底节和中脑区域,进而导致运动障碍、认知受损以及乳酸积累等典型症状。
其中,SURF1基因突变是最常见的致病因素之一,其编码的蛋白参与线粒体呼吸链复合物IV的组装。尽管在酵母和大型动物模型中能够观察到明显表型,但在小鼠模型中却缺乏典型病理特征,这提示不同物种在能量代谢补偿机制上的差异,也使得疾病机制研究与药物开发面临困难。
近年来,研究人员利用患者来源的诱导多能干细胞结合基因编辑技术,构建了脑类器官模型。这些模型显示出神经祖细胞分化受阻、神经元连接能力下降等关键缺陷,提示Leigh综合征可能本质上是一种神经发育障碍。
然而,目前仍缺乏高效的药物筛选策略。传统筛选方法依赖体外实验,耗时且成本高昂。因此,研究人员尝试引入深度学习与多模型联合策略,以加速候选药物的发现过程。
方法
研究人员构建了一个多层级筛选框架,将深度学习预测与实验筛选相结合。
首先,基于脑类器官的单细胞转录组数据,构建了一个细胞类型特异的深度学习模型。该模型通过分析不同细胞状态之间的转录变化,预测能够促进细胞从未分化状态向神经元状态转变的药物。模型核心在于从蛋白扰动层面推断药物作用机制,并结合分子相互作用网络进行传播与整合,从而筛选候选药物。
与此同时,研究人员在SURF1同源基因缺失的酵母模型中,对2250种已获批药物进行生存筛选,以寻找能够恢复细胞活性的候选分子。
最终,通过整合两种策略的结果,并结合药物安全性和代谢相关特征,筛选出一组候选药物用于后续验证。
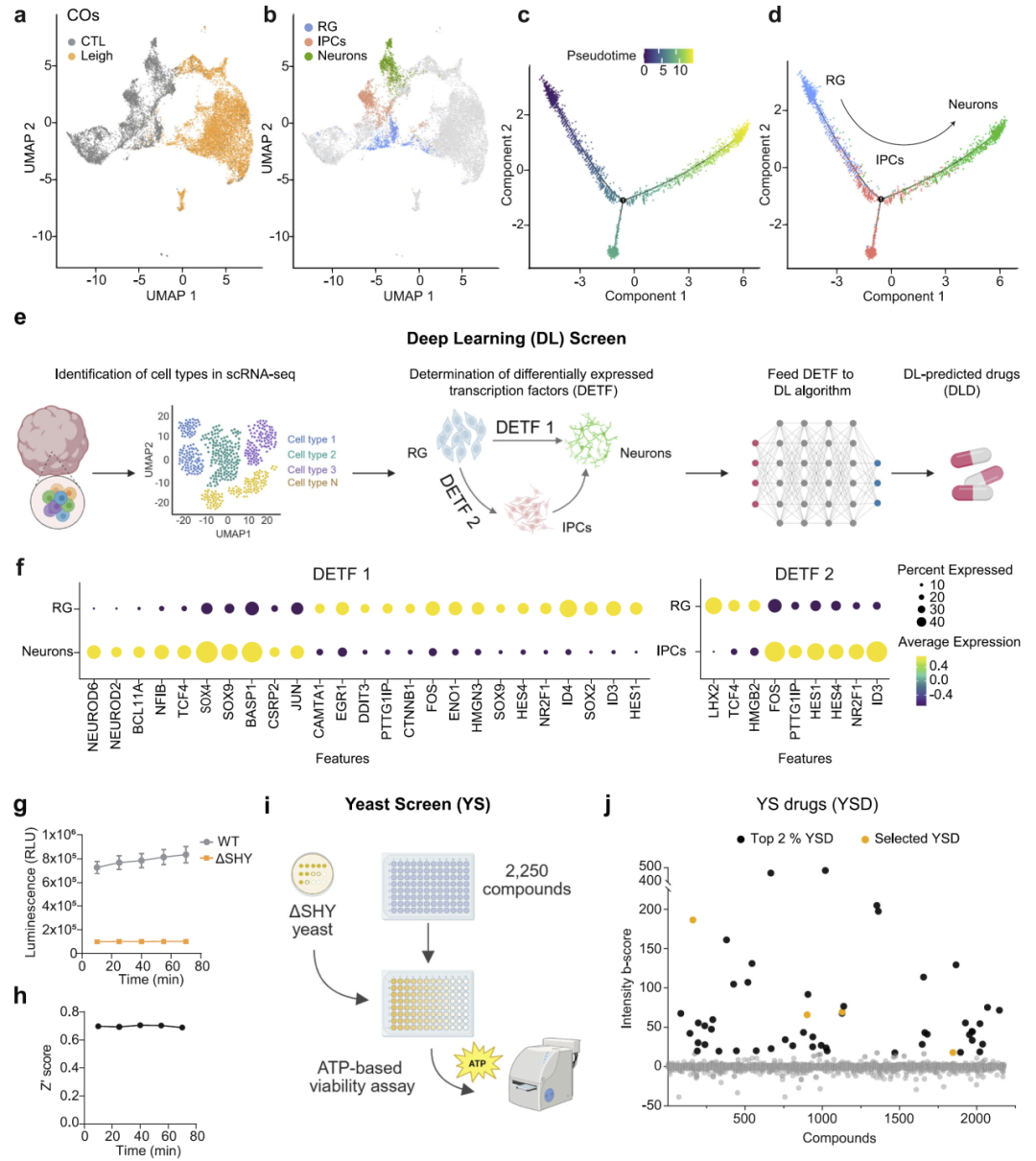
图1:深度学习与酵母筛选整体框架。
结果
深度学习与酵母筛选共同发现候选药物
单细胞分析表明,Leigh脑类器官中主要缺乏中间祖细胞和成熟神经元,而径向胶质细胞仍然存在,这提示神经分化过程受阻。伪时间分析进一步验证了神经发育路径从祖细胞向神经元的演化方向。
基于这一特征,深度学习模型成功预测了一批能够促进细胞命运转换的候选药物。同时,酵母筛选实验独立发现了一类能够提高细胞存活率的化合物。
值得注意的是,两种完全不同的筛选策略最终在唑类化合物上实现收敛,这一结果显著增强了候选药物的可信度。
唑类化合物恢复神经形态发生
在体外神经分化实验中,Leigh来源细胞生成神经元的能力显著降低。经过药物处理后,他拉罗唑和舍他康唑均能显著提高神经元数量,并改善神经突起结构。
其中,他拉罗唑表现出更强的剂量依赖效应,在适当浓度下能够显著提升神经元生成,而高浓度则表现出毒性。这一结果表明药物作用具有明确的剂量窗口。
酵母实验同样显示,这两种化合物能够显著提高突变株的存活率,进一步验证了其功能。
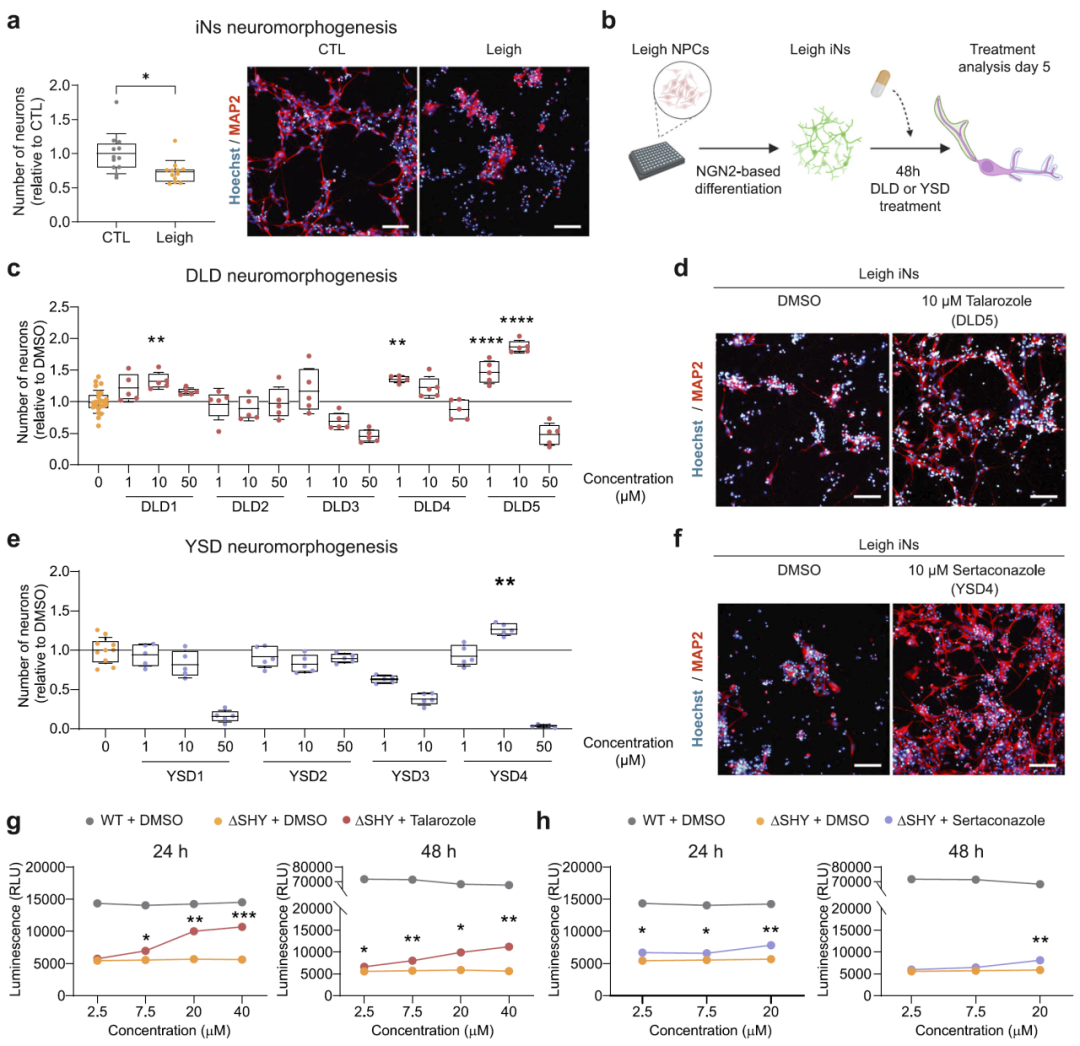
图2 :神经形态恢复实验。
中脑类器官重现疾病表型
研究人员进一步构建了中脑类器官模型,以更准确模拟疾病发生部位。该模型成功再现了Leigh综合征的多个关键特征,包括神经元生成减少、结构标志物表达降低以及乳酸水平升高。
转录组分析显示,与神经发育相关的基因显著下调,而与细胞增殖和代谢相关的基因上调。此外,类器官在代谢应激条件下表现出异常的钙信号响应,提示其能量代谢调控能力受损。
这些结果表明,中脑类器官能够有效模拟Leigh综合征的关键病理特征,是评估药物效果的重要模型。
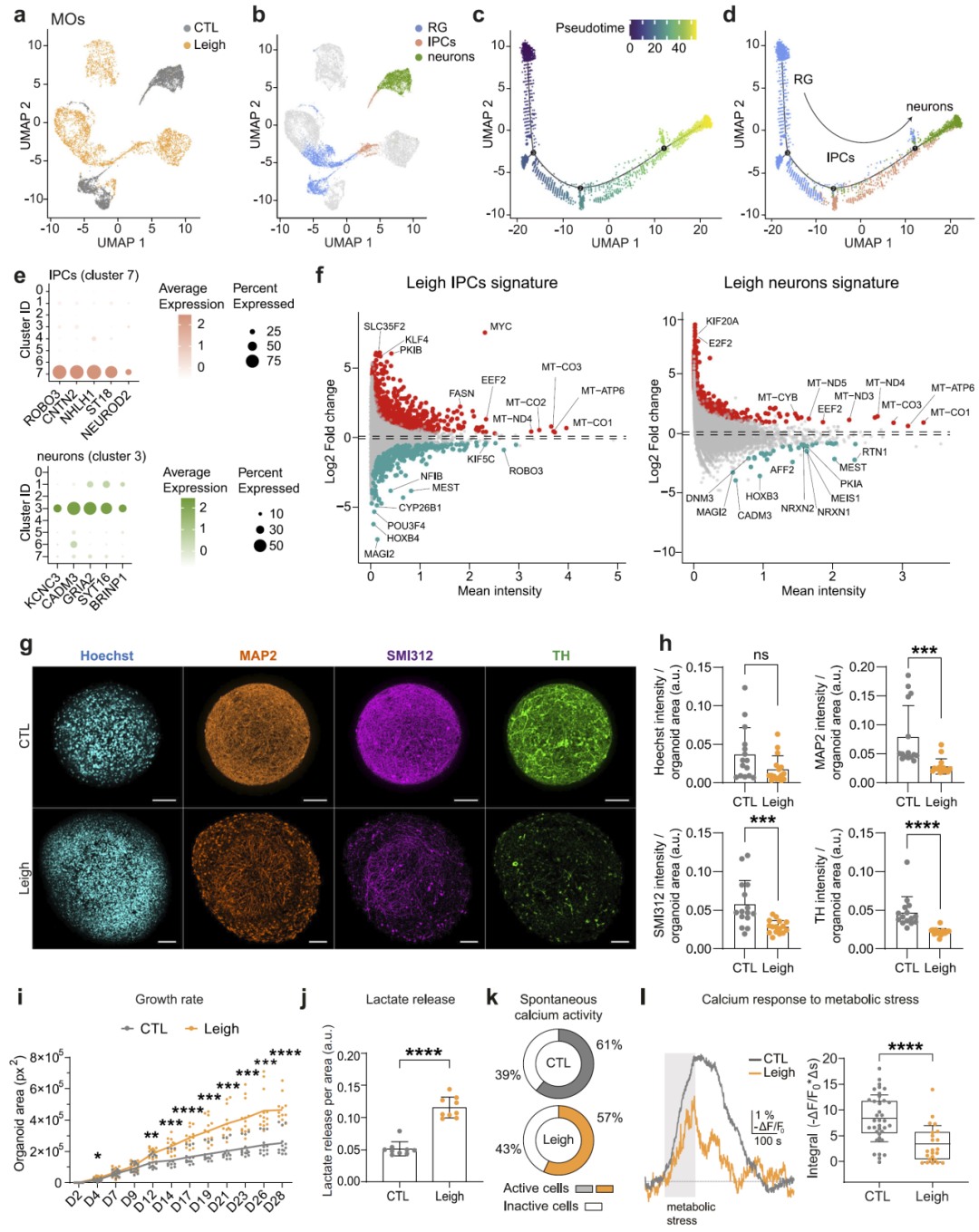
图3:中脑类器官疾病表型。
候选药物在类器官中的治疗效果
在类器官模型中,唑类化合物能够显著降低异常的生长速率,并减少乳酸释放水平。他拉罗唑还能够增加多巴胺能神经元的数量,并改善细胞功能表现。
在功能层面,药物处理后类器官对代谢压力的响应能力显著增强,表明其能量调控能力得到恢复。
尽管药物未能完全逆转所有表型,但其对多个关键病理特征的改善表明其具有潜在治疗价值。
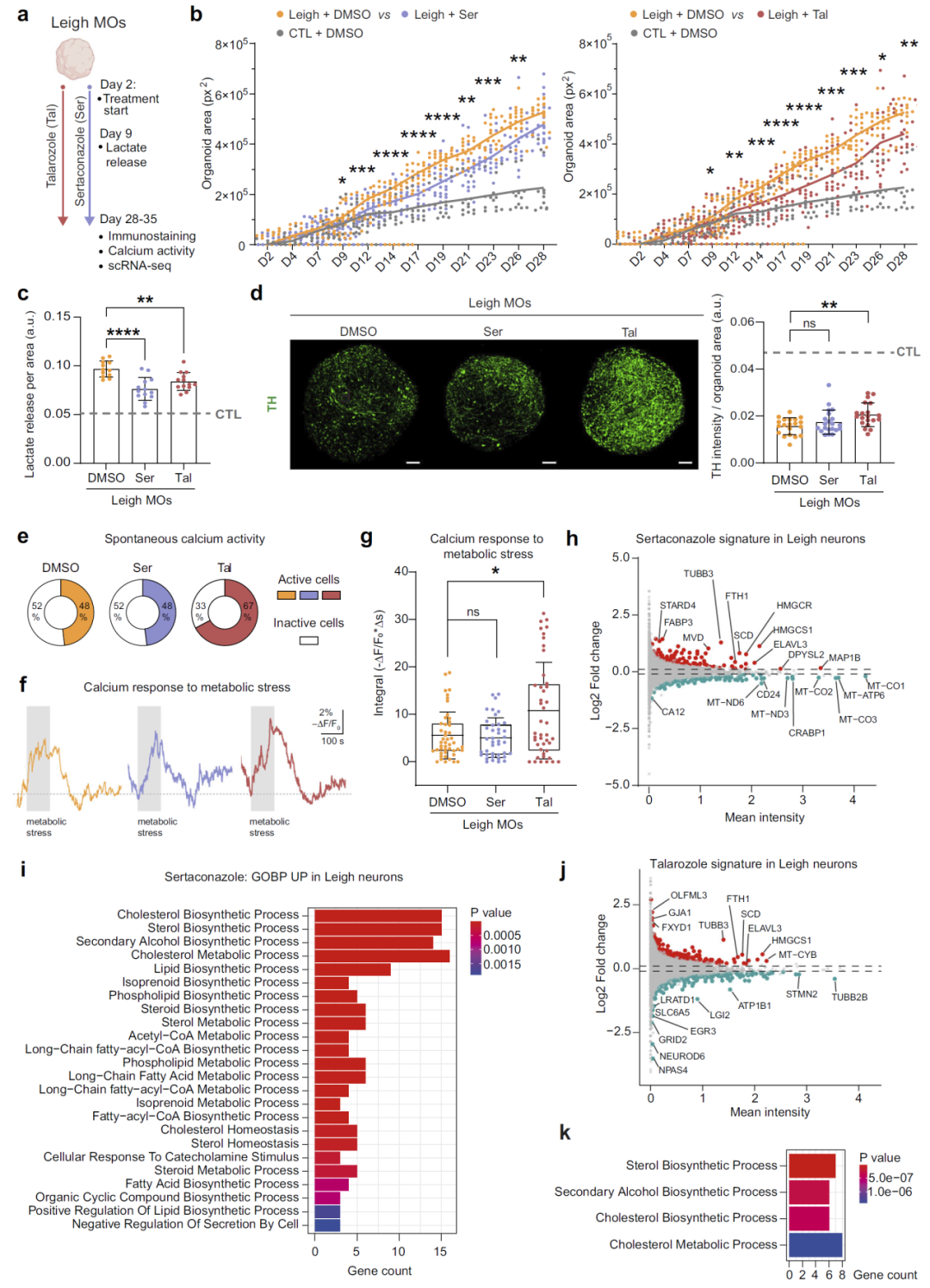
图4:药物在类器官中的作用。
作用机制:能量代谢与脂质调控
代谢组学分析显示,Leigh细胞中能量代谢严重受损,而他拉罗唑能够恢复AMP/ATP比值并改善三羧酸循环代谢。
脂质组学分析进一步表明,舍他康唑主要通过调节膜脂和胆固醇水平发挥作用,而他拉罗唑则在能量代谢恢复方面表现更为显著。
这些结果表明,两种药物在机制上具有互补性,共同调节细胞代谢状态。
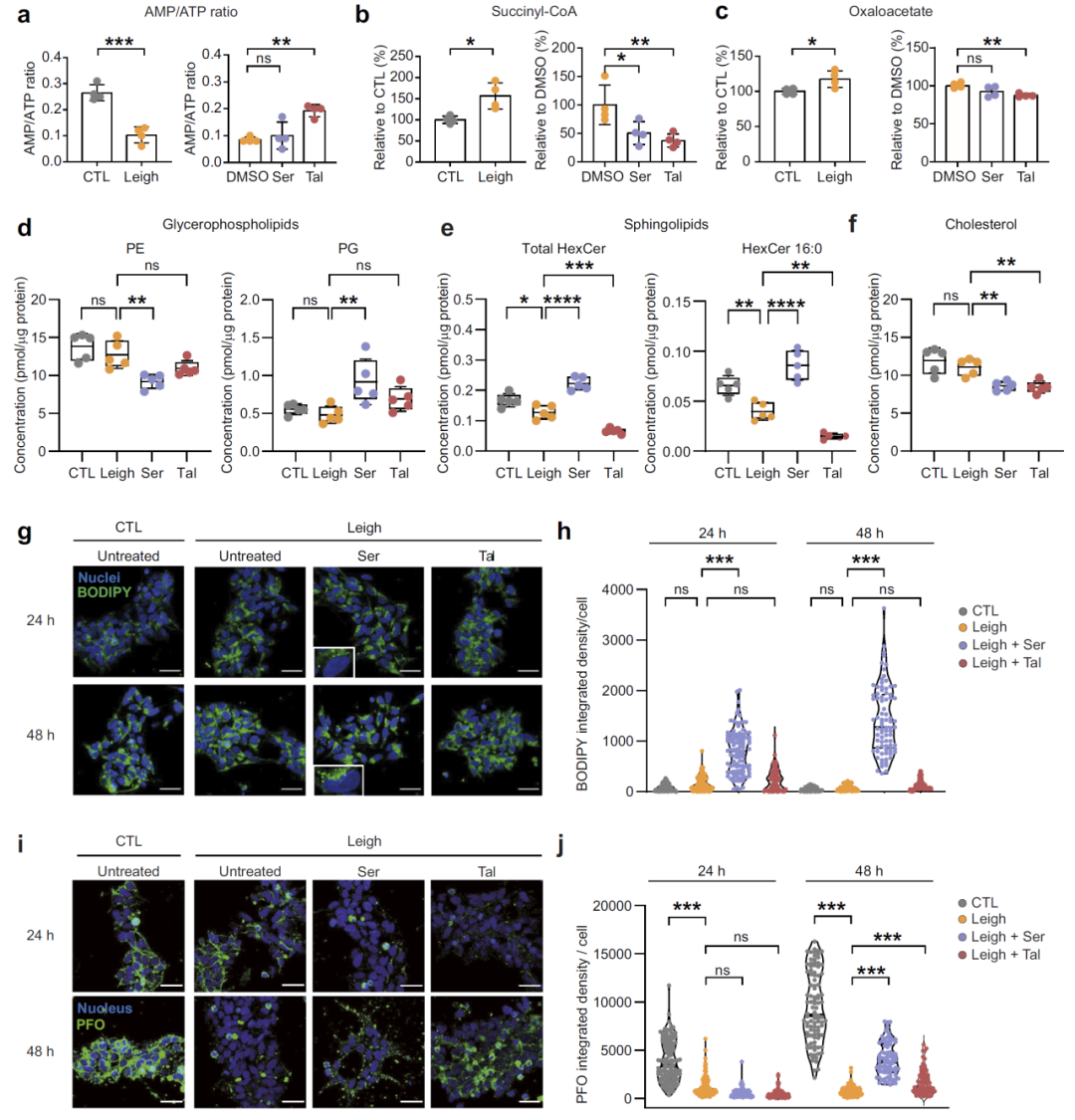
图5:代谢与脂质机制。
分子机制:维甲酸与PPARγ通路
分子对接分析表明,两种唑类化合物能够与维甲酸代谢相关酶CYP26结合,其中他拉罗唑表现出更强的结合能力。
进一步实验表明,他拉罗唑能够恢复维甲酸通路活性,并增强PPARγ信号,而舍他康唑主要影响脂质代谢通路。
这些结果揭示了药物通过调控发育信号与代谢网络共同作用,从而改善神经发育缺陷。
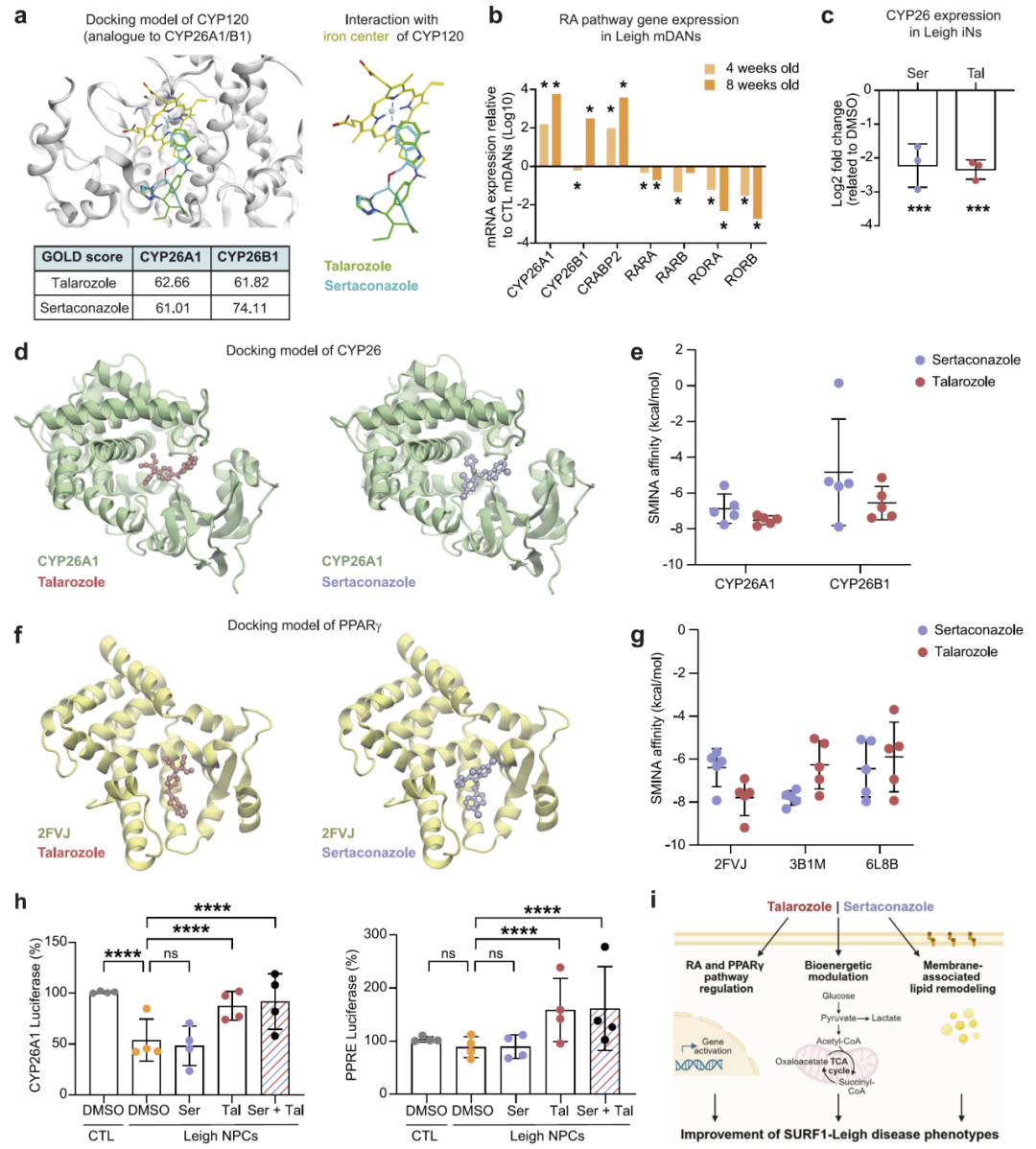
图6:分子作用机制。
讨论
本研究提出了一种结合深度学习与脑类器官的新型药物发现策略,在Leigh综合征这一复杂疾病中取得了重要突破。通过整合计算预测与多模型实验验证,研究人员成功筛选并验证了具有潜力的候选药物。
该方法的核心优势在于能够在早期阶段快速缩小候选范围,从而显著降低实验筛选成本。同时,人源类器官模型的引入,使得筛选结果更具临床相关性。
此外,研究结果强调了神经发育过程在Leigh综合征中的关键作用,并提出通过调控代谢与信号通路促进神经形态发生可能是一种有效治疗策略。
未来,随着更多多模态数据的整合以及类器官模型的进一步优化,这种“AI+类器官”的方法有望成为罕见疾病药物开发的重要范式。
整理 | DrugOne团队
参考资料
Menacho, C., Okawa, S., Álvarez-Merz, I. et al. Accelerating Leigh syndrome drug discovery through deep learning screening in brain organoids. Nat Commun 17, 3570 (2026).
https://doi.org/10.1038/s41467-026-71391-2
内容为【DrugOne】公众号原创|转载请注明来源
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-04-22,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

