Nat. Microbiol. | 解读人类微生物组研究中的多组学整合策略
Nat. Microbiol. | 解读人类微生物组研究中的多组学整合策略

DrugAI
发布于 2026-04-28 10:18:27
发布于 2026-04-28 10:18:27
DRUGONE
多组学研究正在推动人类微生物组研究迈向系统层面,使研究人员能够从多个分子层级同时解析宿主–微生物互作。然而,尽管相关数据迅速增长,其分析仍面临概念、方法和计算层面的多重挑战。与此同时,各类整合方法不断涌现,使研究人员在方法选择上面临更高复杂度。
本综述系统梳理了人类微生物组研究中的多组学整合方法,并以“研究问题”为核心组织框架,强调不同方法所回答的生物学问题差异,包括分子层之间的相互作用、疾病相关变化、患者分层以及潜在机制解析。研究人员旨在提供一个清晰、系统的指南,帮助研究者根据具体问题选择最合适的方法。

多组学驱动的微生物组研究新范式
人类微生物组已成为生物医学研究的重要前沿。大量研究表明,微生物组与多种疾病密切相关,但其背后的分子机制仍未完全阐明。这一瓶颈限制了研究成果向临床应用的转化。
多组学研究试图通过整合宏基因组、转录组、代谢组、蛋白组以及宿主基因组等多层信息,从系统层面解析复杂的宿主–微生物互作。随着技术进步和成本下降,大规模多组学数据迅速积累,例如iHMP等项目提供了前所未有的数据资源。
然而,这些数据具有高度异质性,包括维度差异、稀疏性、分布差异以及技术偏差,使得整合分析极具挑战。同时,方法种类繁多,也增加了研究人员的选择难度。
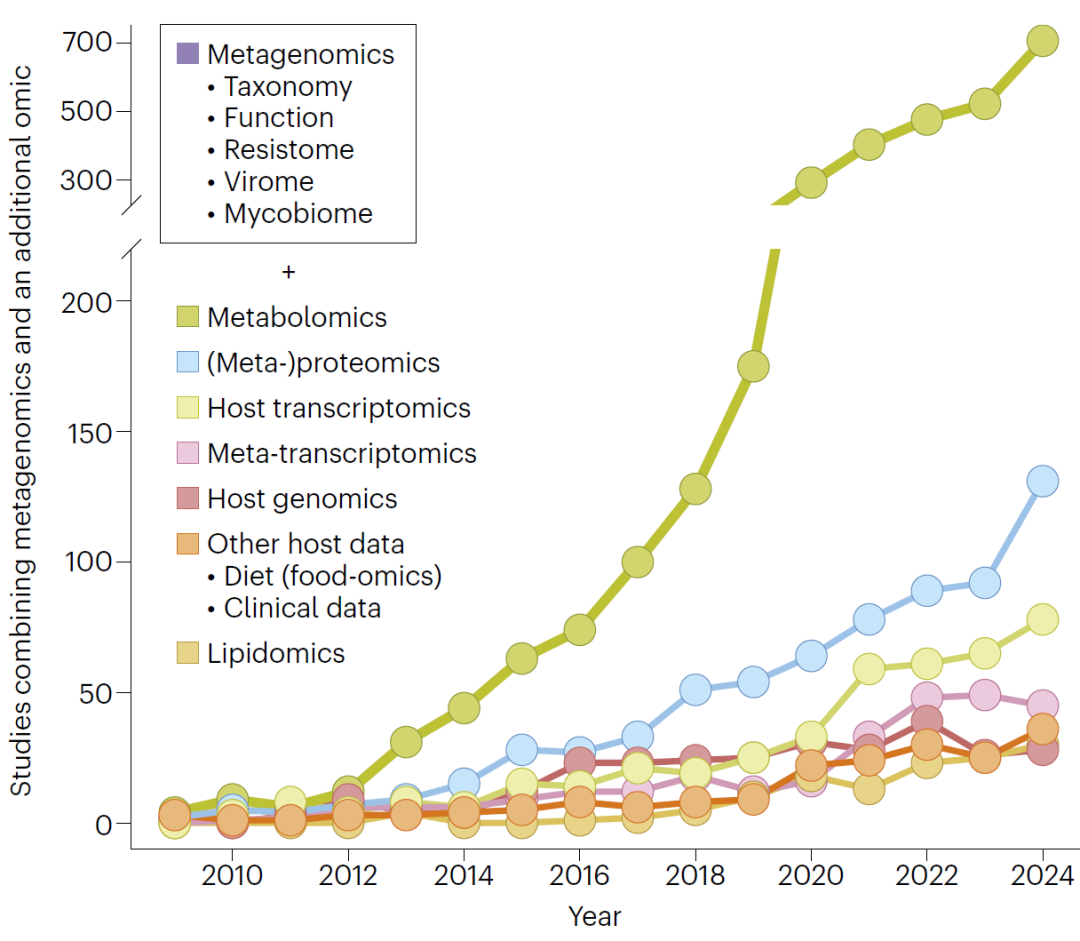
图1:多组学微生物组研究发展趋势(不同组学组合随时间增长)。
多组学整合方法的分类框架
研究人员指出,多组学整合方法可以从多个维度进行分类,包括整合阶段(早期/中期/后期)、算法类型(统计、网络、机器学习等)、整合分辨率以及数据特性。
但最关键的分类维度是研究问题本身。围绕这一维度,多组学研究主要聚焦四类核心问题:
1)不同分子层如何相互作用
2)疾病中分子层如何发生变化
3)如何基于多组学对患者进行分层
4)这些关联背后的机制是什么
这一问题驱动框架成为整个综述的核心组织逻辑。
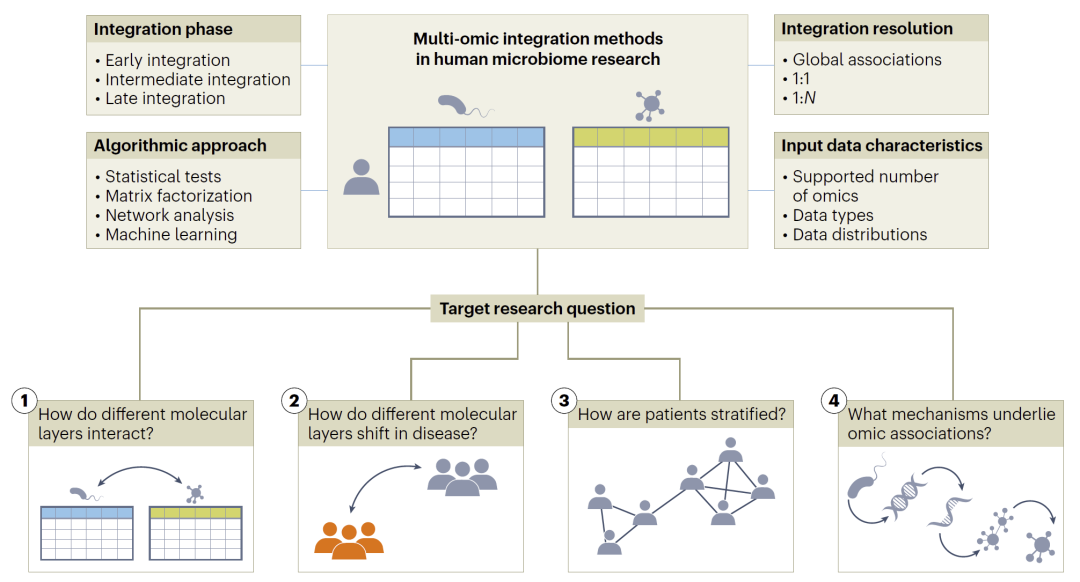
图2:多组学整合方法的分类体系与四大研究问题框架。
分子层之间如何相互作用
理解不同组学层之间的关系,是多组学研究的基础。例如,微生物组成如何影响代谢物水平,或基因表达如何反映功能活动。
研究人员首先从全局关联角度出发,通过样本间距离矩阵比较不同组学之间的一致性。例如Mantel检验、Procrustes分析等方法,可用于评估不同组学在整体层面的相关性。这类方法的优势在于避免特征维度差异带来的偏差,但其缺点是难以解释具体机制。
进一步的方法基于潜在变量建模,将高维数据映射到低维空间,以捕捉跨组学的共同变化。例如PLS、CCA以及MOFA等方法,可以揭示潜在的生物过程。
然而,仅有全局关联不足以解释机制。因此,研究人员进一步关注特征级关联。通过相关性分析和网络构建,可以识别具体分子之间的关联,例如某些菌群与代谢物之间的关系。加权网络方法(如WGCNA)进一步揭示模块结构。
另一类方法关注跨组学预测,即利用一个组学预测另一个组学。例如通过微生物组预测代谢组,从而推断功能关系。这类方法通常依赖机器学习模型。
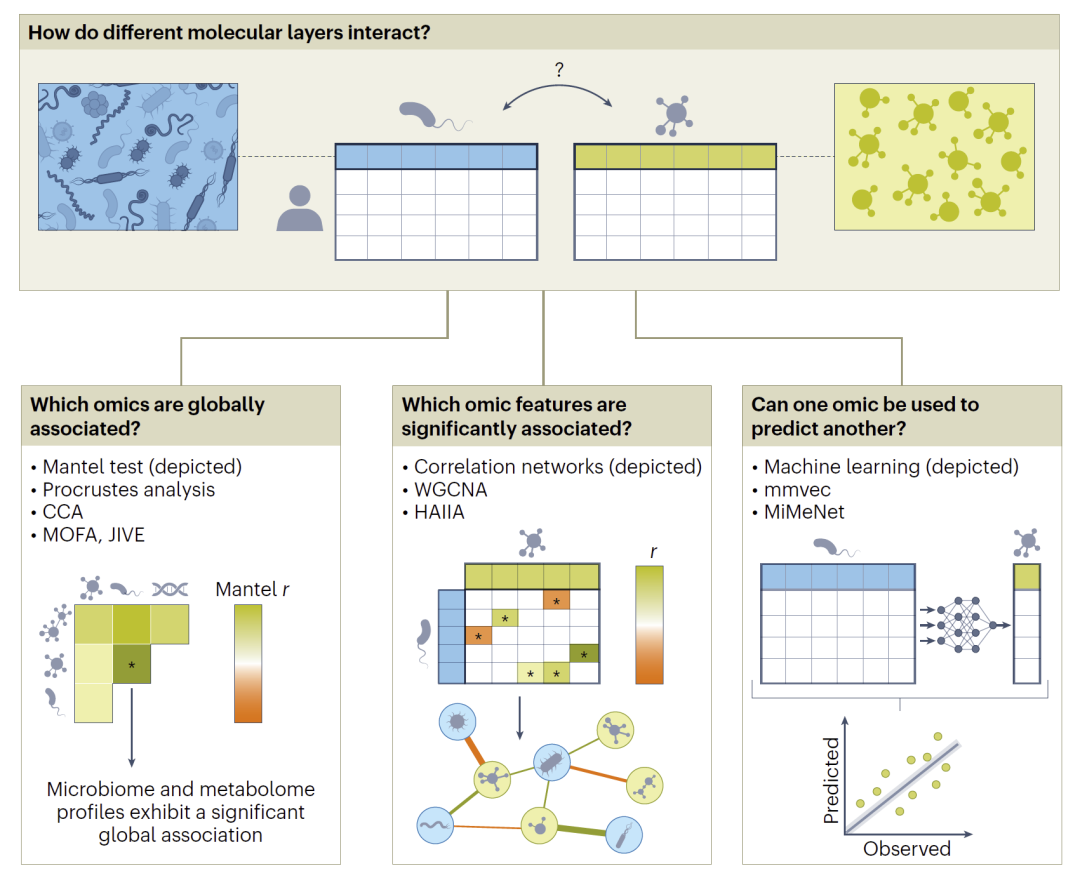
图3:多组学关联分析框架(全局关联、特征关联与跨组学预测)。
分子层在疾病中如何变化
多组学研究的重要目标之一是揭示疾病相关变化。首先可以比较不同组学与疾病表型的整体关联程度。例如使用PERMANOVA或机器学习模型评估各组学的预测能力。
进一步,研究人员关注多组学整合是否能够提升疾病预测能力。早期整合方法将所有特征拼接后建模,而后期整合方法则结合多个模型结果。研究表明,在某些疾病中,多组学整合确实优于单组学,但在另一些情况下优势有限。
在更精细层面,研究人员致力于识别多组学疾病标志物。这可以通过统计检验、网络分析或潜变量方法实现。例如MOFA和DIABLO可以识别与疾病相关的潜在分子模式。
此外,因果分析方法(如中介分析)可用于解析不同组学之间的因果关系,例如微生物是否通过代谢物影响宿主健康。
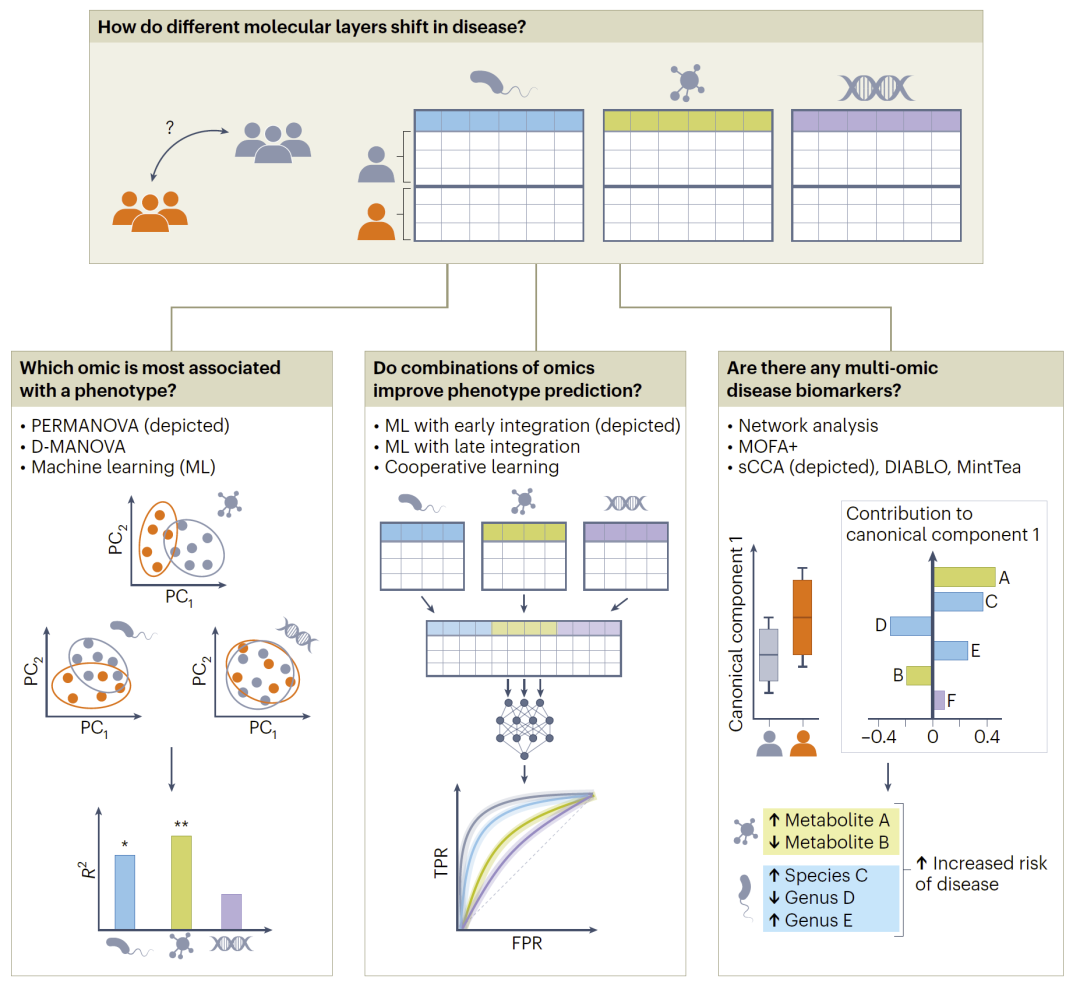
图4:疾病相关多组学分析框架(关联评估、预测建模与标志物识别)。
如何基于多组学对患者进行分层
多组学数据为患者分型提供了新的维度。通过整合不同组学信息,研究人员可以识别具有不同分子特征的亚群,从而揭示疾病异质性。
传统聚类方法可以应用于单组学数据,但多组学聚类更为复杂。方法如相似性网络融合(SNF)通过构建并融合不同组学的样本网络,实现综合分群。
此外,潜变量模型(如iCluster)和图神经网络方法(如MOGONET)也被用于多组学聚类。这些方法能够在共享空间中整合不同组学信息,从而提高分群的生物学意义。
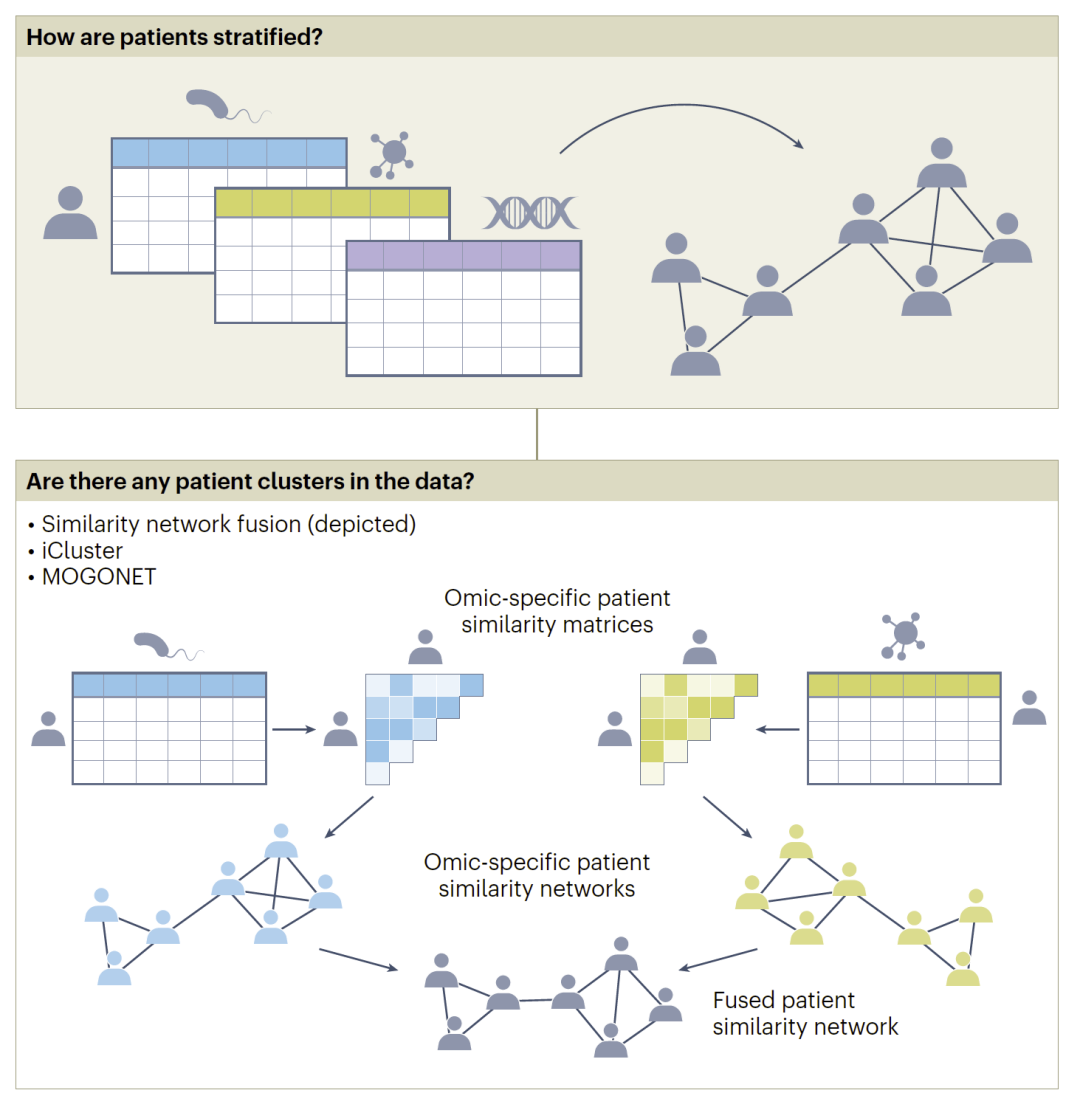
图5:多组学患者分层方法(网络融合与潜变量模型)。
如何解析多组学关联背后的机制
仅仅发现关联并不足够,理解其生物学机制才是关键。为此,研究人员提出引入已有生物学知识进行整合分析。
一种方法基于代谢网络,通过已知的酶反应关系连接基因、代谢物和微生物,从而推断代谢来源。例如MIMOSA等方法可预测某些代谢物是否由微生物产生。
另一种方法基于生物通路,将分子映射到功能通路,从而识别疾病相关路径。这种方法提高了结果的可解释性。
此外,序列驱动方法通过将基因、转录本和蛋白质映射到统一参考框架,实现跨组学整合。例如通过联合分析宏基因组和转录组,可以区分基因丰度变化与表达变化。
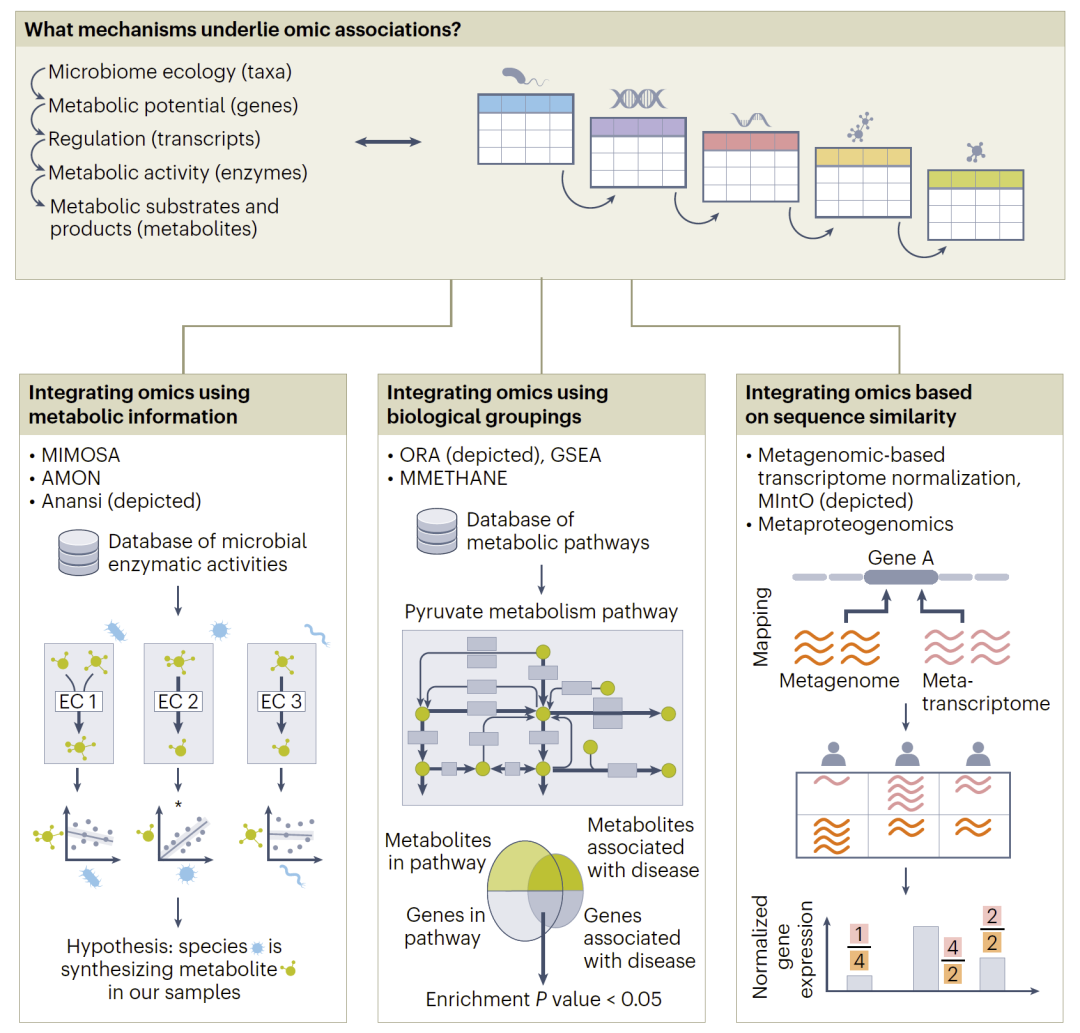
图6:基于先验知识的多组学机制解析(代谢网络、通路与序列整合)。
结论与展望
多组学整合正在推动微生物组研究从相关性分析迈向机制解析。然而,该领域仍面临若干关键挑战,包括缺乏统一的评估标准、结果可重复性不足以及模型解释性有限。
未来的发展方向包括:
- 进一步发展适用于复杂设计(如纵向数据)的模型,
- 引入人工智能方法以处理高维非线性关系,
- 以及强化结果验证与跨数据集泛化能力。
研究人员认为,多组学整合将成为理解微生物组–宿主互作的核心工具,并在精准医学中发挥重要作用。
整理 | DrugOne团队
参考资料
Muller, E., Bamberger, T. & Borenstein, E. Navigating multi-omic integration methods for human microbiome research. Nat Microbiol (2026).
https://doi.org/10.1038/s41564-026-02328-0
内容为【DrugOne】公众号原创|转载请注明来源
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-04-22,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

