免疫组库基础分析15:利用 NAIR 包探索疾病表型或治疗相关的 TCR/BCR 簇
免疫组库基础分析15:利用 NAIR 包探索疾病表型或治疗相关的 TCR/BCR 簇
三兔测序学社
发布于 2026-04-17 16:49:50
发布于 2026-04-17 16:49:50
编者语:
这一篇介绍了NAIR包最重要的功能,就是寻找找到与疾病状态、治疗响应或临床结局显著相关的一组相似免疫受体序列。这也是编者自己主要用的NAIR包核心代码,就是为了这一点醋,才写了前面三篇NAIR包的介绍博文。当然,这样的编写是NAIR包说明书本身的顺序,但实际生物信息学学习过程,其实可以直接从这一篇开始应用即可,再回头去学习代码基础参数与可选参数功能等内容,工具用过完成一个任务即可,不必了解如何制作过程。当然,由于每一个人的分析目的或者默认分析结果不理想,则需要个性化的研究,还是得老老实实阅读英文说明书。
在免疫组库测序(AIRR-Seq)研究中,我们常常不只关心单个 TCR/BCR 序列,更希望找到与疾病状态、治疗响应或临床结局显著相关的一组相似免疫受体序列,也就是免疫受体簇。NAIR 包提供了一套完整流程,能从批量(bulk)免疫组库样本数据中,系统性挖掘这类具有生物学意义的关联簇。
本文将完整介绍这一分析流程,从关联序列筛选、相似克隆识别,到全局网络构建与聚类分析。
一、引言
当我们拥有多份批量适应性免疫受体库测序(bulk -AIRR-Seq)样本时,可以借助 NAIR 包,研究与二分类变量相关的 TCR/BCR 簇。这里的二分类变量可以是疾病 / 健康、治疗组 / 对照组、预后良好 / 不良等。
整个分析的核心思路是:先找到组间差异显著的序列,再扩展到与之相似的序列克隆,最后构建网络并划分簇,得到最终的关联簇。
二、分析流程概览
1.识别关联序列
根据二分类变量将研究对象分为两组,使用费希尔精确检验,筛选出在两组间频率存在统计学显著差异的 TCR/BCR 序列。
2.识别与关联序列相似的克隆
对每个关联序列,设定序列相似度阈值(例如氨基酸差异不超过 1 个),定义其 “邻域序列”,并从所有样本中找出属于这些邻域的克隆。
3.构建关联克隆的全局网络
将上一步筛选出的所有克隆整合为一个全局网络,通过聚类分析将网络划分为不同簇,这些簇即为与目标表型相关的关联簇。
4.后续分析与可视化
在网络图中标记聚类编号、单独分析感兴趣的特定簇、绘制不同分组的着色方案等。
三、安装并加载 NAIR 包
首先安装并加载分析所需的核心包,这是所有步骤的基础。
# 安装NAIR包(首次使用执行)
install.packages("NAIR")
# 加载包
library(NAIR)四、模拟演示数据
为了清晰展示整个流程,我们先构建一套模拟数据,完全贴合真实研究的数据结构。
set.seed(42)
library(NAIR)
data_dir <- getwd()
dir_input_samples <- file.path(data_dir, "input_samples")
dir.create(dir_input_samples, showWarnings = FALSE)
# Number of samples by control/treatment group
n_control <- n_treatment <- 15
n_samples <- n_control + n_treatment
sample_size <- 30 # (seqs per sample)
# sequences (first five are chosen to be associated with treatment)
base_seqs <-
c("CASSGAYEQYF", "CSVDLGKGNNEQFF",
"CASSIEGQLSTDTQYF", # 3 of the associated
"CASSEEGQLSTDTQYF", # sequences differ by
"CASSPEGQLSTDTQYF", # only one amino acid
"RASSLAGNTEAFF", "CASSHRGTDTQYF", "CASDAGVFQPQHF"
)
# relative generation probabilities by control/treatment group
pgen_c <- matrix(rep(c(rep(1, 5), rep(30, 3)), times = n_control),
nrow = n_control, byrow = TRUE)
pgen_t <- matrix(rep(c(1, 1, rep(1/3, 3), rep(2, 3)), times = n_treatment),
nrow = n_treatment, byrow = TRUE)
pgen <- rbind(pgen_c, pgen_t)
simulateToyData(
samples = n_samples,
sample_size = sample_size,
prefix_length = 1,
prefix_chars = c("", ""),
prefix_probs = cbind(rep(1, n_samples), rep(0, n_samples)),
affixes = base_seqs,
affix_probs = pgen,
num_edits = 0,
output_dir = dir_input_samples,
no_return = TRUE
)
# 输入文件与分组标签
group_labels <- c(rep("control", n_control), rep("treatment", n_treatment))
input_files <- file.path(dir_input_samples,paste0("Sample", 1:n_samples, ".rds"))
length(input_files)五、步骤 1:寻找关联序列
第一步核心:筛选两组间分布差异显著的受体序列,使用findAssociatedSeqs()函数完成。根据二分类变量将研究对象分为两组,使用费希尔精确检验,筛选出在两组间频率存在统计学显著差异的 TCR/BCR 序列。
associated_seqs <- findAssociatedSeqs(file_list = input_files,
#每一个样本的路径信息
input_type = "rds",
group_ids = group_labels, #分组信息
seq_col = "CloneSeq",
min_seq_length = NULL,
drop_matches = NULL,
min_sample_membership = NULL,
pval_cutoff = 0.1 #p值小于0.1的克隆进行下游分析
)结果如下:在后续的处理步骤中,只需要关注并使用 ReceptorSeq 这一列的数据
associated_seqs[, 1:5]
#> ReceptorSeq fisher_pvalue shared_by_n_samples samples_g0 samples_g1
#> 8 CSVDLGKGNNEQFF 1.052106e-05 18 3 15
#> 7 CASSGAYEQYF 1.157316e-04 17 3 14
#> 4 CASSEEGQLSTDTQYF 5.197401e-03 10 1 9
#> 5 CASSIEGQLSTDTQYF 6.559548e-02 16 5 11六、步骤 2:查找关联克隆
基于关联序列,找到所有相似的克隆,构建序列邻域数据集
# 建立一个结果文件夹
dir_nbds <- file.path(data_dir, "assoc_seq_nbds")
# Identify clones in a neighborhood around each associated sequence
findAssociatedClones(file_list = input_files,
input_type = "rds",
group_ids = group_labels,
seq_col = "CloneSeq",
assoc_seqs = associated_seqs$ReceptorSeq,#第一步中组间有差异的TCR、BCR序列
min_seq_length = NULL,
drop_matches = NULL,
output_dir = dir_nbds #输入文件夹
)结果如下
# first neighborhood data file
one_nbd <- readRDS(list.files(dir_nbds, full.names = TRUE)[[1]])
# first few rows
head(one_nbd)
#> CloneSeq CloneFrequency CloneCount SampleID GroupID
#> Sample5.14 CSVDLGKGNNEQFF 0.02668662 2924 Sample5 reference
#> Sample7.17 CSVDLGKGNNEQFF 0.01957279 2113 Sample7 reference
#> Sample10.17 CSVDLGKGNNEQFF 0.03594648 4097 Sample10 reference
#> Sample16.10 CSVDLGKGNNEQFF 0.03404553 3802 Sample16 comparison
#> Sample16.28 CSVDLGKGNNEQFF 0.02736537 3056 Sample16 comparison
#> Sample17.3 CSVDLGKGNNEQFF 0.04114818 4603 Sample17 comparison
#> AssocSeq
#> Sample5.14 CSVDLGKGNNEQFF
#> Sample7.17 CSVDLGKGNNEQFF
#> Sample10.17 CSVDLGKGNNEQFF
#> Sample16.10 CSVDLGKGNNEQFF
#> Sample16.28 CSVDLGKGNNEQFF
#> Sample17.3 CSVDLGKGNNEQFF七、步骤 3:构建关联簇的全局网络
整合所有相似克隆,构建全局网络并划分关联簇,这是核心分析步骤。
#创建步骤2输出文件路径向量
nbd_files <- list.files(dir_nbds, full.names = TRUE)
# Combine neighborhoods and perform network analysis
all_clusters <-
buildAssociatedClusterNetwork(
file_list = nbd_files,
#输入文件路径
seq_col = "CloneSeq",
size_nodes_by = 1.5,
print_plots = TRUE
)
# 查看网络核心结果
names(all_clusters )
head(all_clusters$node_data) # 节点信息
head(all_clusters$cluster_data) # 聚类信息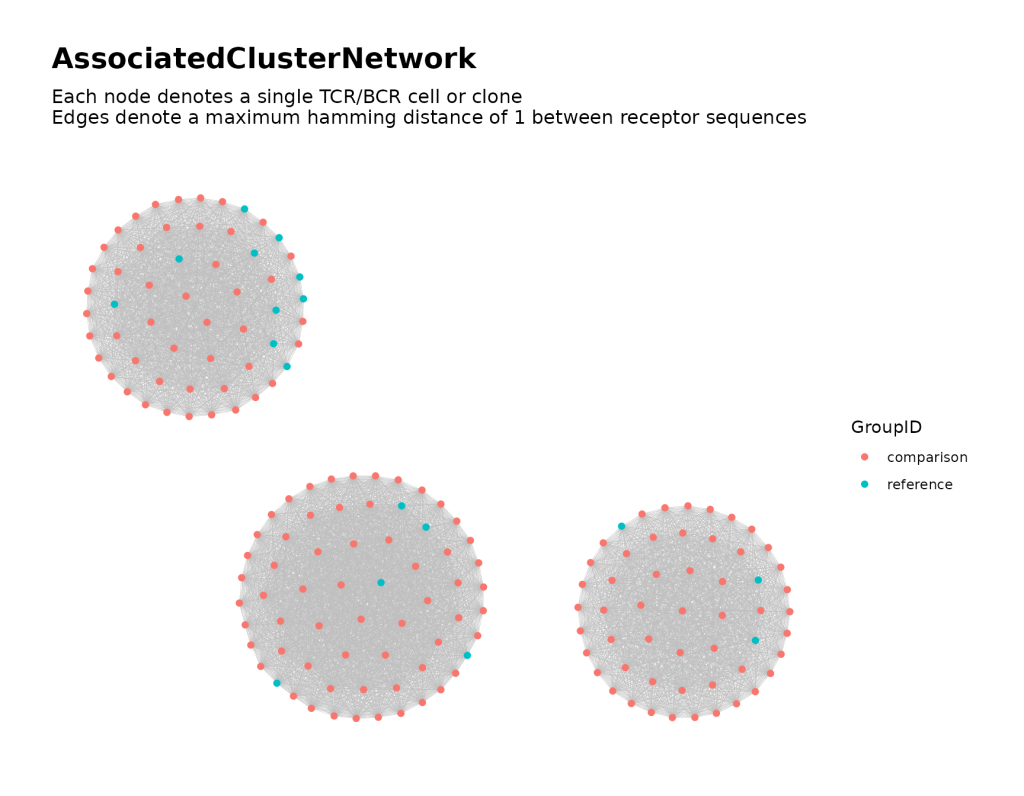
八、步骤 4:附加分析与可视化
对网络结果进行精细化分析,提升结果的实用性和可读性。
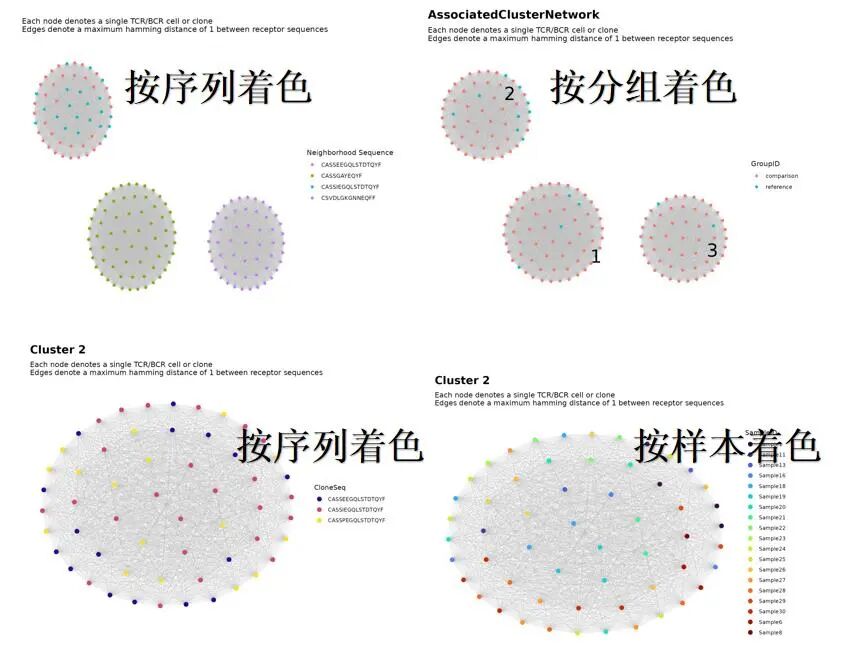
# 全局网络图,节点按关联序列着色
all_clusters <- addPlots(all_clusters,
color_nodes_by = "AssocSeq",
color_title = "Neighborhood Sequence",
size_nodes_by = 1.5,
print_plots = TRUE
)
#标记cluster簇编号
all_clusters <- labelClusters(all_clusters, size = 10)
all_clusters$plots[[1]]
# 关注特定的克隆簇
buildNet(
data = all_clusters$node_data[all_clusters$node_data$cluster_id == 2, ],
#选择簇2
seq_col = "CloneSeq",
color_nodes_by = c("CloneSeq", "SampleID"),
#选择序列或者样本ID进行分组可视化
color_scheme = c("plasma", "turbo"),
size_nodes_by = 3,
plot_title = "Cluster 2",
print_plots = TRUE
)
九、结果保存
将所有分析结果保存,方便后续论文写作与数据复用。
# 保存网络结果
saveRDS(all_clusters, "final_cluster_network.rds")
# 保存聚类表格
write.csv(all_clusters$cluster_data, "cluster_statistics.csv", row.names = FALSE)
write.csv(all_clusters$node_data, "node_information.csv", row.names = FALSE)注意事项:
步骤 | 参数名称 | 作用 | 建议关注点 |
|---|---|---|---|
Step 1 | group_ids | 定义样本分组 | 必须准确,错一位结果全错。 |
Step 1 | pval_cutoff | 设定显著性门槛 | 根据数据量调整,多重检验时可能需要更严格。 |
Step 2 | nbd_radius | 定义“相似”范围 | 设为 0 只找完全相同的序列;设为 1 找突变体。 |
Step 3 | cluster_fun | 选择聚类算法 | 默认算法通常可用,若聚类效果不好可尝试更换。 |
Step 3 | color_nodes_by | 可视化着色 | 调试时可尝试不同值(如 SampleID)以排查数据问题。 |
参考文档:https://mlizhangx.github.io/Network-Analysis-for-Repertoire-Sequencing-/articles/associated_clusters.html
免疫组库分析合集
【生信分析】免疫组库基础分析2-V/D/J基因使用频率可视化图
【生信分析】免疫组库基础分析3-基于V/D/J使用频率的聚类分析
【生信分析】免疫组库基础分析4-VJ/VDJ组合使用频率计算及可视化
【生信分析】免疫组库基础分析6-克隆子的分布分析(优势克隆与罕见克隆)
【生信分析】免疫组库基础分析10-CDR3 氨基酸理化性质分析
免疫组库分析11:Alakazam包【基因使用、多样性及氨基酸理化性质分析】使用说明
免疫组库分析12:TCR、BCR序列相似性网络分析-NAIR包介绍(1)
如果你觉得这篇博文对你有帮助,请点赞、收藏、转发!支持我们持续输出优质内容!
关注“三兔测序学社”,获取更多测序分析实用教程与前沿解读
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-04-15,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

