Science|蛋白质-蛋白质相互作用的结构发生机制
Science|蛋白质-蛋白质相互作用的结构发生机制

DrugAI
发布于 2026-03-03 17:32:55
发布于 2026-03-03 17:32:55
引言
蛋白质如何启动并进化出与其他蛋白质的相互作用,以形成结合位点和蛋白质-蛋白质界面,这一问题仍未得到充分理解。然而,进化形成蛋白质-蛋白质界面的蛋白质表面,与非相互作用的蛋白质表面相比,似乎具有独特的性质。天然蛋白质结合位点通常是给定蛋白质上最「可成药」的位点,且倾向于从组合肽库或抗体库中吸引大多数结合物。是否存在生物物理特性能够区分未进化出配体结合能力的蛋白质表面区域与天然结合位点?这一问题对药物研发具有重要意义。
#蛋白质蛋白质相互作用 #合成共进化 #结合位点 #能量景观 #上位性 #种子接触 #可成药性 #蛋白质设计
由苯丙氨酸残基间的种子接触介导的蛋白质-蛋白质复合物初始结合示意图,该过程通过上位效应传递,最终形成完整的蛋白质-蛋白质界面。
研究依据
本研究旨在探究进化出蛋白质结合能力的蛋白质表面与未进化出该能力的表面之间是否存在根本性差异。为此,通过在无配体识别历史且通常不发生相互作用的蛋白质 「沉默」表面之间设计全新界面,开展了蛋白质-蛋白质共进化的合成模拟研究。通过实验模拟并通过计算解构了蛋白质-蛋白质相互作用最初形成并随后共进化出特异性和高亲和力的过程。这种蛋白质共进化的合成模拟也能更深入地了解蛋白质天然结合位点与非天然结合位点之间的差异。
利用合成共进化设计从头界面
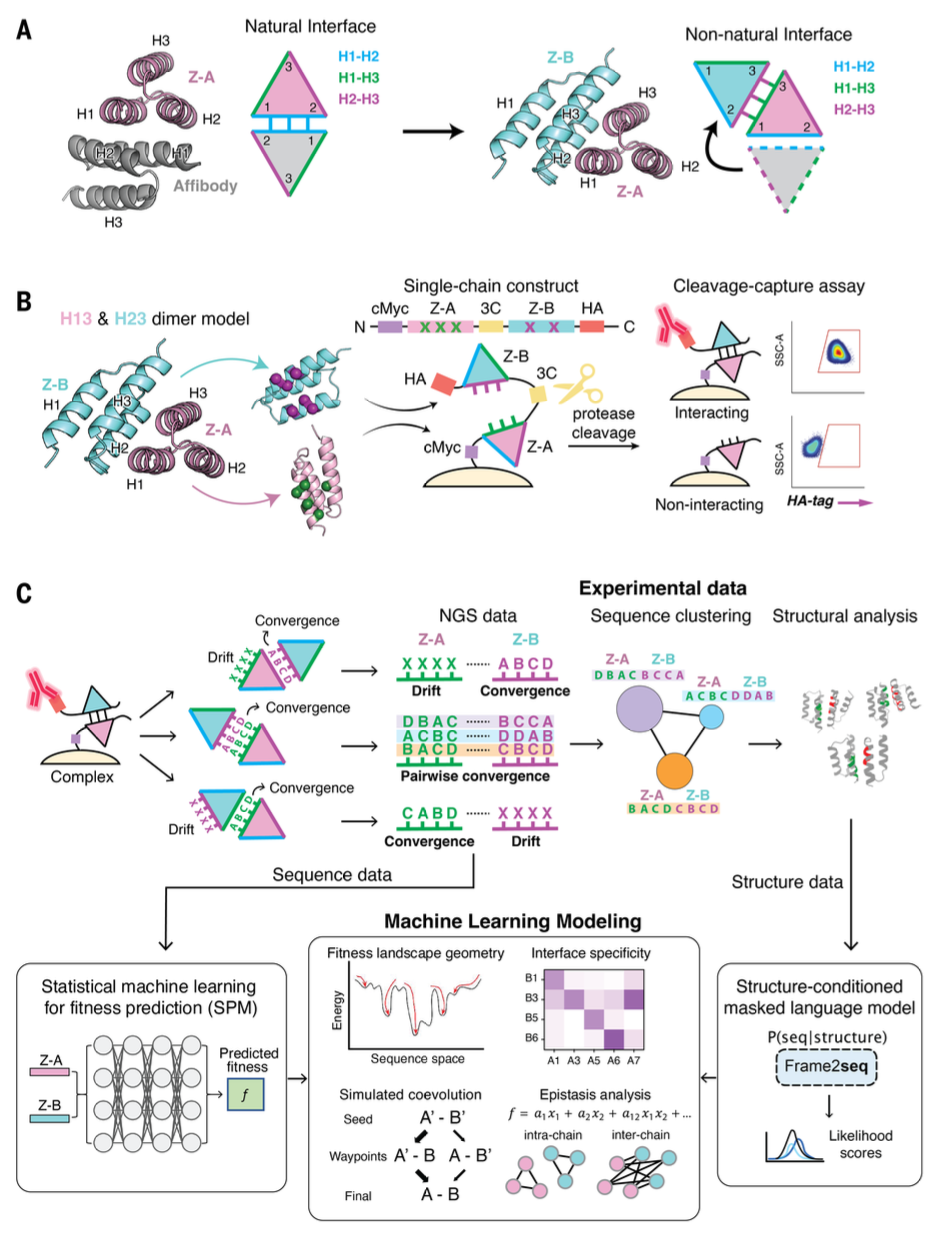
图1 合成共进化工作流程
(A)界面迁移策略概述:蛋白质Z结构域和亲和体的经典结合界面(H1-H2)被迁移至非经典H2-H3和H1-H3表面,以创建新的合成界面。
(B)基于蛋白酶的切割-捕获实验示意图:2种蛋白质作为单链构建体在酵母表面展示,通过含3C蛋白酶切割位点的柔性接头连接。切割后,相互作用的配对保留C端HA标签结合抗体的荧光,而非相互作用配对则失去HA信号,从而可基于结合亲和力进行区分;流式细胞术散点图采用侧向散射面积(SSC-A,衡量细胞颗粒度或复杂性)和别藻蓝蛋白-A(APC-A,HA标签荧光读数)进行门控。
(C)工作流程整合实验与计算方法:酵母展示筛选结合下一代测序(NGS)用于追踪序列进化、识别成对收敛,并构建基于序列关系可视化簇形成的序列相似性网络(SSNs);晶体结构验证这些簇,揭示界面结构和结合模式;NGS数据还通过统计机器学习(ML)方法建模多轮筛选数据,以获得估算的适应度景观,该景观可通过模拟共进化轨迹揭示景观几何结构,并通过上位性分析阐明关键蛋白质-蛋白质相互作用;Frame2seq提供序列-结构映射,以晶体结构为输入,将序列簇与其结构构型关联;源于这些计算模型并经界面结构验证的上位性分析,揭示关键残基-残基相互作用,为塑造蛋白质-蛋白质相互作用的进化机制提供见解。
用于进化新蛋白质界面的共进化库构建与筛选
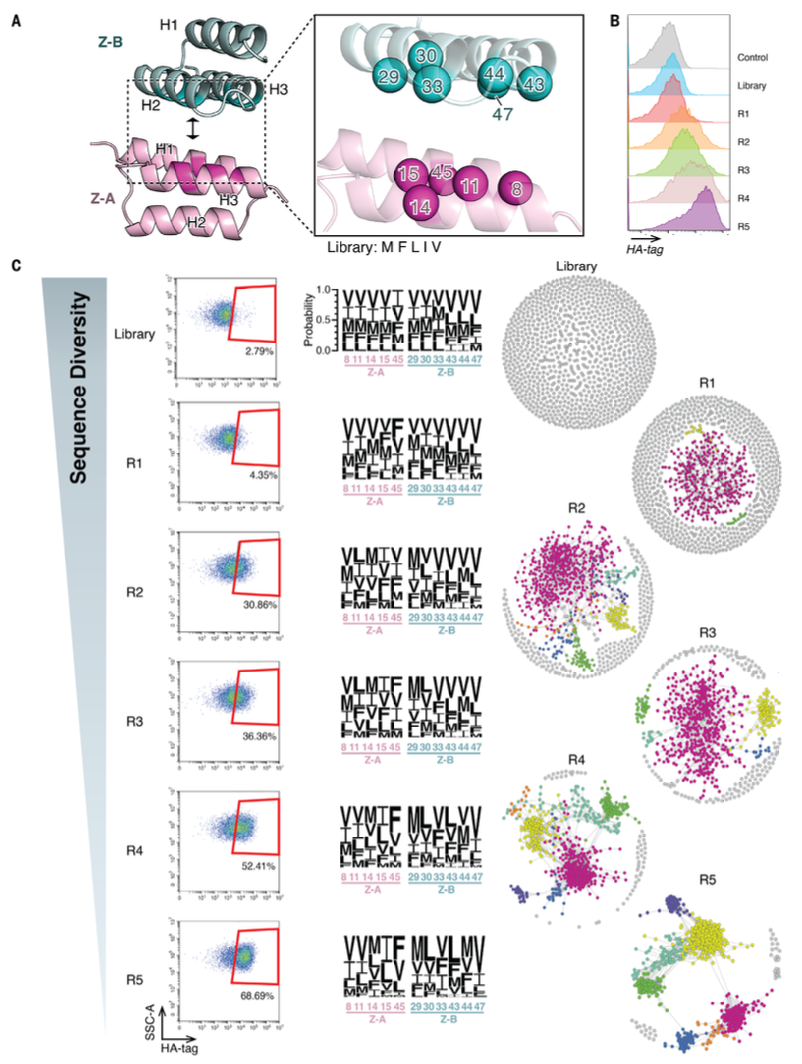
图2 共进化筛选进程
(A)针对Z结构域中非经典结合区域(Z-A的H1-H3面和Z-B的 H2-H3面)的共进化库设计:11个库位点通过5种疏水氨基酸(甲硫氨酸、苯丙氨酸、亮氨酸、异亮氨酸、缬氨酸)进行随机化。
(B)流式细胞术追踪HA标签荧光富集:在各筛选轮次中监测HA标签荧光,显示HA标签信号逐渐增加,表明相互作用配对的富集。
(C)筛选进程与序列多样性分析:(左)流式细胞术散点图展示各轮次HA标签荧光富集,后期轮次中保留荧光的细胞比例更高;(中)基于NGS数据生成的序列标志图表明,即使在最后1轮,所有库位点的氨基酸多样性仍得以维持;(右)富集序列的序列相似性网络(P<0.05)突出显示后期轮次中不同簇的出现,反映序列群落层面而非单个残基层面的收敛模式;序列相似性网络基于Z-A和Z-B蛋白质的11个氨基酸串联序列构建,当2个配对之间的编辑距离低于预设阈值时形成网络中的边;文中及图中涉及的氨基酸残基单字母缩写如下:M(甲硫氨酸)、F(苯丙氨酸)、V(缬氨酸)、I(异亮氨酸)、L(亮氨酸)。
通过序列聚类、结构和适应度景观捕捉合成界面的趋异进化
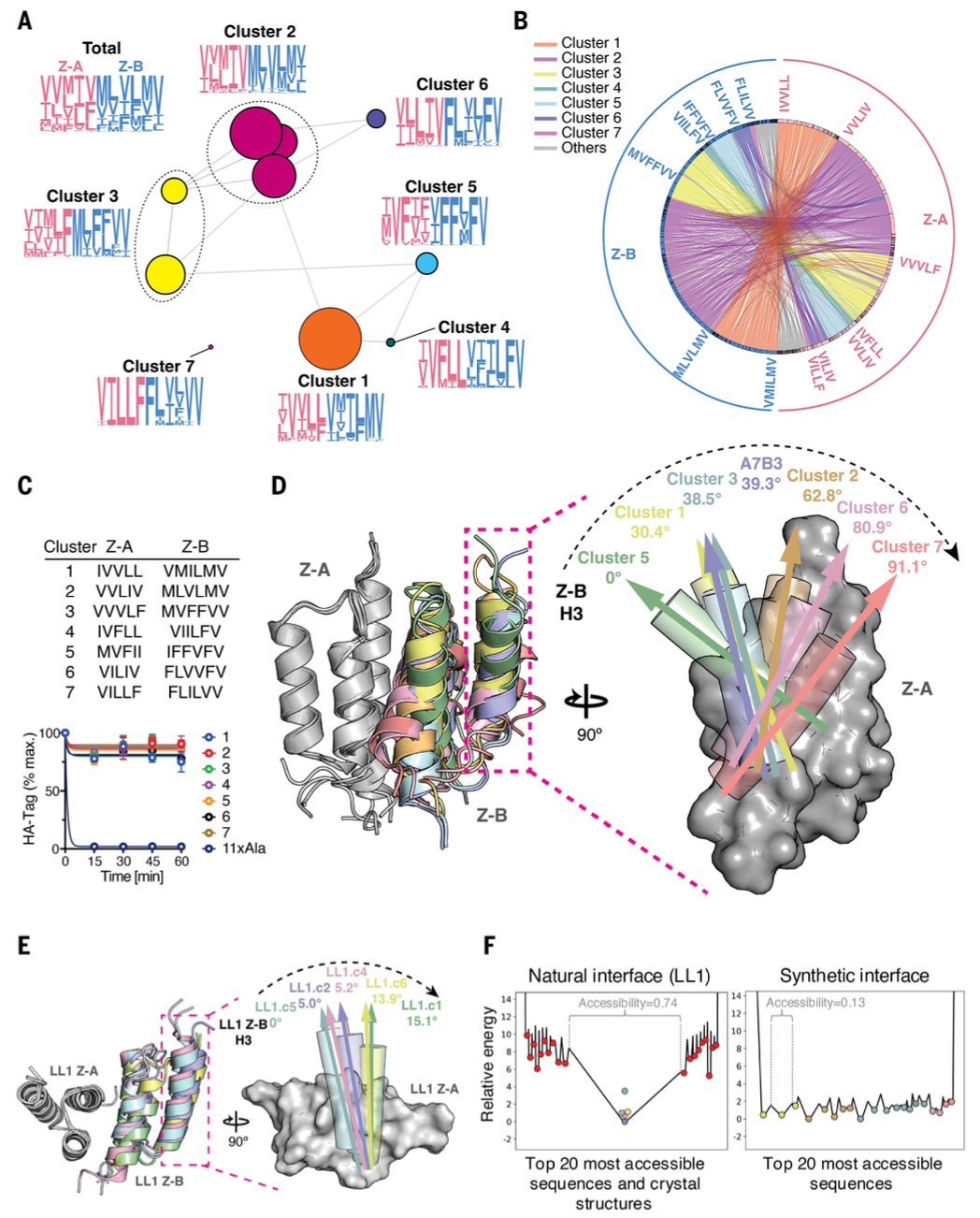
图3 合成界面的序列聚类与适应度景观
(A)第5轮序列的序列相似性网络群落图:聚类群落合并为单个节点形成群落图,识别出7个不同的簇,每个簇均表现出独特的收敛模式(如序列标志图所示)。
(B)展示第5轮NGS数据中Z-A和Z-B蛋白质之间成对关系的Circos图:每个配对被归一化为相同面积,直观呈现每个序列的大致特异性或交叉反应性;该图突出显示高正交性,序列主要在各自簇内配对,簇间相互作用极少。
(C)代表性相互作用的验证:(上)每个簇的代表性配对表格;(下)酵母切割-捕获实验证实所有测试配对均具有强结合亲和力,验证了功能性相互作用;数据为平均值±标准差;n=3个独立重复。
(D)合成界面对接取向的结构多样性:(左)合成界面复合物的叠加晶体结构;(右)Z-B螺旋3相对于簇5结构的对接角度变化,突出簇间对接几何结构的多样性。
(E)天然界面复合物中保守的对接取向:先前研究的结构表明,Z结构域与其亲和体结合物的天然界面复合物表现出相对一致的对接角度,与(D)中的合成界面复合物形成对比。
(F)天然界面(LL1 库)和合成界面的20个最易达能量井的相对能量景观:能量定义为负适应度,为便于界面间比较,对每个界面,通过减去最强结合序列的能量计算每个序列的相对能量(相对能量可在2个图之间比较,而能量本身不可比);每个能量井的宽度对应该井的可及性;在每个子图中,最易达能量井用标注其可及性的花括号标记;对于天然界面,红点表示非晶体结构的20个最易达序列,彩色点对应(E)中的晶体结构,所有晶体结构均落入同一能量井,与其保守的对接模式一致;对于合成界面,点的颜色根据(D)中结构的对应簇确定;为可视化每个景观的几何结构,对20个最易达能量井进行随机排序,但天然界面除外——天然界面始终以最深能量井为中心,其余井随机排序。
簇间特异性与交叉反应的结构洞察
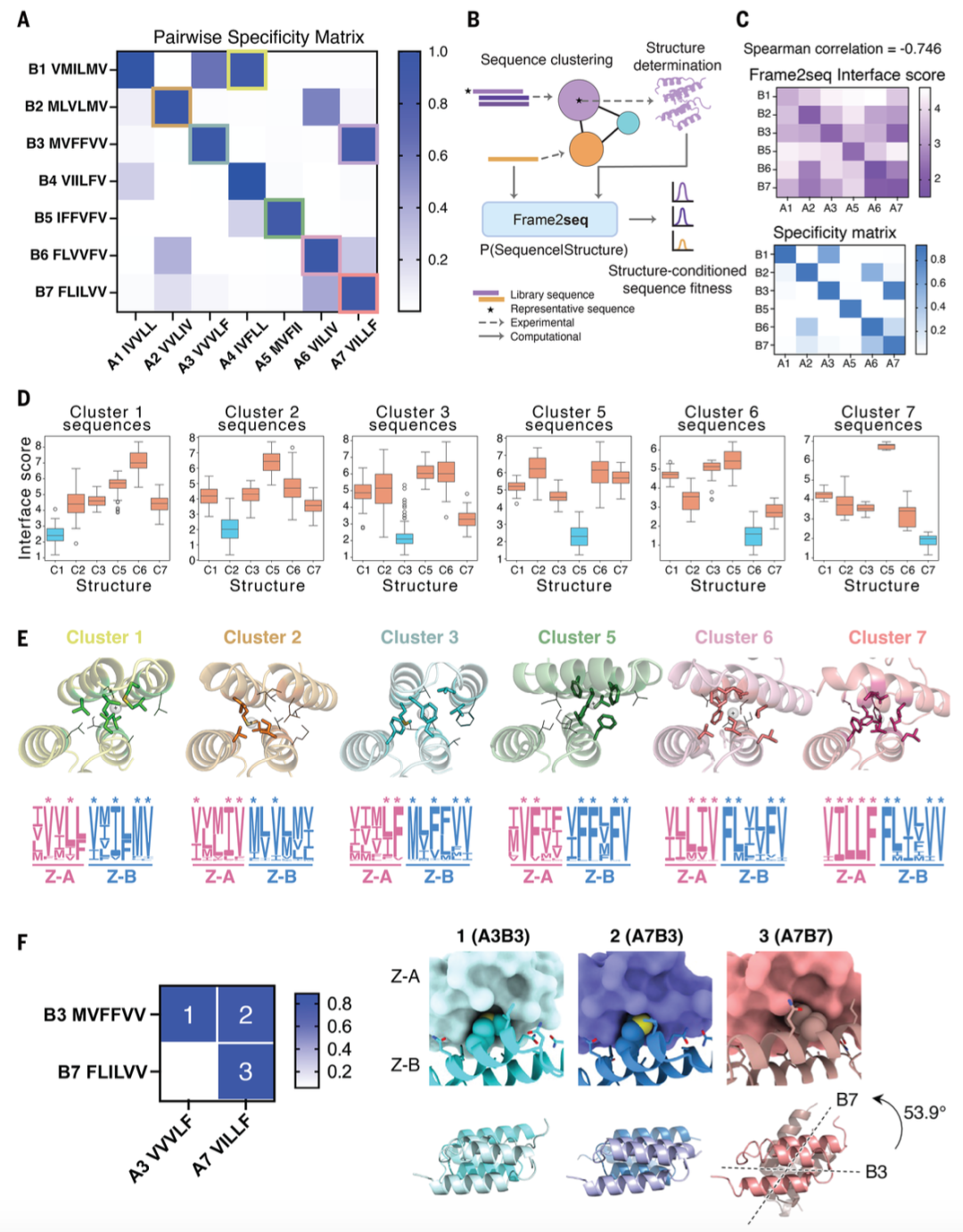
图4 簇间特异性与正交性的结构洞察
(A)图3C中代表性配对所有可能Z-A和Z-B组合的特异性矩阵:通过酵母切割-捕获实验测量的结合亲和力相对于最高亲和力(A4B4复合物)和非相互作用对照(11丙氨酸突变体)进行归一化;该矩阵显示高簇内特异性,同源配对位于对角位置;观察到部分交叉反应,包括非同源配对形成的A4B1和A7B3混合复合物;数据为n=3个独立重复的平均值。
(B)使用Frame2seq评分序列-结构兼容性的工作流程:所有库序列均针对其代表性结构进行兼容性评分。
(C)代表性序列的预测 Frame2seq 界面评分矩阵(上)和实验确定的特异性矩阵(下)(斯皮尔曼相关系数r=-0.746);Frame2seq评分为负对数似然值(分数越低表示适应度越高)。
(D)第5轮序列相似性网络簇序列在所有代表性晶体结构上的Frame2seq界面评分;正确(同源)的序列 - 结构配对以蓝色表示,错误(非同源)的配对以橙色表示。
(E)界面结构揭示收敛残基相互作用:(上)共进化复合物的界面结构以棍状模型突出显示收敛残基,其他库残基以线框模型显示;收敛残基的质心(COM)以灰色球体表示,位于界面处,表明其聚集在邻近区域;每个结构均表现出独特的质心位置,反映不同簇间相互作用和对接几何结构的差异;(下)每个簇的序列标志图阐明残基收敛,收敛残基用星号标记;这些数据表明成对残基收敛是簇特异性相互作用的基础,并与定义对接取向的独特结构决定因素相关,突显共进化界面内特异性的结构基础。
(F)(左)突出簇3和簇7配对之间偏向性交叉反应的成对特异性矩阵;(右)A7通过结合B3和B7表现出双重特异性,而 A3 仅结合 B3;左图中的相互作用强度源自(A)中的特异性矩阵;A3B3(浅青色和青色)、A7B3(蓝灰色和天蓝色)和 A7B7(橙红色和深橙红色)晶体结构的界面图和顶视图;Z-A亚基以表面模型显示,Z-B亚基以卡通模型显示,残基29ᵇ的侧链原子以球体模型显示;顶视图揭示独特的对接几何结构:在A7B7复合物中,Z-B亚基相对于A7B3复合物旋转53.9°;推定的A3B7模型无法形成稳定复合物。
合成与天然蛋白质-蛋白质界面的结构和上位性特征
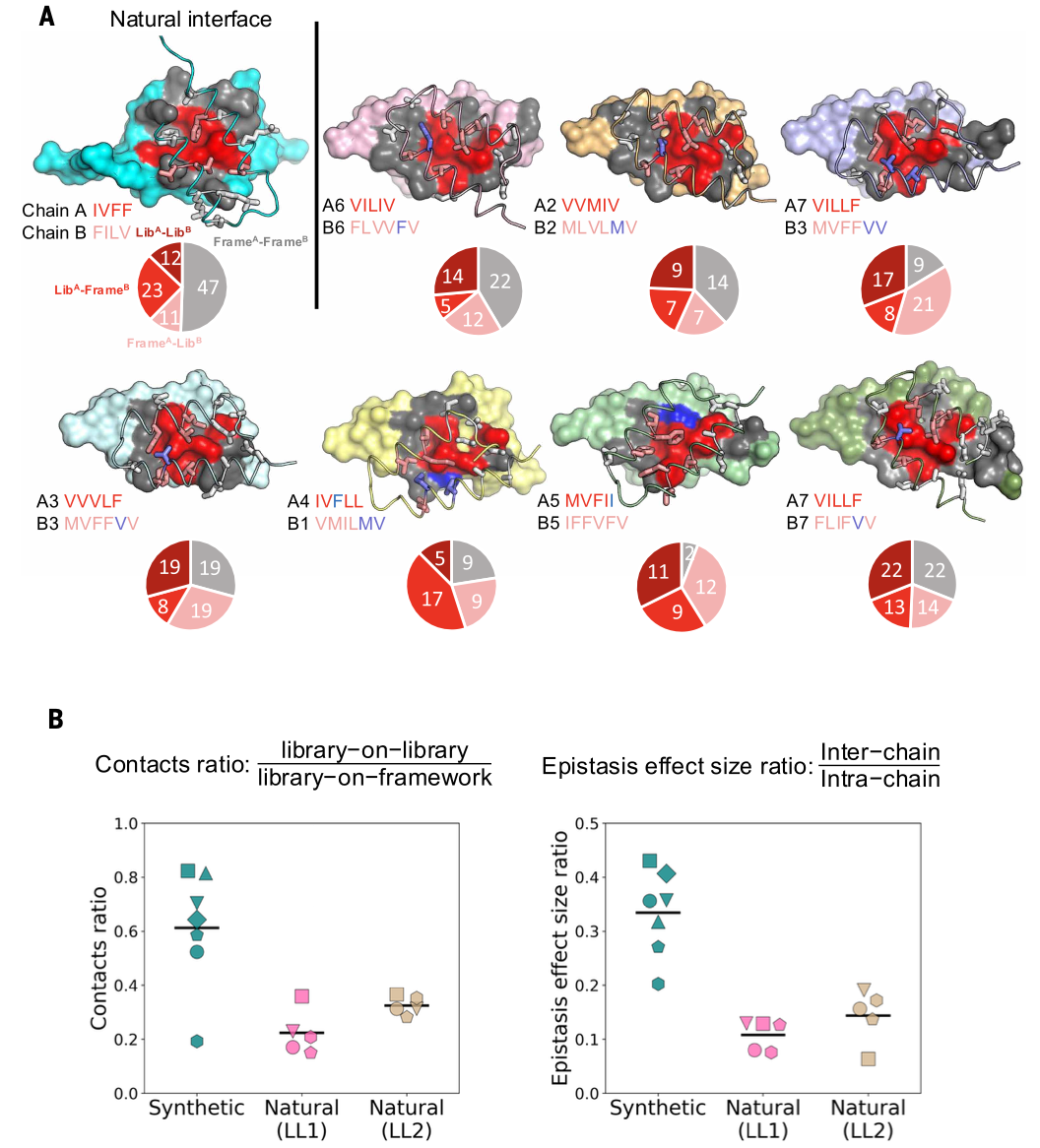
图5 界面组成的结构解析与上位性分析
(A)Z结构域链间接触:对于每个结构,链A以表面模型显示,链B以卡通模型显示,接触残基的侧链以棍状模型显示;非接触库残基为蓝色或蓝灰色,接触框架残基为灰色或白色,链A的接触库残基为红色,链B的接触库残基为橙红色;为清晰起见,省略链B的非接触螺旋;每个结构下方的饼图显示螺旋残基之间的原子接触:A 框架-B框架(灰色)、A框架-B库(橙红色)、A库-B框架(红色)、A库-B库(深红色);代表性天然界面Z结构域-亲和体配对(LL2.c22)以青色显示。
(B)晶体结构的接触比值(库-库接触与库-框架接触的比值)和SPM上位性效应大小比值(链间上位性效应大小与链内上位性效应大小的比值)散点图;对于每种界面类型,黑色水平线标记相应晶体结构的平均接触比值或上位性效应大小比值;每个晶体结构在2个图中使用相同的标记。
合成与天然界面中共进化的上位性解析
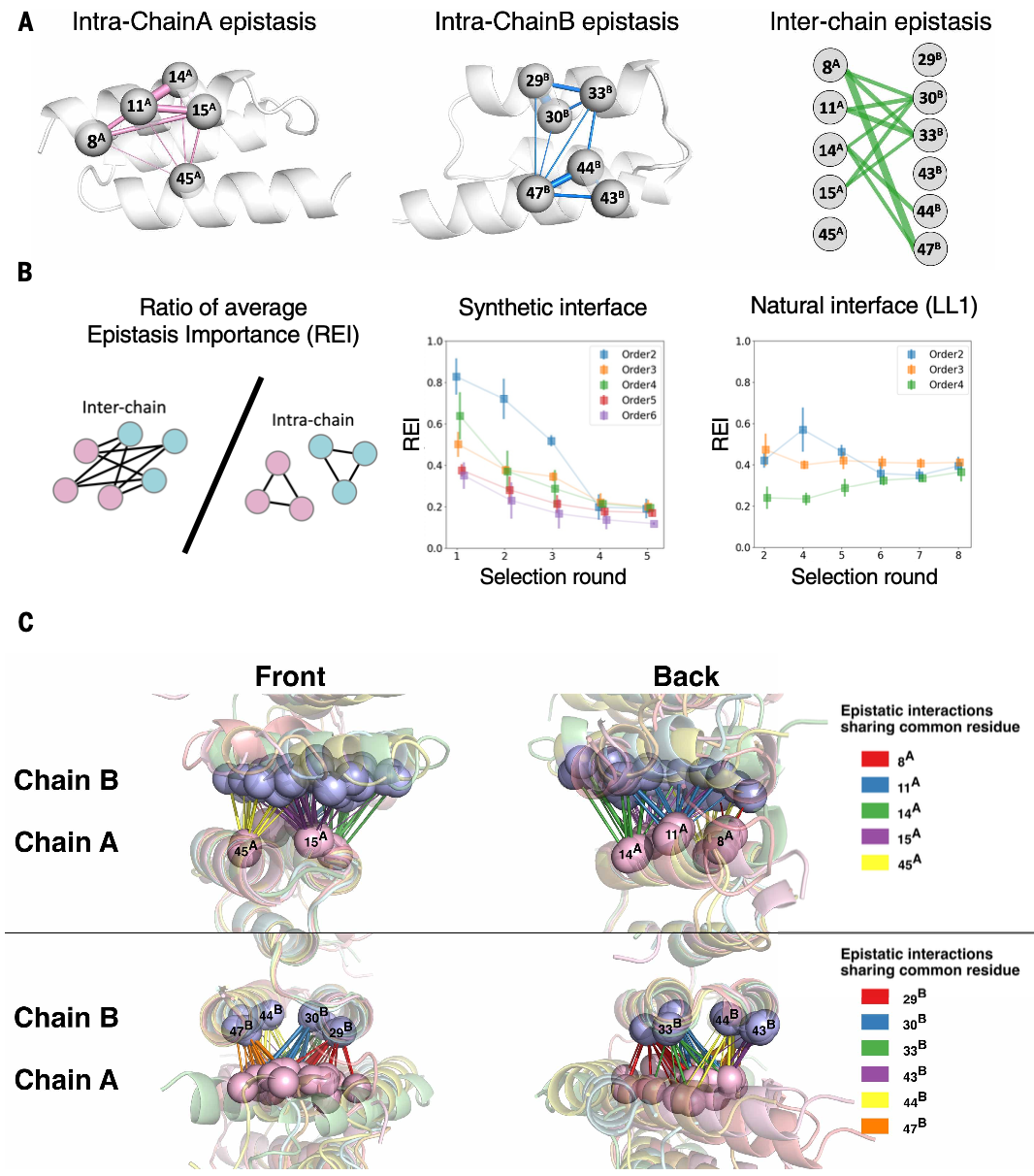
图6 共进化配对之间的上位性贡献
(A)(左和中)叠加在A5B5晶体结构上的链内成对SPM上位性可视化:连接库残基的键宽与相应上位性重要性成正比;(右)前10个链间成对SPM上位性重要性:线宽与相应上位性重要性成正比。
(B)(左)平均上位性重要性比值(REI)示意图:计算为每种相互作用阶数的平均链间SPM上位性重要性per项与平均链内SPM上位性重要性per项的比值;(中和右)合成界面和天然界面各筛选轮次实验的 REI 比较。
(C)每个簇结构的成对上位性项,当从复合物的正面(左)和背面(右)观察时,叠加并对齐在Z-A(上方)和Z-B(下方)上;球体表示库残基,条表示上位性相互作用,条的厚度表示通过Frame2seq计算的上位性强度,颜色表示所有此类相互作用中共享的残基(右侧图例亦有标注)。
共进化路径中的种子序列
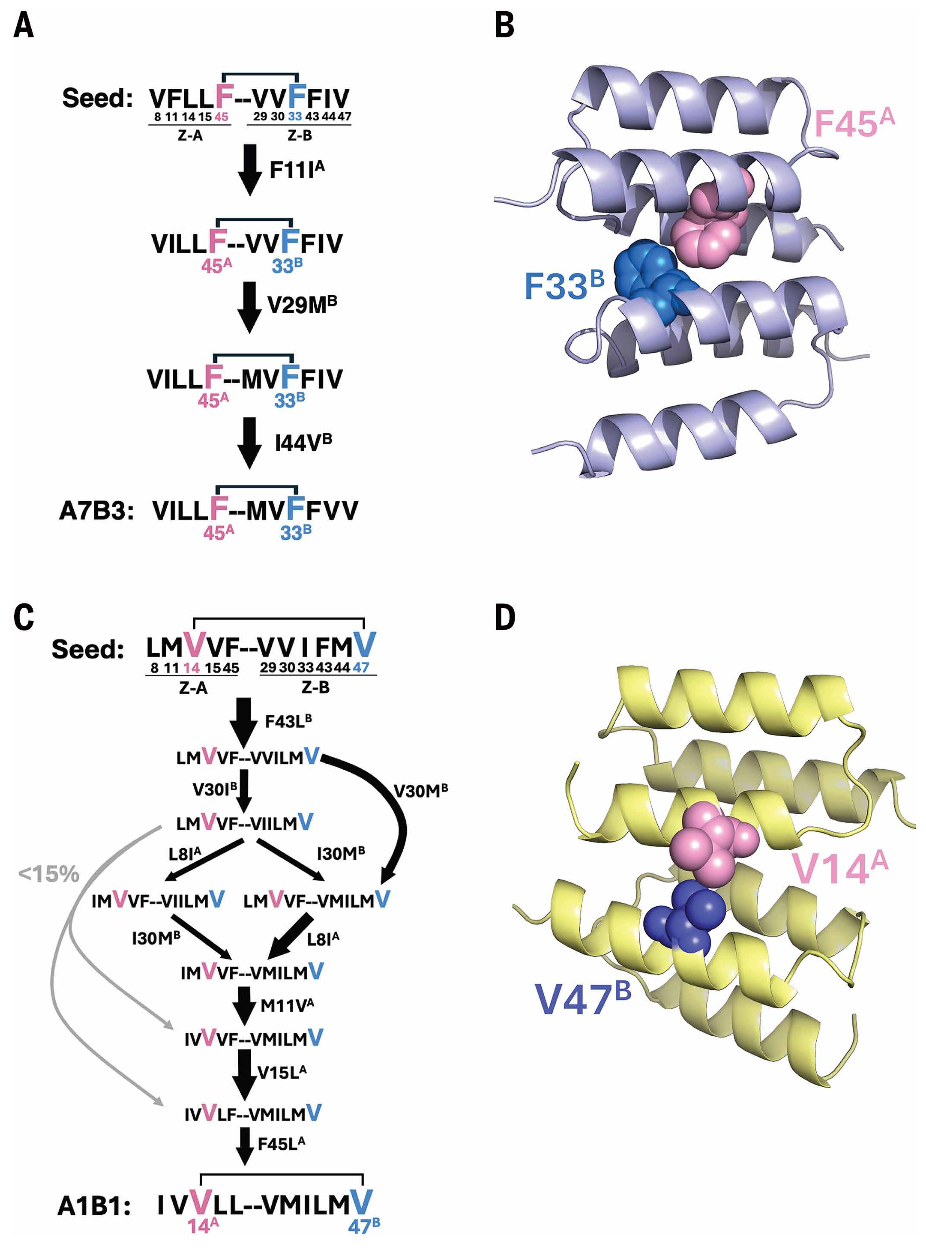
图7 种子序列启动共进化轨迹
(A)从已鉴定种子(VFLLF-VVFFIV)到A7B3的唯一能量有利共进化路径示意图:突出F45ᴬ-F33ᴮ之间顶级链间上位性的保守性。
(B)晶体结构上保守顶级链间上位性F45ᴬ-F33ᴮ的可视化。
(C)从已鉴定种子(LMVVF-VVIFMV)到A1B1的能量有利共进化路径示意图:箭头宽度与访问相应路径的模拟轨迹数量成正比;灰色箭头表示合计访问量低于所有模拟共进化轨迹15%的次要路径;路径中每个序列均突出显示保守的顶级成对链间上位性V14ᴬ-V47ᴮ。
(D)A1B1结构模型上可视化的顶级链间上位性保守性:V14ᴬ-V47ᴮ是种子、所有中间节点和A1B1的最高或第2高排名链间上位性效应大小;A1B1的结构模型通过对A4B1晶体结构进行F14V点突变构建。
结果
通过使用合成共进化平台在不受天然结合印记限制的原始表面上设计相互作用,捕捉到了前所未有的快照,阐明了从头形成蛋白质复合物的过程。发现由天然进化出蛋白质结合能力的表面形成的复合物,与由非结合表面形成的复合物相比,其上位性类型和塑造亲和力、特异性及正交性的结构适应性存在差异。改造天然表面形成的界面可产生具有独特特异性的高亲和力产物,但对接模式在深能量井中保持不变。选择由蛋白质「原始」表面介导的全新界面也能产生独特特异性,但这些特异性由浅能量井中一系列低亲和力、锯齿状对接模式介导,表明同一界面内具有显著的可塑性。为理解新界面的形成,通过机器学习估算的适应度函数模拟了进化轨迹,并结合上位性分析,揭示了在高亲和力复合物进化路径最早期阶段起启动作用的「种子」表面残基。实验数据提出了假设:进化出蛋白质结合能力的蛋白质表面具有利于配体结合的固有生物物理特性,而蛋白质的其他区域可能在进化过程中经过反选择以避免相互作用。
结论
蛋白质-蛋白质共进化平台表明,进化出蛋白质结合能力的蛋白质表面与未进化出该能力的表面之间存在差异。事实上,在本研究的系统中,在无进化结合印记的蛋白质表面之间设计的复合物,其能量适应度和亲和力似乎存在上限。这些数据解释了为何天然结合位点能吸引结合物:替代表面具有浅能量景观,不利于紧密结合,这可能是由于进化反选择所致。这在一定程度上可以解释「不可成药」蛋白质表面的存在,并为克服这一障碍提供新的基于生物物理的策略。
详细总结

思维导图(mindmap)
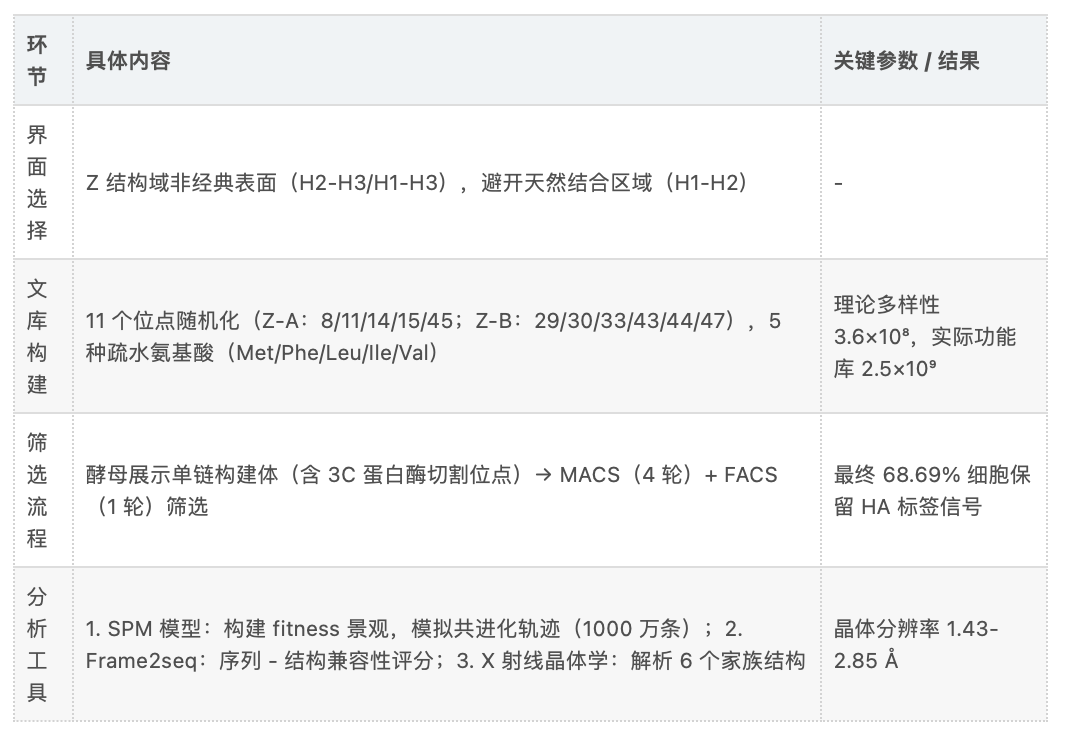
实验设计与方法
天然vs合成界面的能量景观差异

参考
Science. 2026 Feb 12;391(6786):eadx6931. doi: 10.1126/science.adx6931. Structural ontogeny of protein-protein interactions
260212PPI.pdf
注:AI辅助创作,如有错误欢迎指出。内容仅供参考,不构成任何建议。
End
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-02-18,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

