客户引用| 清华团队 Science 发文!AI 24 小时 “扫遍” 人类基因组,虚拟筛选新突破!
原创客户引用| 清华团队 Science 发文!AI 24 小时 “扫遍” 人类基因组,虚拟筛选新突破!
原创
陶术
发布于 2026-03-27 16:55:38
发布于 2026-03-27 16:55:38
人类基因组中约 20,000 个蛋白编码基因仅 10% 被药物靶向,大量潜在药物靶点未被探索。
现有虚拟筛选方法(如分子对接、传统深度学习)计算成本极高,无法覆盖全基因组靶点,限制了药物研发效率。
AlphaFold 等蛋白结构预测技术的突破,为全基因组药物发现提供了可能,但缺乏适配的高效筛选工具。
2026年1月,来自清华大学智能产业研究院(AIR)的兰艳艳教授、生命学院的张伟副教授、闫创业副教授及化学系的刘磊教授带领的研究团队在 Science 发布了一篇题为 "Deep contrastive learning enables genome-wide virtual screening" 的文章,开发了AI驱动的超高通量药物虚拟筛选平台 DrugCLIP。

DrugCLIP 模型设计
DrugCLIP 模型框架图如下:
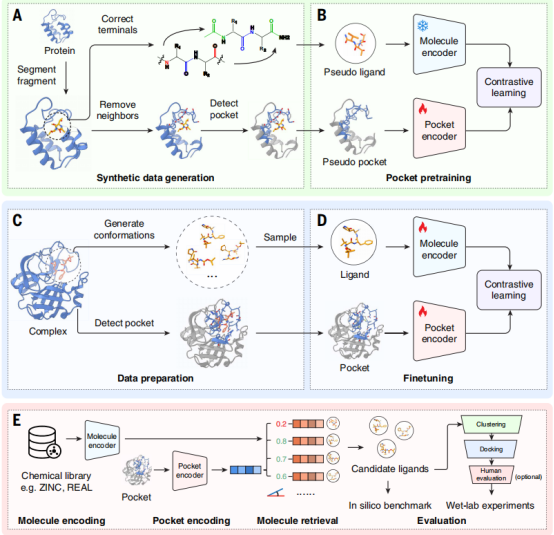
该模型本质是给蛋白和小分子做 “专属编码”(蛋白的凹槽形状、表面化学基团;小分子中能形成氢键的基团、大小形状等),再通过已知的“蛋白口袋 - 小分子结合对”训练 DrugCLIP,使其能够快速从海量小分子里找到能和蛋白精准结合的一个。
DrugCLIP 的基准测试与湿实验验证
基准测试:
研究团队首先证明在 DUD-E (虚拟筛选基准数据集)和 LIT-PCBA (虚拟筛选与机器学习专用基准数据集) 上,DrugCLIP 在 1% 富集因子(EF1%)指标(该指标用于衡量虚拟筛选模型的召回能力)上优于所有基准方法。
随后,通过实验,证明在速度和准确性上均优于传统分子对接和主流深度学习方法(38秒远快于机器学习模型 PLANET 的3小时),且在化学骨架、蛋白家族的泛化性以及结构扰动的稳健性上优于热门虚拟筛选方法 AutoDock Vina。
湿实验验证:
DrugCLIP模型为精神疾病关键靶点5-HT₂AR筛选出最终有效分子命中率约 7.7%(6/78),远高于传统筛选方法(通常<1%)。其中候选分子兼具高亲和力(Ki 低至 21.0nM)和强功能活性(EC₅₀低至 60.3nM),且化学结构新颖,为开发新型非致幻抗抑郁药物提供了优质起点。
实验验证了 DrugCLIP 对 GPCR 类靶点的泛化能力,其筛选结果可直接支撑后续药物优化(如结构修饰提升活性、降低毒性)
DrugCLIP模型从160万个候选分子中为去甲肾上腺素转运体(NET)靶点,筛选出约100个高评分分子,其中15%为有效抑制剂(有12 个阳性分子的 IC₅₀优于安非他酮),更有2 个化合物表现突出:0086-0043(IC₅₀=1.14μM)、Y510-9709(IC₅₀=0.31μM),活性显著提升。并通过冷冻电镜技术成功解析两个复合物的高分辨率结构(分辨率分别为 2.87Å、2.98Å)。
DrugCLIP 在 AlphaFold 预测结构中的应用
结合 GenPack (针对 AlphaFold 预测结构的口袋检测精度问题,该模型优化口袋定位,提升虚拟筛选性能)后,DrugCLIP 在 AlphaFold 预测的蛋白结构上的表现显著优于分子对接和诱导契合对接方法。针对缺乏已知完整结构和配体的靶点 —— TRIP12(多种肿瘤、帕金森综合征的潜在靶点),该模型成功识别出小分子抑制剂,表面等离子体共振检测的命中率达 17.5%,其中两个亲和力较高的分子也对TRIP12的泛素连接酶活性有一定抑制活性
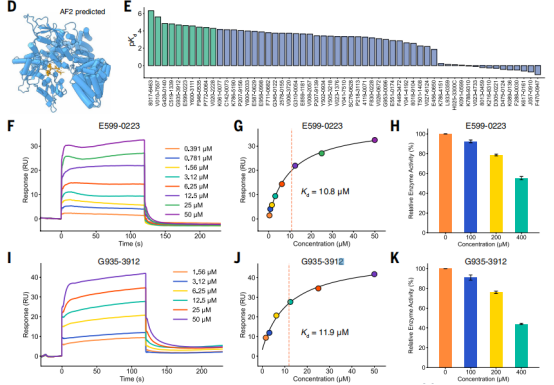
靶点验证过程
全基因组虚拟筛选实践
研究团队利用 DrugCLIP 对约 10,000 个人类蛋白与 5 亿个化合物进行了全基因组虚拟筛选,仅用 8 块图形处理器就在 24 小时内完成了超过 10 万亿次蛋白 - 配体配对打分。筛选结果产生了 200 多万个候选分子,覆盖约 20,000 个口袋,约占人类基因组的一半,所有筛选数据已向公众开放。
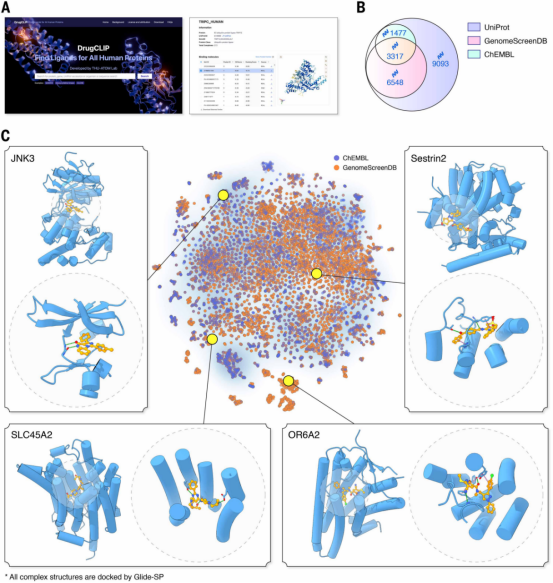
全基因组虚拟筛选结果与 GenomeScreenDB 数据库
结论
DrugCLIP 是一种超快速虚拟筛选方法,现已经过计算机模拟基准评估和湿实验严格验证。该技术可实现对人类可成药蛋白质组进行万亿级筛选,提供了开放获取的资源,为下一代药物研发(尤其是针对了解较少的靶点)奠定了基础。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
评论
登录后参与评论
推荐阅读

