空间组学新纪元:从组织架构到临床决策,深度解码肿瘤生态系统的演进与转化
空间组学新纪元:从组织架构到临床决策,深度解码肿瘤生态系统的演进与转化

生信大杂烩
发布于 2026-01-06 14:55:51
发布于 2026-01-06 14:55:51
导读
在过去十年中,单细胞组学技术如同一把“手术刀”,将复杂的肿瘤组织拆解为遗传、表观遗传和转录程序各异的单个细胞,极大地深化了我们对肿瘤异质性的理解。然而,正如仅凭零件清单无法理解一台机器的运作原理,缺乏空间背景(Spatial Context)的单细胞研究难以解析组织架构、细胞间相互作用以及决定免疫反应和治疗预后的功能生态位(Functional Niches)。近日,来自德克萨斯大学 MD 安德森癌症中心的 王凌华(Linghua Wang) 教授团队在 Cancer Cell 杂志发表了题为 Spatial omics at the forefront: emerging technologies, analytical innovations, and clinical applications 的重磅综述。文章系统性地梳理了空间组学技术的最新进展,探讨了如何通过计算创新(如多模态整合、空间大模型)将空间模式转化为机械性洞察,并勾勒出空间组学从基础发现走向精准肿瘤学临床应用的技术路线图。
一、 空间革命:从单模态向高通量、多组学的跨越
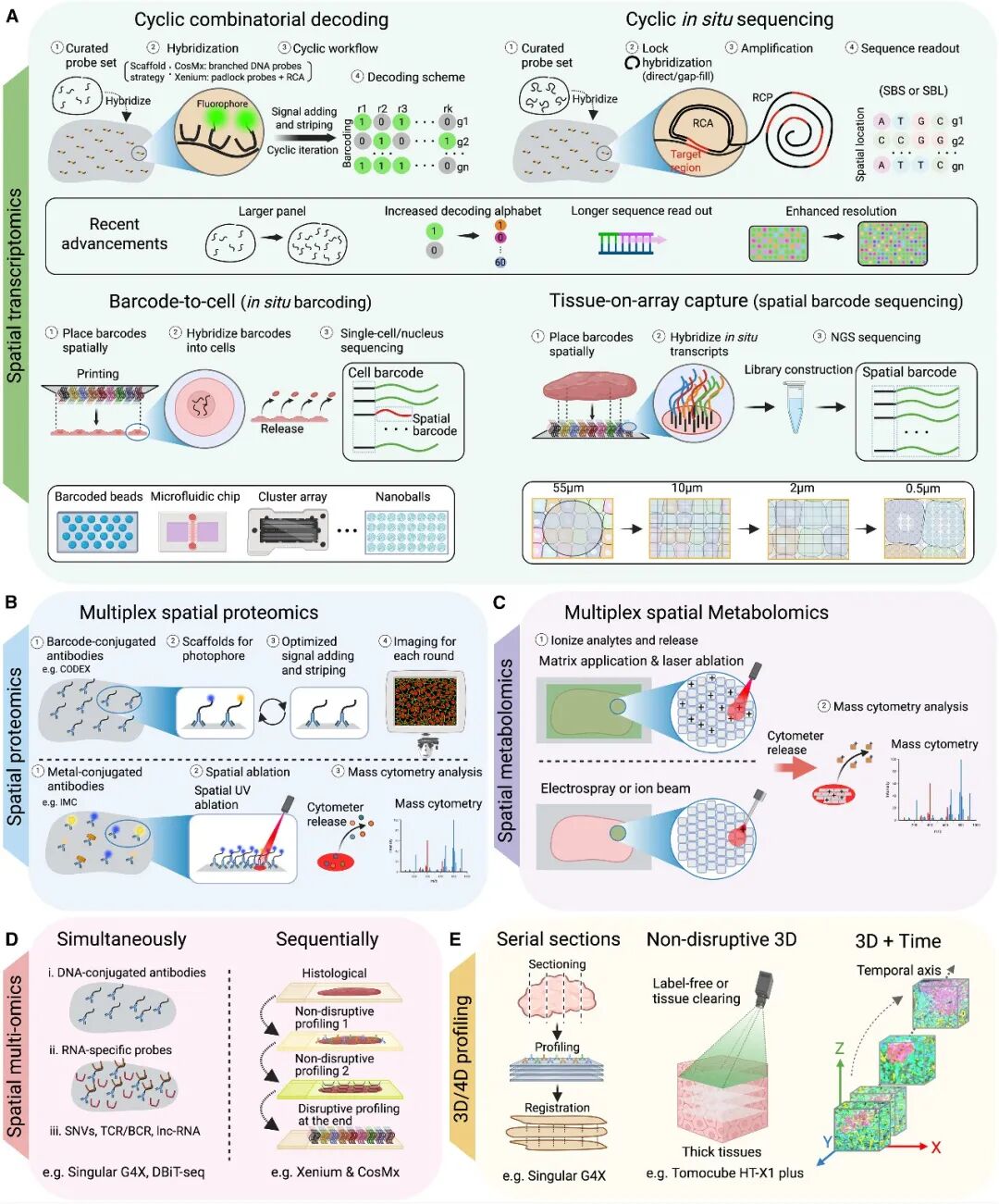
空间组学技术正经历着从“概念验证”到“商业化普及”的急剧转变。目前,主流技术可根据其原理分为空间转录组学、蛋白质组学和代谢组学三大领域。
- 空间转录组学:解析基因表达的“坐标系” 目前的商业化平台主要分为基于成像(Imaging-based)和基于测序(Sequencing-based)两大类: • 成像技术:如 Xenium (10x Genomics) 和 CosMx (Bruker)。前者通过锁式探针(Padlock probes)和滚动循环扩增(RCA)实现亚细胞分辨率,目前最高可检测 5,000 种基因;后者利用分支探针技术,已实现高达 18,000 种基因(全转录组)的检测。 • 测序技术:如 Visium HD 和 Stereo-seq。这些技术通过空间条形码捕捉原位转录本,具有全转录组覆盖的优势。其中 Stereo-seq 利用 DNA 纳米球阵列,分辨率可达 500 纳米。
- 空间蛋白质组学与代谢组学:连接功能与表型 蛋白质是功能的直接执行者。目前的平台如 PhenoCycler (CODEX) 和 IMC (成像质谱流式) 可检测 40-100 种蛋白质标记物,有效识别血管内皮(CD31)或免疫细胞亚群。此外,空间代谢组学(如 MALDI-IMS)通过直接图谱化组织上的小分子和脂质,为研究代谢梯度提供了可能。
- 下一代创新:同片组织的多组学与三维成像 真正的突破在于同片组织的多组学(Same-section Multi-omics)。新兴平台已支持在同一张切片上相继或同步检测 RNA、蛋白质甚至代谢物。同时,空间组学正从 2D 向 3D/4D 演进,通过连续切片重建或非破坏性体积成像(如光片显微镜),构建出立体的肿瘤生态系统模型。
二、 计算突破:赋予空间数据“生物学灵魂”
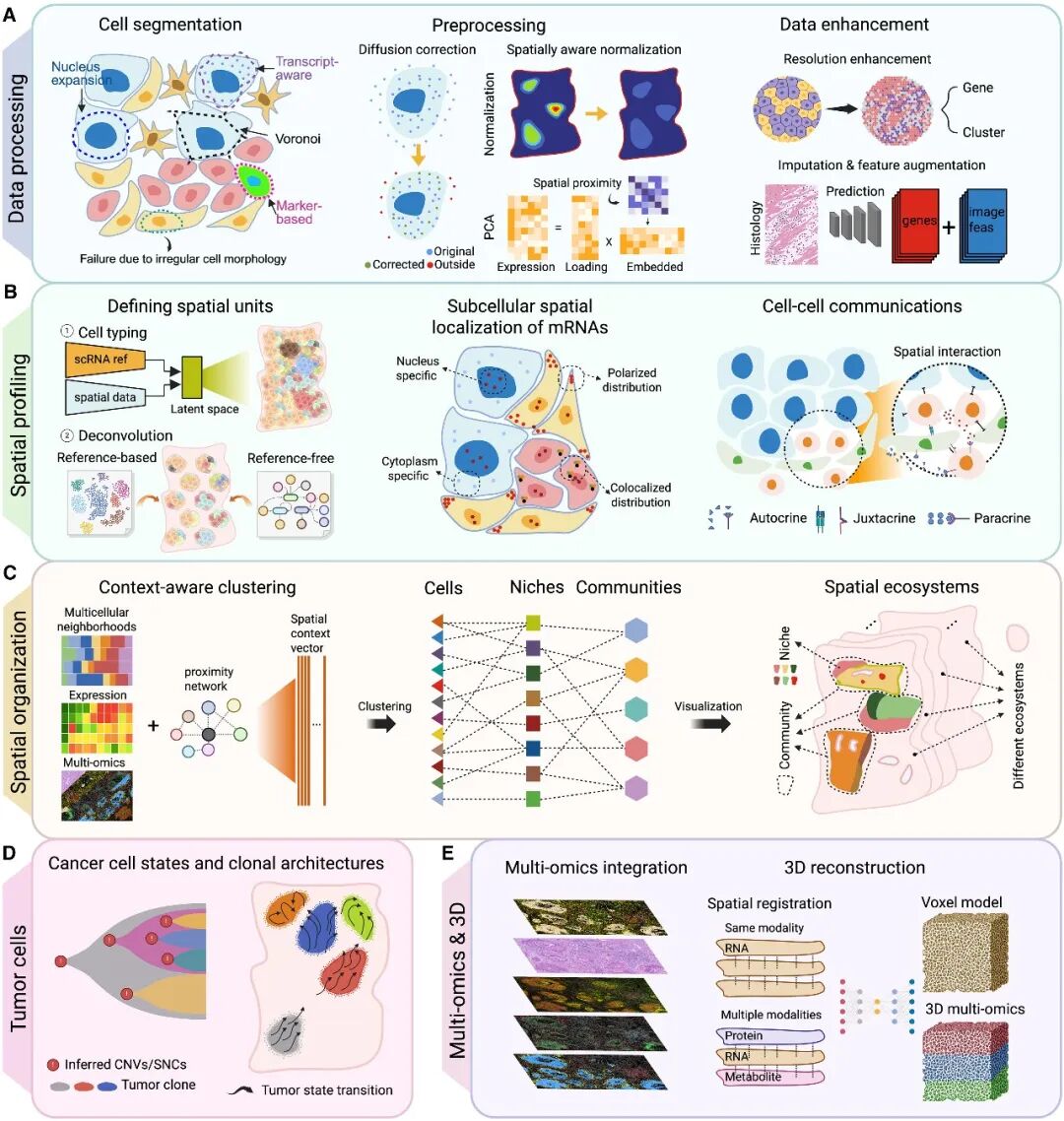
随着数据通量的爆炸式增长,单纯的实验产出已不足以回答复杂的科学问题。计算分析的创新成为了连接原始数据与机制洞察的桥梁。
- 基础数据处理:从分割到增强 • 细胞分割(Cell Segmentation):由于肿瘤细胞形态多样且紧密堆积,准确划分细胞边界至关重要。目前的方法已从单纯依赖核染色(DAPI)演变为结合细胞膜信号和转录本分布规律的综合模型(如 Segger)。 • 分辨率提升与特征扩充:利用图卷积网络(GCN)和自监督学习(如 TESLA),研究者可以将低分辨率的点(Spot)细分为亚点水平,甚至从标准的 H&E 图像中预测蛋白质的空间表达。
- 高阶分析:细胞间通讯与生态系统建模 空间转录组学最独特的优势在于能直接在原位推断细胞间通讯(Cell-cell Communication)。与单细胞数据不同,空间分析可以将配体-受体(LR)相互作用限制在相邻细胞之间,极大地降低了假阳性。 此外,**空间基础模型(Foundation Models, FMs)**的兴起(如 UNI、scGPT-spatial)为跨平台数据整合和细胞类型预测提供了强大的 backbone,使得从嘈杂的空间数据中提取广义生物学特征成为可能。
三、 解码 TME 复杂性:九大关键空间生态位
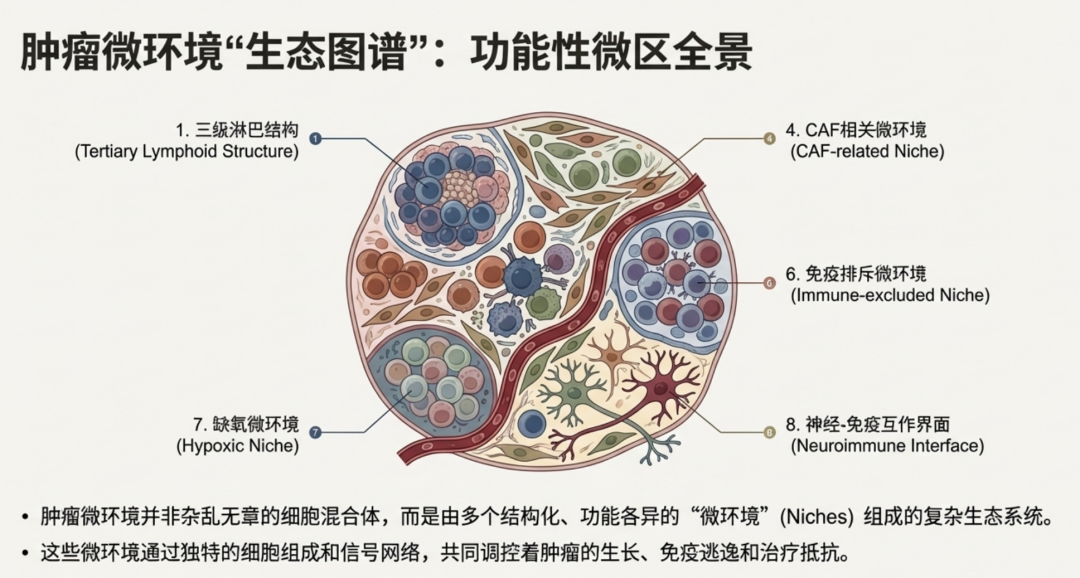
肿瘤微环境(TME)并非混乱的细胞堆砌,而是由具有功能协调性的空间生态位(Spatial Niches)构成的有序系统。文章详细总结了九种具有重要生物学意义的空间龛位:
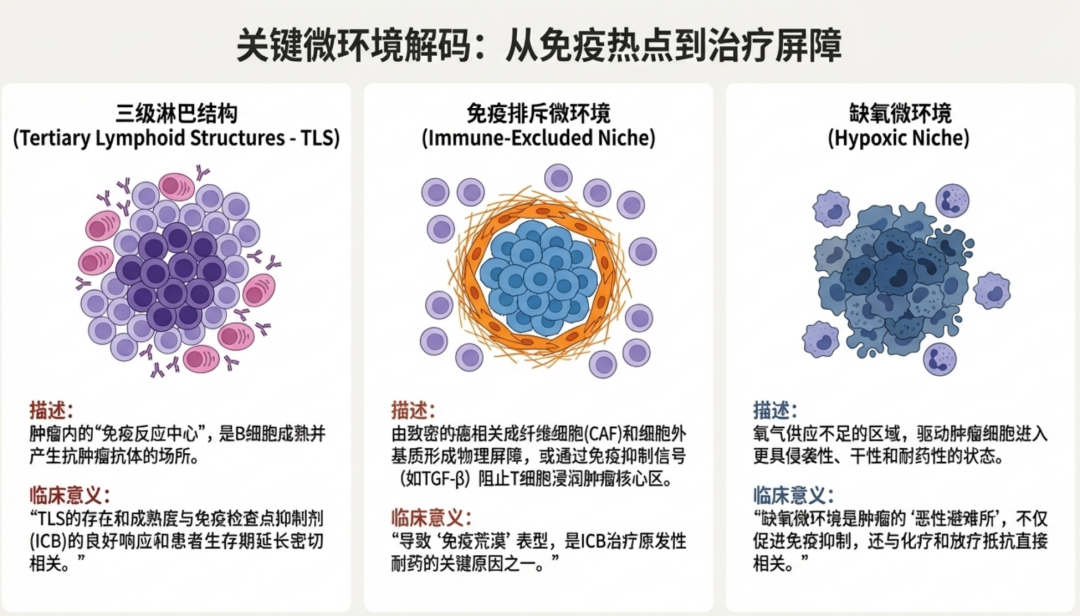
- 三级淋巴结构 (TLS):局部 B 细胞成熟的场所,其成熟度与免疫治疗反应密切相关。
- 血管周围生态位 (Perivascular Niches):调节免疫细胞招募与启动的中心枢纽。
- 干细胞样 CD8+ T 细胞生态位:维持抗肿瘤免疫的“蓄水池”,这类细胞的丰度是 ICB 反应的有力预测因子。
- CAF 相关生态位:不同亚型的肿瘤相关成纤维细胞(CAFs)通过重塑基质,形成免疫排斥屏蔽层。
- 肿瘤侵袭前沿 (Tumor Invasive Front):癌细胞与间质相互博弈的活跃地带,常伴随免疫抑制和表型重塑。
- 免疫排斥生态位 (Immune-excluded Niches):淋巴细胞聚集在基质周边但无法渗入瘤体,由致密的 ECM 或 TGF-β 信号驱动。
- 缺氧生态位 (Hypoxic Niches):低氧诱导的代谢重编程中心,常聚集侵略性强的癌细胞和抑制性巨噬细胞。
- 神经-免疫接口 (Neuroimmune Interface):神经信号(如神经递质)调控局部免疫的新兴研究方向。
- 微生物生态位 (Microbiota-residing Niches):研究表明,富含特定微生物(如具核梭杆菌)的龛位通常呈现高度免疫抑制状态。
四、 临床转化:精准肿瘤学的下一块基石
空间组学不仅是基础研究的利器,更是临床决策的潜在关键。它能将患者的临床表现与切片上的分子机制直接挂钩,实现“从病床到实验室再回到病床”的闭环。
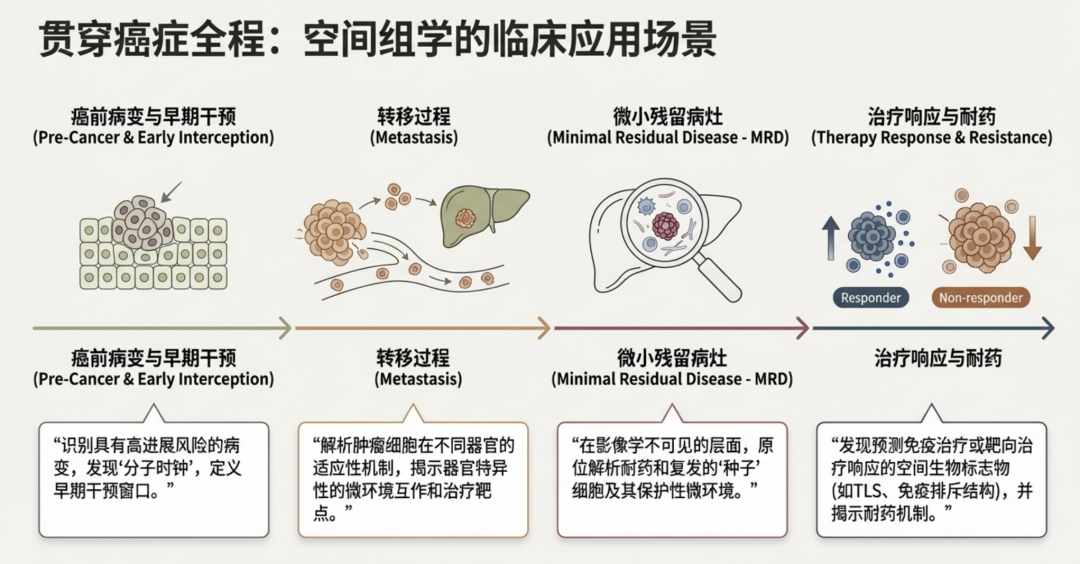
- 早癌研究与拦截 空间组学可绘制癌前病变向侵袭性癌症演变的“分子时钟”。通过识别早期龛位中的风险标志物(如干扰素响应程序),临床医生可以界定最佳的干预窗口。
- 转移演进与微小残留病 (MRD) 转移是一个多步骤的级联过程。空间分析揭示了癌细胞如何利用器官特异性的“信号枢纽”进行定植。对于 MRD,空间组学能识别那些隐匿在术后残余组织中的耐药细胞状态(如缺氧或转运蛋白上调),为清除残余病灶提供靶点。
- 辅助临床试验与生物标志物开发 目前的临床应用案例已初现曙光。例如,王凌华教授团队的一项研究显示,在卵巢透明细胞癌中,具有 PPP2R1A 突变的肿瘤显示出独特的 TLS 密度和 B 细胞景观,这一空间特征与患者对免疫检查点抑制剂(ICB)的优异反应相关。 图 5. 展示了空间组学在早癌转化、转移演变、MRD 监测及治疗反应评估中的应用路径。
五、 挑战与未来展望
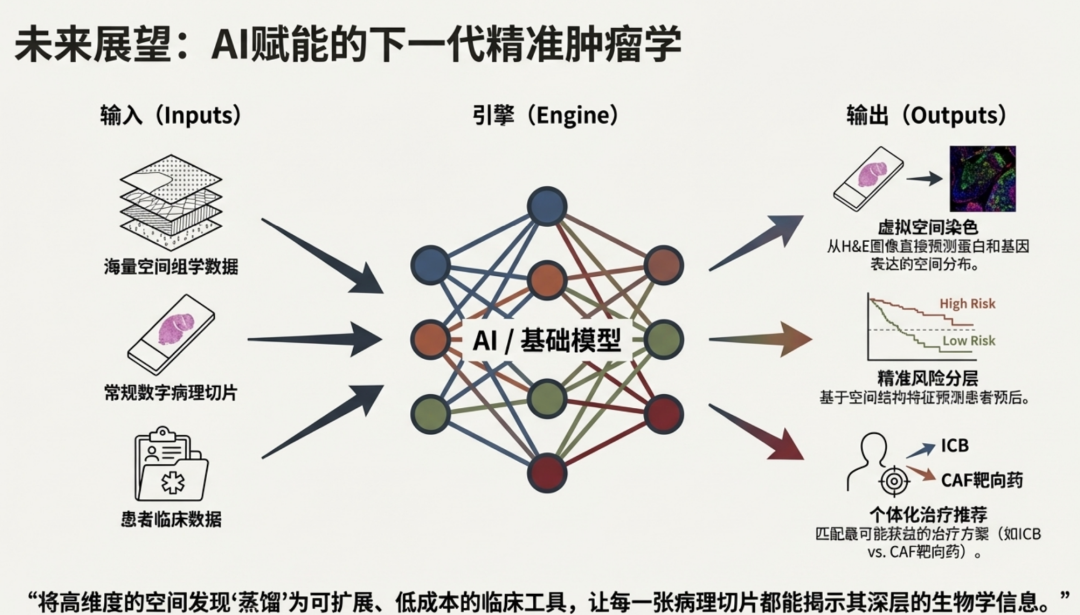
尽管空间组学展现了前所未有的潜力,但要实现广泛的临床应用仍需跨越重重障碍: • 标准化与成本:高深度、高通量的实验目前成本极高且缺乏统一的数据标准。 • 计算可解释性:AI 模型(如 Pathomics)在辅助诊断时,其解释性和透明度对于临床决策至关重要。 • 跨学科协作:这需要临床医生、病理学家、计算科学家和 AI 研究员的紧密配合。
结语
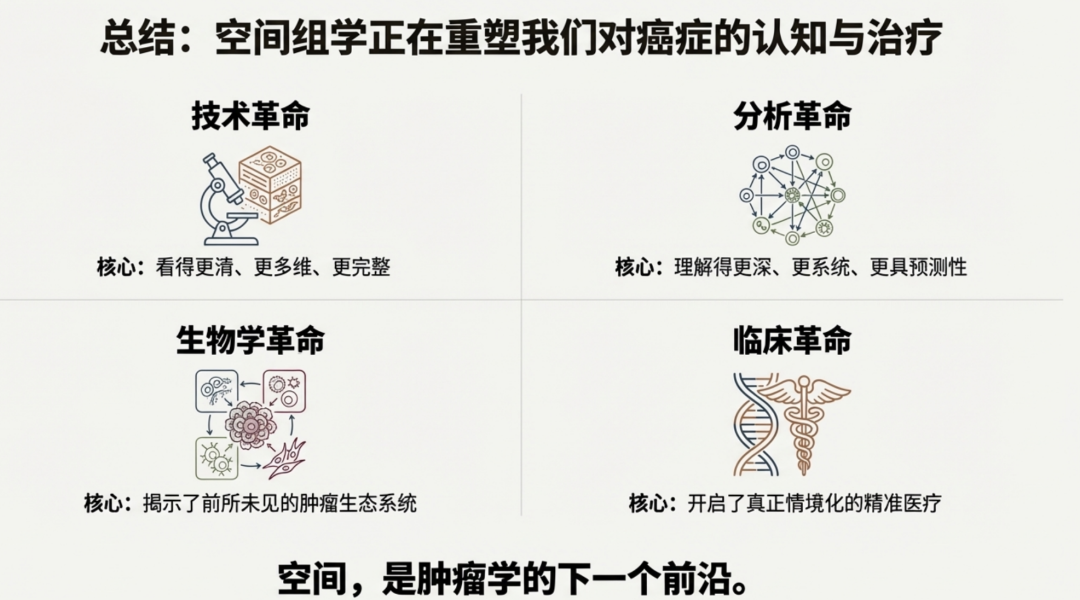
空间组学正在以前所未有的分辨率重构我们对癌症的认知。如果说单细胞测序让我们看清了“演员”是谁,空间组学则让我们看清了整部“戏剧”是如何在组织这一舞台上演的。随着技术的不断进步,我们有理由相信,空间组学将成为下一代精准预测和治疗决策的核心支撑,开启精准肿瘤学的新纪元。
参考文献:
- Liu, Y., Dai, Y., & Wang, L. (2025). Spatial omics at the forefront: emerging technologies, analytical innovations, and clinical applications. Cancer Cell.
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-01-03,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

